
题目列表(包括答案和解析)
7.对处于化学平衡的体系,关于化学平衡与化学反应速率的关系正确的是
A.化学反应速率变化时,化学平衡一定发生移动
B.只有在催化剂存在下,才会发生化学反应速率变化而化学平衡不移动的情况
C.正反应进行的程度大,正反应速率一定大
D.化学平衡发生移动时,化学反应速率一定变化
6.现有下列各组溶液:
①10℃时10mL 0.1mol/L的Na2S2O3溶液和50mL0.1mol/L的H2SO4溶液;
②10℃时10mL 0.05mol/L的Na2S2O3溶液和l0 mL 0.1mol/L的H2SO4溶液;
③30℃时10mL 0.05mol/L的Na2S2O3溶液和10mL0.1mol/L的H2SO4溶液。
若同时将它们混合发生反应:Na2S2O3+ H2SO4≒Na2SO4+S↓++SO2↓+H2O,则出现浑浊的先后次序是
A.①②③ B.②①③ C.③②① D.①③②
5.下列反应的离子方程式书写不正确的是
A.向NaHCO3溶液中加入少量澄清的Ca(OH)2溶液:
2HCO3-+Ca2++2OH- = CaCO3↓+CO32-+2H2O
B.用碳酸钠溶液吸收少量二氧化硫:2CO32-+SO2+H2O=2HCO3-+SO32-
C.在饱和的苏打溶液里滴入少量盐酸:CO32-+2H+=CO2↑+H2O
D.过量二氧化碳通人偏铝酸钠溶液中:CO2+2H2O+AlO2-=Al(OH)3↓+HCO3-
4.欲除去含有1mol·L-1Mg(HCO3)2和2mol·L-1CaCl2的混合溶液中的Mg2+、Ca2+,选用下列一种试
剂适量即可,该试剂是
A.NaHCO3 B.Na2CO3 C.NaOH D.Ca(OH)2
3.下列各组物质反应后,含碳元属的物质既是氧化剂又是还原剂的是
A.CO2+Na 2O2 B.Mg+CO2 C.CaO+C D.CaCO3+SiO2
2.通入少量CO2,下列溶液能发生反应,但无明显现象的是
A.澄清石灰水 B.水玻璃 C.苯酚钠溶液 D. 苏打溶液
1.20世纪80年代后,人们发现和证实了碳的另一类单质,它们是由一系列偶数个碳原子组成的分子,其中C60(足球烯,分子中含有30个双键)最具代表性。下图所示为n个C60连接而成的物质X。下列有关说法不正确的是

A.常温常压下X为固态且难溶于水
B.一定条件下X可与Cl2发生加成反应
C.X是碳的一种同素异形体
D.X的摩尔质量为720n
18.(8分)恒温下,将a mol N2与b mol H2的混合气体通入一个固定容积的密闭容器中,发生如下反应:
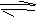 N2(g)+3H2(g)
2NH3(g)
N2(g)+3H2(g)
2NH3(g)
(1)若反应进行到某时刻t时,n(N2)=13mol,n(NH3)=6mol,则a= 。
(2)反应达到平衡时,混合气体的体积为 716.8L(标况下),其中NH3的含量(体积分数)为25%。则平衡时NH3的物质的量是 mol。
(3)原混合气体与平衡混合气体的总物质的量之比(写出最简整数比,下同)为n(始):n(平)= 。
(4)原混合气体中,a:b= 。
(5)达到平衡时,N2和H2的转化率之比,a(N2):a(H2)= 。
(6)平衡混合气体中,n(N2):n(H2):n(NH3)= 。
 17.(16分)教材实验设计也常存在不足,在学习过程中对
17.(16分)教材实验设计也常存在不足,在学习过程中对
其进行改进是研究性学习的一个重要课题。
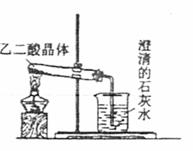
Ⅰ.草酸晶体(H2C2O4·2H2O)受热易分解(分解温
度为175℃),产生CO和CO2。右图为高三教材82
页关于草酸晶体受热分解及验证部分分解产物的实验
装置图。
(1)写出草酸晶体受热分解的化学方程式:
。
(2)该装置欲验证的分解产物是 。
(3)草酸晶体的某些物理性质如下表:
|
|
分子式 |
颜色、状态 |
水溶性 |
熔点/℃ |
密度/g·cm-3 |
|
草酸晶体 |
H2C2O4·2H2O |
无色晶体 |
易溶于水 |
101.5 |
1.650 |
有同学认为,用该装置进行实验,存在不合理因素,请分析指出(任答两点):
① 。
② 。
Ⅱ.下图甲是高一课本65页“铜丝在氯气中燃烧”的演示实验,铜丝在氯气中燃烧的主要现象是 。有人对该实验提出了如下改进方案:
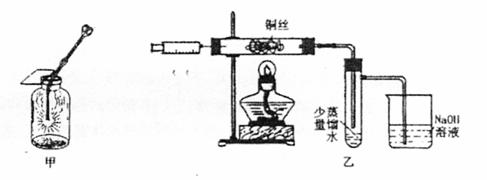 ①按下图乙所示连接好装置,并检查气密性:
①按下图乙所示连接好装置,并检查气密性:
②取下注射器并集满C12;
③点燃酒精灯加热1-2min后,再移开酒精灯。迅速将注射针插入石英玻璃管内,并将C12缓缓推入玻璃管中;
④拔出针头,再用同样的方法快速向玻璃管中推入空气。请回答:
(1)步骤③中,移开酒精灯、推入C12时,观察到铜丝继续保持红热状,由此可判断,该反应为 反应(填“放热”或“吸热”)
(2)步骤④完成后,发现乙试管中的蒸馏水变为蓝绿色。此时缓缓拉动针栓,使少量NaOH溶液吸入乙试管中,看到试管中有 色的沉淀产生,该反应的离子方程式为 。
(3)改进后的实验与课本实验相比较,其优点为 。
16.(14分)下表列出了①-⑨十种元素在周期表中前四周期的位置,请回答下列问题:
 主族族数 主族族数周期序数 |
IA |
ⅡA |
ⅢA |
IVA |
VA |
VIA |
VIIA |
O |
|
二 |
|
|
|
⑤ |
|
⑥ |
⑧ |
|
|
三 |
① |
③ |
④ |
|
|
⑦ |
|
⑩ |
|
四 |
② |
|
|
|
|
|
⑨ |
|
(1)在这十种元素形成的单质中化学性质最不活泼的是 ;(请具体元素的符号或化学式,下同)金属性最强的是 ;非金属性最强的是 。
(2)①、③两元素的氧化物对应的水化物中碱性强的是 ;(请具体物质的化学式,下同)⑤、⑦两元素的最高价氧化物对应的水化物中酸性强的是 。
(3)①、②、③三元素按原子半径由小到大的顺序排列为 。
(4)用电子式表示②、⑨两元素形成化合物的过程 。
(5)①的氧化物对应的水化物与⑦的氢化物反应的离子方程式,因物质的量配比不同产物有所不同,试分别写出有关反应的离子方程式 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com