
题目列表(包括答案和解析)
12.下列反应的离子方程式表示正确的是( )
A.碳酸氢钙溶液和氢氧化钠溶液混合:HCO3-+ OH- == CO32- + H2O
B.醋酸钠溶液和盐酸混合:CH3COONa + H+ == CH3COOH + Na+
C.少量金属钠放入冷水中:Na+ + 2H2O == Na+ + 2OH- + H2↑
D.硫酸铜溶液和氢氧化钡溶液混合:
Cu2+ + SO42- + Ba2+ + 2OH- == Cu(OH)2↓ + BaSO4↓
11.设NA代表阿伏加德罗常数,下列说法正确的是 ( )
A. 5.6 g铁与足量盐酸反应转移的电子数为0.3NA
B. 100 mL 2.0 mol/L的盐酸与醋酸溶液中氢离子均为0.2NA
C. 标准状况下,22.4 L氦气与22.4 L氟气所含原子数均为2 NA
D. 20 g重水(D2O)中含有的电子数为10NA
10.下列叙述正确的是 ( )
A. 发生化学反应时失去电子越多的金属原子,还原能力越强
B. 金属阳离子被还原后,一定得到该元素的单质
C. 核外电子总数相同的原子,一定是同种元素的原子
D. 能与酸反应的氧化物,一定是碱性氧化物
9.在25℃、101 kPa下,1 g甲醇燃烧生成CO2和液态水时放热22.68 kJ,下列热化学方程式正确的是 ( )
A.
CH3OH(l)+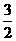 O2(g)=CO2(g)+2H2O(l) DH=+725.8 kJ / mol
O2(g)=CO2(g)+2H2O(l) DH=+725.8 kJ / mol
B. 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) DH=-1452 kJ / mol
C. 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) DH=-725.8 kJ / mol
D. 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) DH=+1452 kJ / mol
8.下列关于胶体的叙述不正确的是 ( )
A.布郎运动是胶体微粒特有的运动方式,可以据此把胶体和溶液、悬浊液区别开来
B.光线透过胶体时,会发生丁达尔效应
C.用渗析的方法净化胶体时,使用的半透膜只能让较小的分子、离子通过
D.胶体微粒具有较大的表面积,能吸附阳离子或阴离子,故在电场作用下会产生电泳现象
7.Se是人体必需微量 元素,下列有关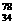 Se和
Se和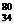 Se的说法正确的是
( )
Se的说法正确的是
( )
A、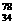 Se 和
Se 和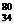 Se互为同素异形体
B、
Se互为同素异形体
B、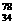 Se和
Se和 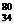 Se互为同位素
Se互为同位素
C、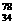 Se和
Se和 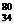 Se 分别含有44和46个质子 D、
Se 分别含有44和46个质子 D、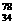 Se和
Se和 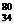 Se都含有34个中子
Se都含有34个中子
6.下列有关药品的保存或使用不正确的是
A、溴水盛于带磨砂玻璃塞的细口瓶中; B、硫酸铜粉末、氯化钙等药品贮存于干燥器中
C、白磷需浸入水中密封保存 D、用碳酸钠滴定盐酸时,Na2CO3溶液应盛于酸式滴定管中
5.在常温常压下呈气态的化合物,降温使其变成固体,得到的晶体属于( )
A.分子晶体 B.原子晶体 C.离子晶体 D.金属晶体
4.下列关于浓硫酸的叙述正确的是 ( )
A.浓硫酸具有吸水性,因而能使蔗糖炭化
B.浓硫酸在常温下可迅速与铜片反应放出二氧化硫气体
C.浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体
D.浓硫酸在常温下能够使铁、铝等金属钝化
3. 已知反应A2(g)+2B2(g) 2AB(g)的△H<0,下列说法正确的是 ( )
已知反应A2(g)+2B2(g) 2AB(g)的△H<0,下列说法正确的是 ( )
A.升高温度,正向反应速率增加,逆向反应速率减小
B.达到平衡后,升高温度或增大压强都有利于该反应平衡正向移动
C.升高温度有利于反应速率增加,从而缩短达到平衡的时间
D.达到平衡后,降低温度或减小压强都有利于该反应平衡正向移动
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com