
题目列表(包括答案和解析)
8、将氨水滴加到盛有AgC1的试管中,AgC1逐渐溶解,对上述过程,下列叙述或解释正确( )
A.所得溶液中c(Ag+)×c(C1-)<KSP(AgC1)B.所得溶液中形成了更难电离的物质
C.上述实验说明C1与NH4+间有很强的结合力 D.上述过程中NH3·H2O的电离程度增大
7、关于某无色溶液中所含离子的鉴别,下列判断正确的是 ( )
A.加入AgNO3溶液,生成白色沉淀,加稀盐酸沉淀不消失,可确定有Cl-存在
B.加入Ba(NO3)2溶液,生成白色沉淀,加稀盐酸沉淀不消失,可确定有SO42-存在
C.通入Cl2后,溶液变为黄色,加入淀粉溶液后溶液变蓝,可确定有I-存在
D.加盐酸,生成的气体能使澄清石灰水变浑浊,则原溶液中一定有大量CO32-
6、已知白磷(P4)与CuSO4溶液反应的化学方程式为:11P4+60CuSO4+96H2O == 20Cu3P+24H3PO4+60H2SO4,则1molCuSO4能氧化白磷的物质的量是 ( )
A.2/5mol B.1/5mol C.11/5mol D.1/20mol
5、NA为阿伏加德罗常数,下列说法中正确的是
A. 17gNH4+中含有的电子数为10NA
B. 1mol·L-1 Mg(NO3)2溶液中含有NO3-的数目为2NA
C. 标准状况下,22.4L甲苯所含的分子数为NA
D. 室温下,28.0g乙烯和丙烯中混合气体中含有的碳原子数为2NA
4、城市环境污染是当前突出的环境问题。如图A所示,X河流经某工业城市Y,其中a处在上游,附近有丰富的黄铁矿资源,d处在下游有多个企业以硫酸为原料。根据某月Y市环保局监测站对X河水质检测的结果,绘制成简图如图B所示。下列说法不正确的
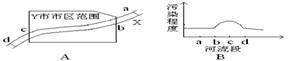
A.造成X河污染的主要污染源最可能分布在bc段
B.工业生活污水、固体废弃物等可能是造成X河污染的污染源
C.该城市建造硫酸厂时,综合考虑诸多因素选址在b处最合理。
D.d处污染程度减小,可能是某些污染物的离子间发生反应生成沉淀所致
3、化学实验中常将溶液或试剂进行酸化,下列酸化处理的措施正确的是
A.定性检验SO32-,将BaCl2溶液用HNO3酸化
B.为提高高锰酸钾溶液的氧化能力,用盐酸将高锰酸钾溶液酸化
C.检验溶液中是否含有Fe2+时,用硝酸酸化
D.检验溶液中是否含有SO42-时,在无其它阳离子干扰的条件下,用盐酸酸化的BaCl2溶液
2、下列说法或做法中正确的是
A.氟氯烃的大量排放是造成酸雨的主要原因
B.等质量的同种煤粉和煤块完全燃烧,放出热量前者大于后者
C.液氯泄漏事故发生时,周边的人应该朝顺风方向逃逸或向避风的沟塘低洼处转移
D.火箭发动机有偏二甲肼(C2H8N2)与N2O4混合后充分燃烧,可生成CO2、N2和H2O
1.化学与科技、社会、生产密切结合,下列有关说法不正确的是
A.“乙醇汽油”的广泛使用能有效减少有害气体的排放
B.“无磷洗涤剂”的推广使用,能有效减少水体富营养化的发生
C.“无氟冰箱”取代“含氟冰箱”,对人类的保护伞--臭氧层起到保护作用
D.“海水淡化”可以解决“淡水供应危机”,向海水中加入净水剂明矾可以使海水淡化
24、 标准状况下,用一定量的水吸收氨气后制得浓度为12.0mol/L,密度0.915g/cm3的氨水,试计算1体积水吸收 体积的氨气可制得上述氨水。(本题中氨的相对分子质量为17.0,水的密度为1.00 g/cm3)
23、(1) BrCl3性质与卤素单质相似,具有很强的氧化性。将BrCl3溶与水,再通人SO2。写出该反应的化学方程式:_________________________________________________________
(2)若将4.66gBrCln溶于水, 再通人SO2反应后,将反应溶液调节至中性,并加入过量Ba(NO3)2,除去沉淀后,所得溶液再用过量AgNO3溶液处理,得到15.46g沉淀,试确定BrCln中的n值为____________。
(3)将10.08g铁粉溶于过量的稀硫酸,所得溶液中加入5.05gKNO3氧化溶液中的Fe2+,待反应完毕后,剩余的Fe2+尚需30 mL 0.5mol/L的溴水才能全部氧化,试写出三步反应的化学方程式。(按反应先后顺序写)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com