
题目列表(包括答案和解析)
6.阿伏加德罗常数约为6.02×1023mol-1,下列说法中正确的是
A.实验室制得的46克NO2在标准状况下该气体体积为22.4L
B.新戊烷与异戊烷的混合物7.2g中所含共价键数目为1.6×6.02×1023
C.通常状况下0.6g氧气和1.0g臭氧(O3)组成的混合气体中含氧原子数小于6.02×1022
D.7.1g氯气与足量石灰乳充分反应转移电子数为0.2×6.02×1023
5.下列说法中正确的是
A.酸性氧化物都是非金属氧化物
B.含有极性键的分子一定是极性分子
C.含有离子键的化合物一定是离子化合物
D.所有物质中都存在化学键
4.下列说法正确的是
A.H2O和D2O互为同位素
B.乙醇和乙二醇互为同分异构体
C.C2H4和C3H6一定属于同系物
D.新戊烷和2,2-二甲基丙烷属于同一种物质
3.下列叙述正确的是
A.碘在碘化钾溶液中溶解度显著增大,原因是发生氧化还原反应生成I3-
B.氯化铁溶液遇KSCN溶液显红色,原因是生成Fe(SCN)3沉淀
C.氢氟酸需保存在塑料瓶中,原因是氢氟酸具有强酸性而腐蚀玻璃
D.氯化银难溶于水而溶于氨水,原因是生成Ag(NH3)2Cl
2.分类是学习和研究化学的一种常用的科学方法。下列分类合理的是
① 根据酸分子中含有的H原子个数将酸分为一元酸、二元酸等
② 根据反应中是否有电子的转移将化学反应分为氧化还原反应和非氧化还原反应
③ 根据电解质在熔融状态下能否完全电离将电解质分为强电解质和弱电解质
④ 根据元素原子最外层电子数的多少将元素分为金属和非金属
⑤ 根据反应的热效应将化学反应分为放热反应和吸热反应
A.②⑤ B.②③ C.①②④ D.②③④⑤
1.2006年9月21日,美国亚特兰蒂斯号航天飞机在爱德华空军基地安全着落,航天飞机
表层的防热瓦曾成为航天飞机能否安全着落的制约因素。防热瓦是以石墨材料为主要成
分的非常疏松的泡沫陶瓷。下列有关说法合理的是
A.石墨成为该泡沫陶瓷主要成分的主要原因是石墨是原子晶体
B.石墨成为该泡沫陶瓷主要成分的主要原因是石墨熔点很高
C.石墨中碳碳键之间的夹角为109°28'
D.C60也可代替石墨用作航天飞机表层的防热瓦材料
22.(物质结构与性质,12分)
氢是新型清洁能源,但难储运。研究发现,合金可用来储藏氢气。镧(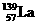 ) 和镍(
) 和镍(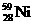 ) 的一种合金就是储氢材料。该合金的晶胞如右图,镍原子除一个在中心外,其他都在面上,镧原子在顶点上。储氢时氢原子存在于金属原子之间的空隙中。
) 的一种合金就是储氢材料。该合金的晶胞如右图,镍原子除一个在中心外,其他都在面上,镧原子在顶点上。储氢时氢原子存在于金属原子之间的空隙中。
(1)一定条件下,该贮氢材料能快速、可逆地存储和释放氢气,若每个晶胞可吸收 3 个 H2, 这一过程用化学方程式表示为: 。
(2)下列关于该贮氢材料及氢气的说法中,正确的是 ( 填序号 )
A.该材料中镧原子和镍原子之间存在化学键,是原子晶体
B.氢分子被吸收时首先要在合金表面解离变成氢原子,同时放出热量
C.该材料贮氢时采用常温高压比采用常温常压更好
D.氢气很难液化是因为虽然其分子内氢键很强,但其分子间作用力很弱
E.己知镧和镍的第一电离能分别为 5.58eV、7.64eV, 可见气态镧原子比气态镍原子更容易变成+1 价的气态阳离子
(3)某研究性学习小组查阅的有关镍及其化合物的性质资料如下:

①写出 Ni3+ 的核外电子排布式:
②写出将NiO(OH) 溶于浓盐酸的离子方程式:
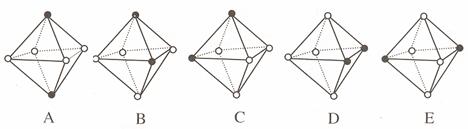
(4)Ni(CO)6为正八面体结构,镍原子位于正八面体的中心,配位体CO在正八面体的六个顶点上。若把其中两个CO配位体换成 NH3 得到新的配合物,则以下物质中互为同分异构体的是 。 ( 填字母编号,任填一组 )( 图中黑点为NH3,圆圈为CO,Ni略去)
21.(8分)为研究水滑石的组成、结构和性质,某校研究性学习小组取得了二种牌号的水滑石样品拟进行探究,请你参与探究并回答相关问题。
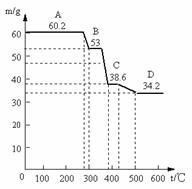 (1)甲同学取天然水滑石样品进行恒重分析,已知天然水滑石的化学式可表示为:6MgO·Al2O3·CO2·12H2O,取0.1mol水滑石进行加热时,温度与剩余固体质量的关系如下图,平行线上的数字表示残留固体的质量。
(1)甲同学取天然水滑石样品进行恒重分析,已知天然水滑石的化学式可表示为:6MgO·Al2O3·CO2·12H2O,取0.1mol水滑石进行加热时,温度与剩余固体质量的关系如下图,平行线上的数字表示残留固体的质量。
当温度在0-280℃质量不变,是什么原因: 。
A→B减少的物质及其物质的量为: ;
C→D减少的物质及其物质的量为: ;
D处化学组成为: 。
(2)乙组取的CA(美国化学文摘)登记号为12304-65-3 的合成水滑石样品,现只知其化学式为:MgaAlb(OH)C(CO3)d, a+b+c+d=25, a、b、c、d为正整数。取该水滑石样品0.1mol,用1mol/L盐酸使其完全溶解。
①消耗盐酸的体积至少为: L(用字母表示);
②若参加反应的盐酸的物质的量与生成CO2的物质的量之比为18∶1,则该水滑石的化学式为: 。
20.(12分)有机化学反应因反应条件不同,可生成不同的有机产品。例如:
(1) (X为卤素原子)
(X为卤素原子)
 (2)苯的同系物与卤素单质混合,若在光照条件下,侧链上氢原子被卤素原子取代;若在催化剂作用下,苯环上的氢原子被卤素原子取代。
(2)苯的同系物与卤素单质混合,若在光照条件下,侧链上氢原子被卤素原子取代;若在催化剂作用下,苯环上的氢原子被卤素原子取代。
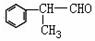
工业上利用上述信息,按下列路线合成结构简式为 的物质,该物质是一种香料。
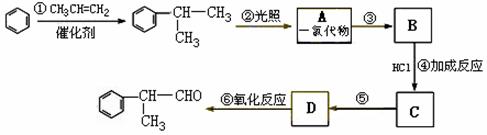
请根据上述路线,回答下列问题:
(1)A的结构简式可能为 和 。
(2)反应①、③、⑤的反应类型分别为 、 、 。
(3)反应④的化学方程式为(有机物写结构简式,并注明反应条件)
。
(4)这种香料具有多种同分异构体,其中某些物质有下列特征:①其水溶液遇FeCl3溶液呈紫色 ②分子中有苯环,且苯环上的一溴代物有两种。写出符合上述条件的物质可能的结构简式(只写两种):
。
19.(10分)某活动课程小组拟用50mLNaOH溶液吸收CO2气体,制备Na2CO3溶液。为了防止通入的CO2气体过量生成NaHCO3,设计了如下实验步骤:
a.取25 mL NaOH溶液吸收过量的CO2气体,至CO2气体不再溶解;
 b.小火煮沸溶液1-2 min;
b.小火煮沸溶液1-2 min;
c.在得到的溶液中加入另一半(25mL)NaOH溶液,使其充分混合反应。
(1)此方案能制得较纯净的Na2CO3,写出a、c两步的化学反应方程式 ____________________、____________________________。
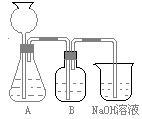
此方案第一步的实验装置如下图所示:
(2)加入反应物前,如何检查整个装置的气密性________________________________________。
(3)装置B中盛放的试剂是______________,作用是_______________________________。
 (4)在实验室通常制法中,装置A还可作为下列_____________气体的发生装置(填序号)。
(4)在实验室通常制法中,装置A还可作为下列_____________气体的发生装置(填序号)。
①CH2==CH2 ②H2S ③CH4 ④CH≡CH ⑤H2
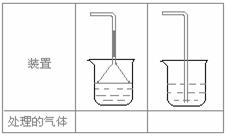
(5)实验室制取下列气体:①NH3,②Cl2,③HCl,④H2S,⑤CH4, ⑥CO,⑦CO2,⑧O2时,属于必须进行尾气处理,并能用下图所示装置进行处理的,将气体的序号填入装置图的下方空格内。
(6)已知所用NaOH溶液中溶质的质量分数为40%,室温下该溶 液密度为1.44 g / mL,假设反应前后溶液的体积不变,不考虑实验误差,计算用此种方法制备所得Na2CO3溶液的物质的量浓度为____________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com