
题目列表(包括答案和解析)
18、(11分)用石墨电极电解200mL0.5mol/L的NaCl溶液,阳极收集到2.24L(标准状况)气体时,停止通电。请回答以下问题:
(1)电解过程中阳极的电极反应分别为 、 ;
(2)阴极生成的气体体积为 L(标准状况);
(3)若将阳极生成的气体通入电解后的溶液中,充分反应后,则所得溶液中离子的浓度由
大到小依次是 ;
(4)常温下,若将电解后的稀溶液稀释至1L,则溶液的pH约为 ;
(5)若将电解后阳极所产生的气体全部通入1mol/L500mLNa2SO3的溶液中,使之充分反应(假设溶液的体积变化忽略不计),则所得溶液中SO42-的物质的量浓度最多为 mol/l
选修四第四章电化学基础单元检测题
第Ⅰ卷 选择题
1C 2B 3B 4C 5D 6C 7B 8B 9C 10C 11B 12D
17、(2分)从NO3-、SO42-、Cl-、H+、Cu2+、Ba2+、Ag+等离子中选出适当的离子组成电解质,采用惰性电极对其溶液进行电解。若两极分别放出气体,且体积比为1∶1,电解质的化学式可能是 。
16、 (12分)工业上处理含Cr2O72-的酸性工业废水用以下方法:①往工业废水中加入适量的NaCl,搅拌均匀;②用Fe为电极进行电解,经过一段时间有Cr(OH)3和Fe(OH)2沉淀产生;过滤回收沉淀,废水达到排放标准。试回答:
(12分)工业上处理含Cr2O72-的酸性工业废水用以下方法:①往工业废水中加入适量的NaCl,搅拌均匀;②用Fe为电极进行电解,经过一段时间有Cr(OH)3和Fe(OH)2沉淀产生;过滤回收沉淀,废水达到排放标准。试回答:
⑴ 电解时的电极反应: 阳极______________ ,阴极______________ 。
⑵ Cr2O72-转变成Cr3+的离子反应方程式
⑶ 电解过程Cr(OH)3和Fe(OH)3沉淀是怎样产生的?
⑷ 能否用Cu电极来代替Fe电极?______________(填“能”或“不能”),简述理由。
15、(8分)宇宙飞船上的氢氧燃料电池,其电池反应为:2H2+O2=2H2O 试写出:
(1)电解质溶液若为硫酸时的负极反应式
正极反应式_____________________ 。
(2)电解质溶液若为氢氧化钾溶液时的负极反应式
正极反应式_____________________ 。
14、(12分)如图所示,组成一个原电池.
 (1)当电解质溶液为稀硫酸时:
①Fe电极是__________(填“正”或“负”)极,其电极反应为________________________,
(1)当电解质溶液为稀硫酸时:
①Fe电极是__________(填“正”或“负”)极,其电极反应为________________________,
该反应是__________(填“氧化”或“还原”下同)反应; ②Cu电极是__________电极,其电极反应为______________________
该反应是__________反应.
(2)当电解质溶液为稀硝酸时:
①Fe电极是_____极,其电极反应为__________ ,该反应是_____ 反应.
分数 姓名 班级
②Cu电极是_____极,其电极反应为__________ ,该反应是_____ 反应.
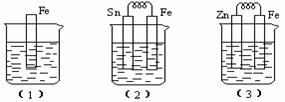
13、(7分)如下图所示,烧杯中都盛有稀硫酸。
(1)中反应的离子方程式为
(2)中的电极反应:Fe:
、Sn:
Sn极附近溶液的pH(填增大、减小或不变)
(3)中被腐蚀的金属是
、其电极反应式为
。
比较(1)、(2)、(3)中纯铁被腐蚀的速率由快到慢的顺序是
。
12、用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,向所得溶液加入0.2mol CuO,恰好恢复到电解前的浓度和pH。则电解过程中转移电子的物质的量为( )
A.0.1mol B.0.2mol C.0.3mo1 D.0.4mol
第Ⅱ卷(非选择题 共52分)
11、下列四种装置中,溶液的体积均为250 mL,开始时电解质溶液的浓度均为0.10摩/升,工作一段时间后,测得导线上均通过0.02 mol电子,若不考虑溶液体积的变化,则下列叙述正确的是( )

A、 工作一段时间后溶液的浓度①=②=③=④
B、 工作一段时间后溶液的pH值:④>③>①>②
C、 产生气体的总体积:④>③>①>②
D、 电极上析出的固体的质量:①>②>③>④
10、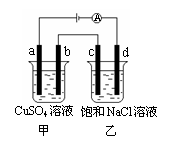 如图所示,a、b、c、d均为石墨电极,通电进行电解。下列说法正确的是( )
如图所示,a、b、c、d均为石墨电极,通电进行电解。下列说法正确的是( )
A.乙烧杯中d的电极反应为 2Cl––2e– =Cl2↑
B.a、c两极产生气体的物质的量相等
|
2NaCl + 2H2O  2NaOH + H2↑+ Cl2↑
2NaOH + H2↑+ Cl2↑
D.甲、乙两烧杯中溶液的pH均保持不变
9、 有关右图装置中的叙述正确的是 (
)
有关右图装置中的叙述正确的是 (
)
A.这是电解NaOH溶液的装置
B.这是一个原电池装置,利用该装置可长时间的观察到 Fe(OH)2 沉淀的颜色
C.Pt为正极,其电极反应为:O2+2H2O +4e-=4OH-
D.Fe为阳极,其电极反应为:Fe-2e-+2OH-=2Fe(OH)2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com