
题目列表(包括答案和解析)
31.(10分)按要求对下图中两极进行必要的联接并填空:
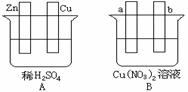
(1)在A图中,使铜片上冒H2气泡。请加以必要联接,则联接后的装置叫 。电极反应式:锌板: ;铜板: 。
(2)在B图中,使a极析出铜,则b析出: 。加以必要的联接后,该装置叫
。电极反应式,a极: b极: 。经过一段时间后,停止反应并搅均溶液,溶液的pH值 (升高、降低、不变),加入一定量的 后,溶液能恢复至与电解前完全一致。
30、 (6分)分析右图,按要求写出有关反应方程式:
(6分)分析右图,按要求写出有关反应方程式:
(1)、铁棒上的电极反应式为: ;
(2)、碳棒上的电极反应式为: ;
(3)、溶液中发生反应的化学方程: 。
29、(7分)煤燃烧的反应热可通过以下两个途径来利用:a.利用煤在充足的空气中直接燃烧产生的反应热;b.先使煤与水蒸气反应得到氢气和一氧化碳。然后是使得到的氢气和一氧化碳在充足的空气中燃烧。这两个过程的化学方程式为:
a.C(s)+ O2(g) = CO2(g) △H=E1 ①
b.C(s) + H2O(g) = CO(g)+ H2(g) △H=E2 ②
H2(g)+ 1/2 O2(g) = H2O(g) △H=E3 ③
CO(g)+ 1/2 O2(g) = CO2(g) △H=E4 ④
回答:
⑴与途径a相比途径b有较多的优点,即______ _________.
⑵上述四个热化学方程式中哪个反应△H >0?________________
⑶等质量的煤分别通过以上两条不同的途径产生的可利用的总能量关系正确的是( )
A、a比b多 B、a比b少 C、a与b在理论上相同
⑷根据能量守恒定律,E1、E2、E3、E4之间的关系为____________
28. (7分)中和热是指酸跟碱发生中和反应生成lmol H2O所放出的热量。某学生想通过测定反应过程中所放出的热量来计算中和热。他将50mL0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应。请回答下列问题:
(7分)中和热是指酸跟碱发生中和反应生成lmol H2O所放出的热量。某学生想通过测定反应过程中所放出的热量来计算中和热。他将50mL0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应。请回答下列问题:
(1) 从实验装置上看,图中尚缺少的一种玻璃用品是__________________,烧杯间填满碎塑料泡沫的作用是______________ ___________________。
(2) 大烧杯上如不盖硬纸板,则求得的中和热数值_______(填“偏大”、“偏小’、“无影响”)
(3) 实验中改用60 mL 0.50 mol/L的盐酸跟50mL 0.55 mol/L的NaOH溶液进行反应,
与上述实验相比,所放出的热量________(填“相等”或“不相等”),理由是____________
___________________________________;所求中和热的数值会________(填“相等”
或“不相等”),理由是__________________________________________________。
第Ⅱ卷(非选择题,共46分)
27.金属镍有广泛的用途。粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍,下列叙述正确的是(已知:氧化性Fe2+<Ni2+<Cu2+)( )
A. 阳极发生还原反应,其电极反应式:Ni2++2e- =Ni
B. 电解过程中,阳极质量的减少与阴极质量的增加相等
C. 电解后,溶液中存在的金属阳离子只有Fe2+和Zn2+
D. 电解后,电解槽底部的阳极泥中只有Cu和Pt
班级 学号 姓名
26.某同学为了使反应2HCl
+ 2Ag 2AgCl
+ H2↑能进行,设计了下列四个实验,如下图所示,你认为可行的方案是( )
2AgCl
+ H2↑能进行,设计了下列四个实验,如下图所示,你认为可行的方案是( )

24.一种新型燃料电池,一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-。下列对该燃料电池说法正确的是( )
A.在熔融电解质中,O2-由负极移向正极
B.通入丁烷的一极是正极,电极反应为:2C4H10+26e-+13O2-=4CO2+5H2O
C.通入空气的一极是负极,电极反应为:O2+4e-=2O2-
D.电池的总反应是:2C4H10+13O2 ® 8CO2+10H2O
25
|
A.A池为电解池,B池为原电池
B.D、E两极都发生氧化反应
C.E极应为粗铜板材料
|
 D.B池中E极质量增加12.8g
D.B池中E极质量增加12.8g23、.用铂电极电解CuSO4和KNO3的混合液500mL,经过一段时间后,两极均得到标况下11.2L气体,则原混合液中CuSO4的物质的量浓度为( )
A.0.5mol·L-1 B.0.8mol·L-1 C.1.0mol·L-1 D.1.5mol·L-1
22. (07上海).用一张已除去表面氧化膜的铝箔紧紧包裹在试管外壁(如右图),将试管浸入硝酸汞溶液中,片刻取出,然后置于空气中,不久铝箔表面生出“白毛”,红墨水柱右端上升。根据实验现象判断下列说法错误的是
(07上海).用一张已除去表面氧化膜的铝箔紧紧包裹在试管外壁(如右图),将试管浸入硝酸汞溶液中,片刻取出,然后置于空气中,不久铝箔表面生出“白毛”,红墨水柱右端上升。根据实验现象判断下列说法错误的是
A 实验中发生的反应都是氧化还原反应
B 铝是一种较活泼的金属,
C 铝与氧气反应放出大量的热量
D 铝片上生成的白毛是氧化铝和氧化汞的混合物
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com