
题目列表(包括答案和解析)
23.把Cl2通入氨水中发生如下反应:3Cl2+8NH3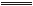 6NH4Cl+N2↑,当逸出的气体中含有0.28 g N2时,反应中被氧化的氨的质量是________________
6NH4Cl+N2↑,当逸出的气体中含有0.28 g N2时,反应中被氧化的氨的质量是________________
22.(12分)实验室用浓盐酸、二氧化锰共热制氯气,并用氯气和Ca(OH)2制取少量漂白粉。现已知反应:2Cl2+2Ca(OH)2===Ca(ClO)2+CaCl2+2H2O,该反应是放热反应,温度稍高即发生副反应:6Cl2+6Ca(OH)2===Ca(ClO3)2+5CaCl2+6H2O。现有三个同学分别设计的三套实验装置如下图:
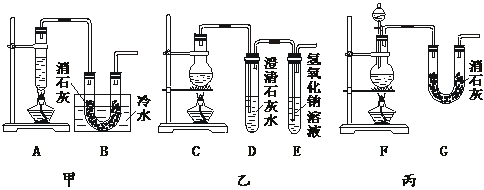 (1)写出制取氯气的化学方程式:_______________________________。
(1)写出制取氯气的化学方程式:_______________________________。
(2)请从以下几个方面对甲、乙、丙三套实验装置的优缺点作出评价,并将符合题目要求的选项的序号填在表中空格内。a 不容易控制反应速率 b.容易控制反应速率 c.有副反应发生 d.可防止副反应发生 e.污染环境 f.可防止污染环境
|
|
优点 |
缺点 |
|
甲装置 |
|
|
|
乙装置 |
|
|
|
丙装置 |
|
|
(3)上述装置中,甲由A、B两部分组成,乙由C、D、E三部分组成,丙由F、G两部分组成。请从上述装置中选取合理的部分,组装一套较完整的实验装置,装置各部分连接顺序是__________________。该组合中还缺少的装置是_________________________________________________________,原因是___________________________________________________________。
21.(5分)某化学兴趣小组按照下列方案进行“由含铁废铝制备硫酸铝晶体”的实验:
步骤1:取一定量含铁废铝,加足量的NaOH溶液,反应完全后过滤。
步骤2:边搅拌边向滤液中滴加稀硫酸至溶液的pH=8-9,静置、过滤、洗涤。
步骤3:将步骤2中得到的固体溶于足量的稀硫酸。
步骤4:将得到的溶液蒸发浓缩、冷却、结晶、过滤、干燥。
请回答以下问题:
⑴上述实验中的过滤操作需要玻璃棒、______________、______________等玻璃仪器。
⑵步骤1过滤的目的是__________________________________________。
⑶当步骤2中的溶液pH=8-9时,检验沉淀是否完全的方法是______________。
⑷步骤2中溶液的pH控制较难操作,可改用____________________。
20.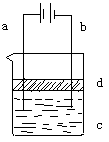 (9分)由于Fe(OH)2极易被氧化,所以实验室很难用亚铁盐溶液与烧碱溶液反应制得白色、纯净的Fe(OH)2沉淀。可用如右下图所示电解实验来制得Fe(OH)2沉淀。两电极的材料分别为铁和石墨。
(9分)由于Fe(OH)2极易被氧化,所以实验室很难用亚铁盐溶液与烧碱溶液反应制得白色、纯净的Fe(OH)2沉淀。可用如右下图所示电解实验来制得Fe(OH)2沉淀。两电极的材料分别为铁和石墨。
⑴ a电极材料应为_________,电极反应式为_____________。
⑵ 电解液c可以是___________(选填编号)
A.纯水 B.NaCl溶液 C.NaOH溶液 D.CuCl2溶液
⑶ d是苯,其作用为__________________________,在加入苯之前应对c溶液进行如何处理?_______________________________。
⑷ 为了在较短时间内看到白色沉淀,可采取的措施是_____(选填编号)
A.改用稀硫酸做电解液 B.适当增加电源的电压
C.适当减小两电极间距离 D.适当降低电解液的温度
⑸ 若c用硫酸钠溶液,当电解一段时间看到白色Fe(OH)2沉淀后,再反接电源电解,除在电极上可以看到气泡外,混合物中另一明显现象为________________________________________________________________。
19.(5分)下图是以黄铁矿为开始反应物的一系列变化,其中不含硫的反应产物已略去。

(1)写出化学式:A________。
(2)写出化学方程式:⑤___________________________________。
(3)写出离子方程式:②__________________________________。
18.(5分)某化学反应的反应物和产物如下:
KMnO4+KI+H2SO4 MnSO4+I2+KIO3+K2SO4+H2O
MnSO4+I2+KIO3+K2SO4+H2O
(1)该反应的氧化剂是____________。
(2)如果该反应方程式中I2和KIO3的化学计量数都是5
①KMnO4的化学计量数是____________。
②在下面的化学式上标出电子转移的方向和数目
KMnO4+ KI+ H2SO4
(3)如果没有对该方程式中的某些化学计量数作假定,可能的配平化学计量数有许多组,原因是____________________________________________________。
17.(6分)在①渗析 ②盐析 ③聚沉 ④溶胶 ⑤凝胶 ⑥布朗运动 ⑦电泳 ⑧丁达尔效应 ⑨中和 ⑩水解 中选出适当的词语填入下列每小题的空格中(填编号)。
(1)在肥皂水中透过强光,从侧面可以见到光带。这种现象称为____________;
(2)在浓肥皂水中加入饱和食盐水(或固体食盐的细粒)使肥皂聚沉。这种现象称为______________________;
(3)热的浓肥皂水使之冷却并全部固化后的物质叫_________________;
(4)在肥皂水中加入酚酞变成红色,说明高级脂肪酸根离子发生了_________;
(5)在Fe(OH)3胶体中加入(NH4)2SO4,产生红褐色沉淀,这种现象叫做_________________;
(6)用半透膜把制取的Fe(OH)3胶体中含有的NaCl分离出去的方法叫做_______。
16.某结晶水合物的分子式为R·nH2O其相对分子质量为M,在25℃时,a g该晶体溶于b g水中,即达到饱和,形成V mL密度为d g/cm3的溶液。下列表达式中正确的是
A.该饱和溶液的物质的量浓度为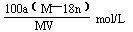
B.25℃时,R的溶解度为
C.该饱和溶液的物质的量浓度为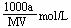
D.该饱和溶液的质量分数为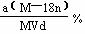
15.在吸收塔用98.3%的浓硫酸而不是用水吸收SO3的原因是
A.用水不能吸收SO3 B.用水吸收生成的酸雾多,影响吸收
C.用浓硫酸吸收不形成酸雾,吸收速率快 D.用浓硫酸吸收可以得到更浓的硫酸
14.下图中验证氯化钠溶液(含酚酞)电解产物的装置是

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com