
题目列表(包括答案和解析)
16、下图表示各物质之间的转化关系。
已知:常温下D、E、F、I、J为气体;C的焰色反应为黄色;M为有颜色的固体。
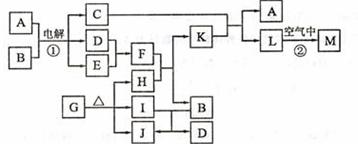
(1)写出:A的电子式 ,J的结构式 ,M的化学式 。
(2)基于反应①原理的化学工业称为 ,写出该反应的化学方程式 。
(3)写出K和E反应的离子方程式 。
写出F溶液和H反应的离子方程式 。
(4)已知由G分解得到的H、I、J三者的物质的量相等,则G的化学式为 。
15、贮气袋中存有有色气体,可能是NO2、CH4、CO2、HCl、NH3、Br2蒸气等气体中的几种,进行以下操作:①通少许于水中,得无色溶液;②通少许于AgNO3溶液中,有沉淀产生;③通少许于澄清石灰水中,无浑浊现象;④通过装有水的洗气瓶中,导出的气体再通入澄清石灰水,产生浑浊。则:由①可判断,一定存在_________;一定不存在________。由②可判断,一定存在_________;一定不存在_________.由③、④可判断,一定存在________;可能存在的是________。
14、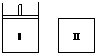 如图,Ⅰ是恒压密闭容器,Ⅱ是恒容密闭容器。其它条件相同时,在Ⅰ、Ⅱ中分别加入2mol X和2mol Y,起始时容器体积均为V L,发生如下反应并达到平衡(X、Y状态未知):2X(?)+Y(?)
如图,Ⅰ是恒压密闭容器,Ⅱ是恒容密闭容器。其它条件相同时,在Ⅰ、Ⅱ中分别加入2mol X和2mol Y,起始时容器体积均为V L,发生如下反应并达到平衡(X、Y状态未知):2X(?)+Y(?) aZ(g)。此时Ⅰ中X、Y、Z的物质的量之比为1∶3∶2,则下列说法一定正确的是
aZ(g)。此时Ⅰ中X、Y、Z的物质的量之比为1∶3∶2,则下列说法一定正确的是
A.若X、Y均为气态,则平衡时气体平均摩尔质量:Ⅰ>Ⅱ
B.若X、Y不均为气态,则平衡时气体平均摩尔质量:Ⅰ>Ⅱ
C.若X为固态,Y为气态,则Ⅰ、Ⅱ中从起始到平衡所需时间相同
D.平衡时Ⅰ容器的体积小于VL
非选择题部分(72分)
12、在10mL0.1mol·L-NaOH溶液中加入同体积、同浓度的HAc溶液,反应后溶液中各微粒的浓度关系正确的是
A.c(Na+)>c(Ac-)>c(H+)>c(OH-)
B.c(Na+)=c(Ac-)>c(OH-)=c(H+)
C.c(OH-)=c(H+)+c(HAc)
 D.2c(Na+)+c(H+)=2c(Ac-)+c(OH-)+c(HAc)
D.2c(Na+)+c(H+)=2c(Ac-)+c(OH-)+c(HAc)
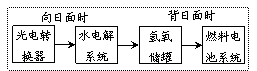
13右图是某空间站能量转化系统的局部
示意图,其中燃料电池采用KOH为电解液,
下列有关说法中不正确的是
A.该能量转化系统中的水也是可以循环的
B.燃料电池系统产生的能量实际上来自于水
C.水电解系统中的阴极反应:O2+2H2O+4e-=4OH-
D.燃料电池放电时的负极反应:H2-2e-+2OH-=2H2O
11、下列离子方程式正确的是
A.将0.1mol/L HCl溶液数滴缓缓滴入1mol/L 50mL Na3PO4溶液中,且不断搅拌
3H++PO43-=H3PO4
B.将1mol/L NaAlO2溶液和1.5mol/L的HCl溶液等体积互相均匀混合
6AlO2-+9H++3H2O=5Al(OH)3↓+Al3+
C.向1mol/L明矾溶液50mL中滴入数滴0.1mol/L Ba(OH)2溶液
Al3++2SO42-+2Ba2++3OH-=Al(OH)3↓+2BaSO4↓
D.将少量SO2气体通入NaClO溶液中:SO2+H2O+ClO-=SO42-Cl-+2H+
10、鸦片最早用于药物(有止痛、止泻、止咳作用),长期服用
会成瘾。现有鸦片的替代品用于脱瘾治疗,结构如下:
 1mol该化合物完全燃烧耗O2的物质的量、与NaOH溶液作
1mol该化合物完全燃烧耗O2的物质的量、与NaOH溶液作
用消耗NaOH的物质的量、其苯环上的一溴代物的种数分别是
A.26 mol、4 mol、7 mol B.24 mol、4 mol、8 mol
C.26 mol、5 mol、7 mol D.24 mol、5 mol、8 mol
9、右表为元素周期表短周期的一部分。下列有关A、B、C、D、E五种元素的叙述中,不正确的是
A .A与B形成的阴离子可能有:AB32-、A2B42-
 B .E的氢化物的沸点比C的氢化物的沸点高
B .E的氢化物的沸点比C的氢化物的沸点高
C .D在过量的B中燃烧的主要产物为DB3
D.这5种元素形成只含极性键的非极性分子多于5种
8、半导体工业用石英砂做原料通过三个重要反应生产单质硅
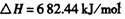
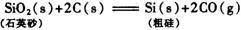


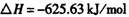
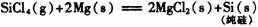
生产1.00kg纯硅的总反应热为:
A.2.43 × 104 kJ B.-2.35 × 104 kJ C.-2.23 × 104 kJ D.-2.14× 104 kJ
7、类推的思维方式在化学学习与研究中经常采用,但类推出的结论是否正确最终要经过实践的验证。以下类推的结论正确的是
A.由甲酸可以发生银镜反应可推出其余的羧酸也均能发生银镜反应
B.NaCl与CsCl化学式相似,故NaCl与CsCl的晶体结构也相似
C.由“2Fe+3Cl2=2FeCl3”反应可推出“2Fe+3I2=2FeI3”反应也能发生
D.Na、K具有强还原性,Na常温下与水剧烈反应,故K常温下也能与水剧烈反应
6、用NA表示阿伏加德罗常数的值,下列说法中正确的是
A.100mL 1mol/L FeCl3溶液中含阳离子数为0.1NA
B.常温常压下1 mol NO2气体与水反应生成NA个NO3-离子
C.0.6 g CaCO3与Mg3N2的混合物中所含质子数为0.3NA
D.80mL 10mol/L浓盐酸与足量MnO2反应,转移电子数为0.4NA
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com