
题目列表(包括答案和解析)
3.下列关于电解质知识的叙述,正确的是
A.Cl2 的水溶液能导电,但Cl2 是非电解质
B.0.1mol/L的氨水可以使酚酞试液变红,说明氨水是弱电解质
C.给pH=12的NaOH溶液通电一段时间后溶液的pH > 12
D.中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同
2.下列选项与胶体知识无关的是
A.在豆浆里加入盐卤做豆腐
B.水泥、冶金厂常用高压电除去工厂烟尘,以减少对空气污染
C.一束平行光线照射暗箱中的蛋白质溶液时,从侧面可以看到光亮的通路
D.氯化铝溶液中加入小苏打溶液会产生白色沉淀和气体
1.下列叙述正确的是
A.目前加碘食盐中主要添加的KIO3
B.日常生活中无水乙醇常用于杀菌消毒
C.绿色食品是不含化学物质的食品
D.空气质量日报中CO2含量属于空气污染指数
24、本题有3小题,每题2分:
(1)若1 mol某烃充分燃烧耗氧6 mol,则此有机物的分子式为 。
(2)若4.4g某烃的衍生物完全燃烧生成8.8gCO2和3.6gH2O,则该有机物的实验式为
。
(3)若某烃的衍生物中,碳的质量分数为60.0%,氢的质量分数为13.33%,则该有机物的分子式为 。
|
|
|
|
|
题 |
|
名 姓 |
答 |
|
|
准 |
|
号 座 |
不 |
|
|
内 线 |
|
级 班 |
封 |
|
|
密 |
|
|
|
第一学期期末考试
22.(11分)A、B、C、D、E、F六种物质在一定条件下有如下图所示的相互转化关系,所有反应物和生成物均已给出。
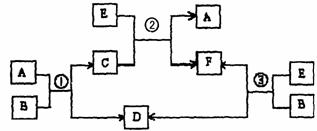
(1)若反应①、②、③均为溶液中的置换反应,A、D、E为第ⅦA族元素单质。则A、D、E的氧化性由强到弱的顺序为(用字母表示) ,其中A的化学式是 。
(2)若B是某元素R的氢化物,B的沸点大于与R同主族的其他元素氢化物的沸点,且B在常温下为液态;C是一种有磁性的化合物;E是一种无色、无味的有毒气体。则反应①的化学方程式 ,③的化学方程式 。
(3)若B由短周期元素X、Y组成,且X、Y原子个数比为1:1,B晶体中既含有离子键,又含非极性共价键;绿色植物的光合作用和呼吸作用可实现自然界中D、E的循环。则B的电子式为 ,反应①的离子方程式 。在反应③中,若生成1mol D,则转移电子数目为 。
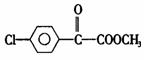
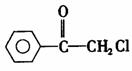 23.(12分)苯氯乙酮是一种具有荷花香味的有机物,其结构简式为
23.(12分)苯氯乙酮是一种具有荷花香味的有机物,其结构简式为
(1)苯氯乙酮可能发生的化学反应类型有 (选填字母)。
a.加成反应 b.取代反应 c.消去反应 d.水解反应 e.银镜反应
(2)同时符合①分子内有苯环但不含甲基:②氯原子与链烃基直接相连;③能发生银镜
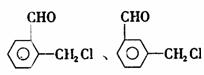 反应这三个要求的苯氯乙酮的同分异构体有
、
反应这三个要求的苯氯乙酮的同分异构体有
、
、 。
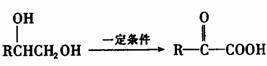
(3)已知:
苯氯乙酮的一种同分异构体M,可发生银镜反应,能用于合成杀菌剂
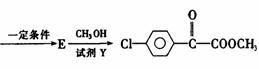 转化关系如下:
转化关系如下:
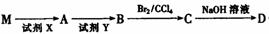
请回答:
①M的结构简式为 ,D中含氧官能团名称为 。
②A→B的化学反应方程式为 。
③C与NaOH醇溶液反应,所得产物的分子式为C8H5C1,则该产物的结构简式为 。
21.(11分)某短周期元素A,其最高价氧化物对应水化物甲与其气态氢化物乙反应可生成盐丙。已知乙的密度是同温同压下H2密度的8.5倍。
请回答:
(1)乙的电子式为 。
(2)甲具有不稳定性,其发生分解的化学反应方程式为 。
实验室保存甲的方法是 。
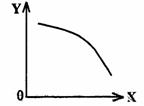 (3)在一定条件下,将乙放入固定容积的密闭容器中使其发生分解反应,已知△H>0,达到平衡状态后,改变其中一个条件X,Y随X的变化符合图中曲线的是
(3)在一定条件下,将乙放入固定容积的密闭容器中使其发生分解反应,已知△H>0,达到平衡状态后,改变其中一个条件X,Y随X的变化符合图中曲线的是
(选填字母)
a.当X表示温度时,Y表示乙的物质的量
b.当X表示压强时,Y表示乙的转化率
c.当X表示反应时间时,Y表示混合气体
|
d.当X表示乙的物质的量时,Y表示某一生成物的物质的量
(4)现有硫酸与甲的混合液20mL,其中硫酸的物质的量浓度为2mol·L-1,甲的物质的量浓度为1mol·L-1。向该混合液中加入0.96g铜粉,假设只生成一种无色气体,则所收集到的气体的体积在标准状况下为 。
(5)丙对水的电离起 作用(填“抑制”、“促进”或“不影响”),原因是(结合离子方程式简要说明)
。
20、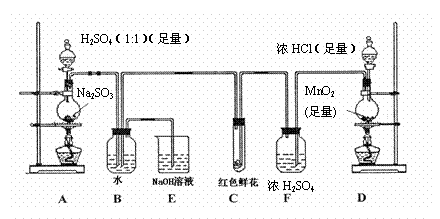 (10分)某学生为了测定部分变质的Na2SO3样品的纯度,设计了如下实验:
(10分)某学生为了测定部分变质的Na2SO3样品的纯度,设计了如下实验:
回答下列问题
(1)写出A装置中玻璃仪器的名称:酒精灯、 。
(2)实验开始后,写出B中反应的离子方程式 。
 (3)C中的现象是
,E装置的作用是
。
(3)C中的现象是
,E装置的作用是
。
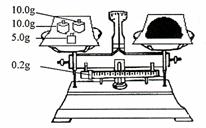
(4)按右图所示称取一定量的Na2SO3样品放入A装置的烧瓶中,滴入足量的H2SO4完全反应。然后将B中完全反应后的溶液与足量的BaCl2溶液反应,过滤、洗涤、干燥,得白色沉淀23.3g,则原样品中Na2SO3的纯度为 (精确到0.1%)。
(5)在过滤沉淀时若过滤液出现浑浊,则必须要重复操作,若该学生没有重复过滤,则测定的结果将 (填“偏高”、“偏低”或“无影响”)。
(6)要使测定结果准确,第一:装置气密性必须良好;第二:应先点燃 处酒精灯(填装置字母)。
19. (6分)三氟化氮(NF3)是一种新型电子材料,它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3,请根据要求回答下列问题:
(1)反应过程中,被氧化与被还原的元素的物质的量之比为 。
(2)写出该反应的化学方程式。 。
若反应中生成0.2 mol HNO3,转移的电子数目为 个。
(3)NF3是一种无色、无臭的气体,但一旦NF3在空气中泄漏,还是易于发现。你判断该气体泄漏时的现象是 。
(4)一旦NF3泄漏,可以用NaOH溶液喷淋的方法减少污染,其产物除NaNO2,NaF、H2O外。还肯定有 (填化学式)。
18.某浓度的硝酸与过量铁粉反应时生成了4.48LN2O气体(标准状况下),若改与铝反应(生成NO气体),则最后可溶解的铝的质量是( )
A.13.5g B.9g C.27g D.8.9g
第Ⅱ卷 非选择题(共56分)
17.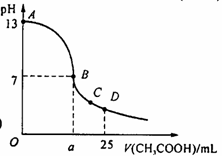 在25 mL 0.1 mol/L NaOH溶液中逐滴加入0.2 mol/L CH3COOH溶液,曲线如下图所示,有关粒子浓度关系比较正确的
( )
在25 mL 0.1 mol/L NaOH溶液中逐滴加入0.2 mol/L CH3COOH溶液,曲线如下图所示,有关粒子浓度关系比较正确的
( )
A.在A、B间任一点,溶液中一定都有
c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
B.在B点,a>12.5,且有
c(Na+)=c(CH3COO-)=c(OH-)=c(H+)
C.在C点:c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
D.在D点:c(CH3COO-)+c(CH3COOH)= c(Na+)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com