
题目列表(包括答案和解析)
16.常温时,将V1mL c1mol/L的氨水滴加到V2mL c2mol/L的盐酸中,下叙结论中正确的是( )
A.在V1=V2,c1=c2,则混合液中c(NH4+)>c(Cl-)
B.若混合液的pH=7,则混合液中c(NH4+) = c(Cl-)
C.若V1=V2,且混合液的pH<7,则一定有c1<c2
D.若混合液的pH=7,则c1V1=c2V2
15.高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:3Zn + 2K2FeO4+ 8H2O 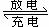 3Zn(OH)2 + 2Fe(OH)3
+ 4KOH,下列叙述不正确的是( )
3Zn(OH)2 + 2Fe(OH)3
+ 4KOH,下列叙述不正确的是( )
A.放电时负极反应为:Zn + 2OH- === Zn(OH)2 + 2e-
B.充电时阳极反应为:Fe(OH)3 + 5OH- === FeO42- + 4H2O + 3e-
C.放电时每转移3mol电子,正极有1molK2FeO4被氧化
D.放电时正极附近溶液的碱性增强
14.某同学为证明NaOH溶液能使酚酞试液变红是OH-的性质,他所设计的下列实验中没有意义是( )
A.取KOH、Ba(OH)2、Ca(OH)2溶液分别与酚酞试液作用,观察溶液颜色
B.取NaCl溶液与酚酞试液作用,观察溶液颜色
C.测定NaOH的溶解度,证明其易溶于水,并观察溶液的颜色
D.向滴有酚酞的NaOH溶液中加入盐酸,观察溶液的颜色
13. 在一定条件下,固定容积的密闭容器中反应:2NO2(g)
在一定条件下,固定容积的密闭容器中反应:2NO2(g)  2NO(g) + O2(g) ;△H>0,达到平衡。当改变其中一个条件X,Y随X的变化符合图中曲线的是( )
2NO(g) + O2(g) ;△H>0,达到平衡。当改变其中一个条件X,Y随X的变化符合图中曲线的是( )
A.当X表示温度时,Y表示NO的物质的量
B.当X表示压强时,Y表示NO2的转化率
C.当X表示反应时间时,Y表示混合气体的密度
D.当X表示向容器中充入气体Ne的物质的量时,Y表示NO的物质的量
12.下列离子方程式书写正确的是( )
A.向Ba(OH)2溶液中滴加NH4HSO4溶液至刚好沉淀完全:
Ba2+ + 2OH- + NH4+ + H+ + SO42- === BaSO4↓ + NH3·H2O + H2O
B.硫化钠溶液中滴入稀硝酸:S2- + 2H+ === H2S↑
C.用Pt电极电解MgCl2溶液:2Cl- + 2H2O  Cl2↑+ H2↑+ 2OH-
Cl2↑+ H2↑+ 2OH-
D. K2CO3溶于水:CO32- + H2O === HCO3- + OH-
11.下列各组离子一定能大量共存的是( )
A.在强碱性溶液中:Na+、K+、[Al(OH)4]-、CO32-
B.在含有大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN-
C.在c(H+)=10-13mol·l-1的溶液中:NH4+、Al3+、SO42-、NO3-
D.在pH=1的溶液中:K+、Fe2+、Cl-、NO3-
10.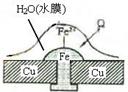 铜板上铁铆钉处的吸氧腐蚀原理如右图所示,下列有关说法中,不正确的是( )
铜板上铁铆钉处的吸氧腐蚀原理如右图所示,下列有关说法中,不正确的是( )
A.此过程中铜并不被腐蚀
B.此过程中还涉及到反应:4Fe(OH)2 +2H2O +O2 == 4Fe(OH)3
C.正极电极反应式为:2H+ + 2e- → H2↑
D.此过程中电子从Fe移向Cu
9.下列依据热化学方程式得出的结论正确的是( )
A.已知2H2(g) + O2(g) == 2H2O(g); △H=-483.6kJ·mol-1
则2g氢气燃烧生成液态水时放热为241.8 kJ·mol-1
B.已知C(石墨,s)=C(金刚石,s),△H>0 则金刚石比石墨稳定
C.已知2C(s) + 2O2(g) == 2CO2(g);△H1 2C(s) + O2(g) == 2CO(g);△H2,则△H1>△H2
D.已知NaOH(aq) + HCl(aq) == NaCl(aq) + H2O(l); △H=-57.6 kJ·mol-1
则含20.0gNaOH的稀溶液和稀盐酸完全中和,放出28.7kJ的热量
8.NA表示阿伏加德罗常数,下列叙述正确的是( )
A.如果5.6LN2含有n个氮分子,则阿伏加德罗常数一定约为4n
B.46gNO2和N2O4混合气体中含有原子数为3NA
C.含有1mol碳原子的金刚石,C-C共价键数为2NA
D.常温下1mol氯气与熟石灰完全反应转移电子数为2NA
7.在元素周期表短周期中的X和Y两种元素可组成化合物XY3,下列说法正确的是( )
A.XY2晶体一定是离子晶体
B.若Y的原子序数为n,X的原子序数一定是n±4
C.X和Y可属于同一周期,也可属于两个不同的周期
D.X和Y一定不属于同一主族
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com