
题目列表(包括答案和解析)
21.(12分)
(I)(1) mol·L-1·min-1。(2) mol·L-1。(3)
(II)(1) 极,b极的电极反应式为 。
(2) L。
20.(10分)
(1)M的电子式 。
(2)E是由 键构成的 分子。
(3) 。
(4) 。
19.(8分)
(1) ;
(2) ;
(3) ;
(4) ;
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
|
|
|
|
|
|
|
|
|
|
|
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
|
|
|
|
|
|
|
|
|
|
|
|
|
23.(12分)向浓度相同、体积均为50mL的A、B两份NaOH溶液中,分别通入一定量的CO2后,再稀释到100mL。
(1)在稀释后的A、B溶液中分别逐滴加入0.1mol·L-1的盐酸,产生的CO2体积(标准状况)与所加盐酸的体积关系如下图所示。

① A曲线表明,在NaOH溶液中通入一定量CO2后,溶液中溶质是
(填化学式), a值为 (标准状况)。
② B曲线表明,当0<V(HCl)≤60时,涉及反应的化学方程式为 。
(2)原NaOH溶液的物质的量浓度为_________mol·L-1,B溶液最多还能吸收CO2体积为 (标准状况)。
浦江县高三年级第一次模拟考试
化学答卷纸
22.(14分)由两种固体组成的混合物A可以发生如下框图所示的一系列变化。
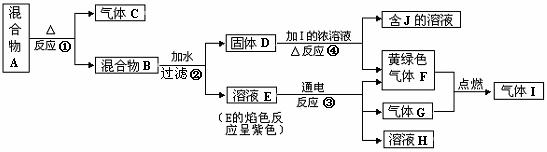
(1)按要求写方程式:
反应①的化学方程式 ;
反应③的离子方程式 ;
反应④的离子方程式 ;
(2)根据下图回答问题:
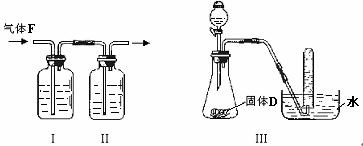
①在实验室中要获得干燥纯净的黄绿色气体F,可以将它通过如图I、II所示的装置,其中瓶I中盛放的是 ,目的是 ;
②用图III装置制取并证明气体C,分液漏斗内盛放的液体是 ,试管中收集满气体后,下一步实验操作是: 。
21.(12分)
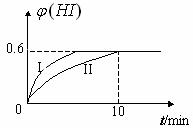 (I)将1molI2(g)
和2molH2(g)置于2L密闭容器中,在一定温度下发生反应:I2(g)+H2(g)
(I)将1molI2(g)
和2molH2(g)置于2L密闭容器中,在一定温度下发生反应:I2(g)+H2(g) 2HI(g);
2HI(g);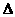 H<0。2min时,测得I2的物质的量为0.6mol。10min后达到平衡,HI的体积分数
H<0。2min时,测得I2的物质的量为0.6mol。10min后达到平衡,HI的体积分数 随时间变化如下图中曲线II所示。
随时间变化如下图中曲线II所示。
请回答下列问题:
(1)前2min内,用H2表示的平均反应速率为
mol·L-1·min-1。
(2)达到平衡时,I2(g)的物质的量浓度为 mol·L-1。
(3)若改变反应条件,在某条件下 的变化如 上图曲线I所示,则该条件可能是
的变化如 上图曲线I所示,则该条件可能是
(填入下列条件的序号)
①恒容条件下,升高温度 ②恒容条件下,降低温度
③恒温条件下,缩小反应容器的体积 ④恒温条件下,扩大容器的体积
⑤恒温恒容条件下,加入适当的催化剂
(II)有下图所示的装置:
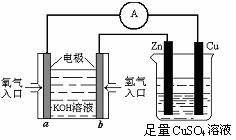
(1)该装置中铜片电极名称为 极,b极的电极反应式为 。
(2)当铜片的质量变化为12.8 g时,a极上消耗的O2在标准状况下的体积为 L。
20.(10分)已知三角锥形分子E和直线形分子G反应,生成两种直线形分子L和M(组成E、G、L、M分子的元素原子序数均小于10)如下图
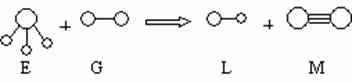
回答下列问题:
(1)M的电子式 。
(2)E是由 键构成的 分子(填“极性”或“非极性”)。
(3)组成G的元素在周期表中的位置 。
(4)上述反应中氧化剂与还原剂的物质的量之比为 。
19.(8分)根据水在化学反应中的作用,按要求完成下列氧化还原反应的化学方程式:
(1)水只作氧化剂:
(2)水只作还原剂:
(3)水既作氧化剂,又作还原剂:
(4)水既不作氧化剂,又不作还原剂:
18.2008年北京奥运会“祥云”奥运火炬所用环保型燃料丙烷(C3H8),悉尼奥运会所用火炬燃料为65%丁烷(C4H10)和35%丙烷,已知丙烷的燃烧热为:2221.5 kJ·mol-1;正丁烷的燃烧热为:2878kJ·mol-1;异丁烷的燃烧热为:2869kJ·mol-1。下列有关说法正确的是
A.丙烷燃烧的热化学方程式可表示为:
C3H8(g)+5O2(g)=3CO2(g)+4H2O(g);ΔH=-2221.5 kJ·mol-1
B.正丁烷燃烧的热化学方程式可表示为:
2C4H10(g)+18O2(g)=8CO2(g)+10H2O(l);ΔH=-2878 kJ·mol-1
C.正丁烷转化为异丁烷的过程是一个放热过程
D.正丁烷比异丁烷稳定
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com