
题目列表(包括答案和解析)
7.下列说法正确的是( )
A.氮族元素的单质的沸点随由上至下的顺序递增。
B.氮单质的熔沸点低于白磷,说明氮单质的稳定性弱,氮元素的非金属性强。
C.氮族元素的氢化物中,NH3最稳定,说明氮的非金属性最强。
D.白磷比红磷活泼的原因是它们各由不同种的磷原子构成。
6.x、Y是元素周期表ⅦA族中的两种元素。下列叙述中能说明X的非金属性比Y强的是( )
A.X原子的电子层数比Y原子的电子层数多
B.X的气态氢化物比Y的气态氢化物稳定
C.X的氢化物的沸点比Y的氢化物的沸点低
D.Y的单质能和NaX的溶液反应生成X的单质
5.最近医学界通过用具有放射性的14C试验,发现C80的一种羧酸衍生物在特定条件下可通过断裂DNA杀死病毒,从而抑制艾滋病(AIDS)的传播。有关14C试验的叙述中正确的是( )
A.与C80中普通碳原子的化学性质不同 B.与12C互为同位素
C.与12C中的中子数相同 D.与C80互为同素异形体
4.氯仿(CHCl3)可用作麻醉剂,常因保存不慎被空气氧化而产生剧毒物COCl2(光气)和氯化氢,为了防止事故发生,在使用前要检查氯仿是否变质,应选用的检查试剂是( )
A.NaOH溶液 B.AgNO3溶液
C.BaCl2溶液 D.KI溶液
3.已知常温常压下,N2(气)和H2(气)反应生成2molNH3(气)放出92.4kJ热量。在同温同压下向密闭容器中通入1molN2和3molH2,达到平衡时放出热量为Q1kJ;向另一体积相同的密闭容器中通人0.5molN2、1.5molH2和1molNH3,相同条件下达到平衡时放出热量为Q2kI。则下列关系式正确的是 ( )
A.2Q2=Q1=92.4 B.Q2<Q1<92.4
C.Ql<Q2<92.4 D.Ql=Q2<92.4
2.下列叙述正确的是( )
A.离子晶体中只存在离子键
B.原子晶体中只存在非极性共价键
C.冰是水分子间通过氢键作用有规则排列成的分子晶体
D.液态氯化钠和铜导线的导电原理是相同的
1.1995年我国科学家发现了91号元素中的一种新原子,其质量数为239,则该新原子的中子数是 ( )
A.330 B.239 C.148 D.91
31.(10分)A、B、C、D、E、F、M、N、X、Y是中学化学中常见的物质,其中A、B、C、D、E、F是化合物,M、N、X、Y是单质。已知反应关系如右图所示(部分产物已略去):

(1)向沸腾的蒸馏水中滴加A的饱和溶液,可以得到红褐色液体。A的化学式是
。
(2)将NaOH溶液注入新B溶液中,观察到的现象是 (选填序号)。
①生成白色沉淀
②生成血红色沉淀
③生成红褐色沉淀
④生成蓝色沉淀
⑤生成白色沉淀后,迅速变成灰绿色沉淀,最后变成红褐色沉淀
(3)C溶液电解的离子方程式是 。
(4)化合物F中含有组成单质N的元素,且该元素质量分数为70%。化合物F和单质Y反应的化学方程式是 。
(5)组成单质N的元素和碳的合金在潮湿的空气中容易腐蚀。发生腐蚀时,正极的电极反应式是 。
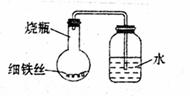 30.(10分)某学生在A、B、C、D四个小烧瓶中分别
30.(10分)某学生在A、B、C、D四个小烧瓶中分别
放入干燥的细铁丝、浸过食盐水的细铁丝、浸过清
水的细铁丝、食盐水及细铁丝(并使铁丝完全浸没
有食盐水中)。然后分别装配成如右图所示的装置,
每隔一段时间测量导管中水面上升的高度,结果如
下表所示(表中所列数据为导管中水面上升的高
度/cm),回答下列问题:
|
时间/小时 |
0 |
0.5 |
1.0 |
1.5 |
2.0 |
2.5 |
3.0 |
|
A瓶(盛干燥铁丝) |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
B瓶(盛浸了食盐水的铁丝) |
0 |
0.4 |
1.2 |
3.4 |
5.6 |
7.6 |
9.8 |
|
C瓶(盛浸了清水的铁丝) |
0 |
0 |
0 |
0.3 |
0.8 |
2.0 |
3.5 |
|
D瓶(盛完全浸没在食盐水中的铁丝) |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
(1)为什么有的导管中的水面会上升?
。
(2)上述实验中,铁生锈的速度由大到小的排列顺序为 (填小烧瓶的字母编号)。
(3)影响铁生锈的因素除氧气外还有
。
(4)日常生活中常见到铁制品生铁锈,试写出铁制品生成铁锈(Fe2O3·xH2O)的化学方程式 。
(5)通过上面的研究,你认为在日常生活中应该如何保护铁锅等铁制品?
。
29.(14分)某市拟投资建设一个工业酒精厂,目的是用工业酒精与汽油混合制成“乙醇汽油”,以节省石油资源,减少大气污染。已知制酒的方法有三种:
①在催化剂作用下乙烯与水反应
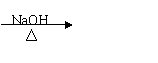
②CH3CH2Br+H2O CH3CH2OH+HBr
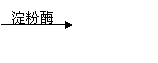
③(C6H10O5)n(淀粉)+nH2O nC6H12O6(葡萄糖)

C6H10O6(葡萄糖) 2C2H5OH+2CO2↑
(1)方法①反应的化学方程式是 。
方法②的化学反应类型是 。
(2)为缓解石油短缺带来的能源危机,你认为该市应选用哪一种方法生产工业酒精?请简述理由
。
(3)如果从绿色化学(“原子利用率”最大化)的角度看,制酒精最好的一组方法是
(填序号)
A.① B.③ C.①③ D.①②③
(4)乙醇分子中的氧原子被硫原子取代后的有机物叫乙硫酸,其性质与乙醇相似,但乙醇有酸性,它能与NaOH等强碱溶液反应生成无色溶液。汽油中因含乙硫醇(无色液体,微溶于水)使汽油有臭味且其燃烧产生的二氧化硫会污染环境,因此要把它除去。
①用化学方法除去汽油样品中的乙硫醇,请写出有关反应的化学方程式
。
②乙硫醇与乙醇在一定条件下可发生酯化反应,写出该反应的化学方程式
。
③在120℃、1.01×105Pa时,将乙醇、乙硫醇的混合蒸气1L和5LO2混合,充分燃烧后,恢复到原状况,气体密度减小为燃烧前混合气体的10/11,则乙醇和乙硫醇的体积之比为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com