
题目列表(包括答案和解析)
15.(12分)某研究性学习小组对过量炭粉与氧化铁反应中气体产物的成分进行了研究。
[提出假设]该反应中的气体产物可能是CO或者是CO2和CO的混合物。
[查阅资料]氮气不与碳、氧化铁发生反应。实验室可以用氯化铵饱和溶液和亚硝酸钠 ( NaNO2)饱和溶液混合加热反应制得氮气。
[设计方案 ] 如图所示,将一定量的氧化铁在隔绝空气的条件下与过量炭粉完全反应,测定参加反应的碳元素与氧元素的质量比。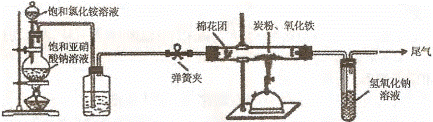
试回答下列问题:
(l)按上图连接装置,如何检查该装置的气密性
(2)广口瓶内盛放的试剂为 ,其作用为
(3)实验开始时,应先打开弹簧夹,一段时间后关闭;再点燃酒精喷灯,理由是
(4)称取3.20g氧化铁、2.00g炭粉混合均匀,放入质量为48.48g的硬质玻璃管中;待反应结束,再通一段时间的氮气。冷却至室温,称得硬质玻璃管和固体总质量为52.24g。经进一步测定得知参加反应的氧元素质量为0.96g 。从而确认该反应的气体产物是C02和CO 的混合物,理由是 。根据数据处理结果判断,反应产生的气体中n(C02):n(CO)= 。
(5)有同学根据实验得出的结论,认为应对实验装置进一步完善,你认为应作如何改进?
14. 已知N02和N204可以相互转化:
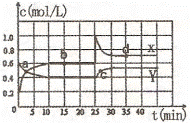
已知N02和N204可以相互转化: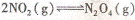 △H < 0。在恒温条件下将一定量N02和N204的混合气体通入一容积为2L的密闭容器中,反应物浓度随时间变化关系如右图。下列说法正确的是
A.图中的两条曲线,X是表示NO2浓度随时间的变化曲线 B.前10min内用v(NO2)表示的化学反应速率0.06mol/(L·min)
△H < 0。在恒温条件下将一定量N02和N204的混合气体通入一容积为2L的密闭容器中,反应物浓度随时间变化关系如右图。下列说法正确的是
A.图中的两条曲线,X是表示NO2浓度随时间的变化曲线 B.前10min内用v(NO2)表示的化学反应速率0.06mol/(L·min)
C.25min时导致平衡移动的原因是将密闭容器的体积缩小为lL
D.a、b、c、d四个点中,只有b、d 点的化学反应处于平衡状态
13. X、Y、Z和W代表原子序数依次增大的四种短周期元素,X原子核内没有中子,在周期表中,Z与Y、W均相邻;Y、Z和W三种元素的原子最外层电子数之和为17。则下列有关叙述正确的是:
A.Y、Z和W 三种元素可能位于同一周期
B.上述元素形成的氢化物中,W的氢化物相对分子质量最大,熔沸点最高
C. Y和W所形成的含氧酸均为强酸
D.X、Y、Z和W可以组成物质的量之比为5:1:4:1的离子化合物
12.镁及其化合物一般无毒(或低毒)、无污染,镁电池放电时电压高而平稳,因而越来越成为人们研制绿色原电池所关注。有一种镁原电池的反应为: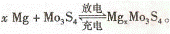 在镁原电池放电时,下列说法错误的是
在镁原电池放电时,下列说法错误的是
A. Mg2+向正极迁移 B.正极反应为: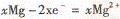
C. Mo3S4发生氧化反应 D.负极反应为: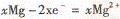
11.某化合物的结构式(键线式)及球棍模型如下: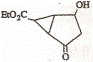
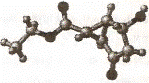 该有机分子的核磁共振波谱图如下(单位是 ppm )。
该有机分子的核磁共振波谱图如下(单位是 ppm )。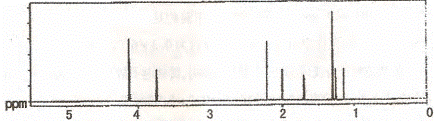
下列关于该有机物的叙述正确的是:
A.该有机物不同化学环境的氢原子有8种 B.该有机物属于芳香族化合物
C.键线式中的Et代表的基团为一CH3 D.该有机物在一定条件下能够发生消去反应
10.下列叙述中,不正确的是
A.在相同条件下,焓变小于O而熵变大于O的反应肯定能自发进行
B.升高温度会加快化学反应速率,其原因是增加了活化分子的百分数
C.青石棉的化学式为Na2Fe5Si8O22(OH)2,用氧化物的形式表示为:Na2O·3FeO·Fe203·8SiO2·H2O D.某离子被沉淀完全时,该离子在溶液中的浓度即为 0
9.下列反应的离子方程式正确的是
A. Fe203溶于过量的氢碘酸中:Fe203+6H+=2Fe3+ +3H2O
B.向 NaA102溶液中通入过量CO2: AlO2-+C02+2H2O=Al(OH)3↓+HCO3-
C.向漂白粉溶液中通入S02气体:Ca2++ 2 ClO–+S02 + H2O= CaSO3↓+2HC10
D.向Fe(NO3)2溶液中加入稀盐酸:3Fe2++4H++ NO3一=3Fe3++No↑+2H20
8. U(铀)是重要的核工业原料,常见化合价有+4和+6。硝酸铀酰[UO 2 (N03)
2]加热可发生如下分解: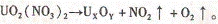 在600K时,收集满一试管气体产物,并将试管倒扣于水中,气体全部被吸收,水充满试管。则生成铀的氧化物中铀元素的化合价是
在600K时,收集满一试管气体产物,并将试管倒扣于水中,气体全部被吸收,水充满试管。则生成铀的氧化物中铀元素的化合价是
A. +4 B.+6 C.+4和+6 D. 0
7.常温下的下列情况中,可以大量共存于同一溶液中的离子组是
A.使甲基橙呈红色的溶液中:I一、Cl一、NO3一、Na+
B.使石蕊呈蓝色的溶液中:NH4+、Al3十、NO3一、HCO3-
C.由水电离出的c(H+)=1 xl0-12mol·L一1的溶液中:K十、Cl一、NO3一、Na+
D.含有大量Al3十的溶液中:Na+、Mg2+、K十、ClO–
0.2 x6.02xl023
C.标准状况下,2.24L乙烷中含有的非极性键数约为0.7x6.02xl023
D.含1mol硅原子的SiO2晶体中Si一O键的个数约为2x6.02xl023
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com