
题目列表(包括答案和解析)
16.下列各溶液中能大量共存的离子组是 ( )
A.使紫色石蕊溶液呈红色的溶液中: Ag+、Mg2+、Br-、K+
B.使PH试纸呈红色的溶液中:Fe2+、I-、NO-3、Cl-
C.C(H+)=1×10-14mol/L的溶液中:Na+、AlO-2、F-、SO2-3
D.水电离出的C(H+)与C(OH-)乘积为10-28的溶液中K+、Na+、HCO-3、Ca2+
15.某温度下向100g澄清的饱和石灰水中加入5.6g生石灰,充分反应后恢复到原来的温度下,下列叙述正确的是 ( )
A.沉淀物的质量为5.6g B.沉淀物的质量为7.4g
C.饱和石灰水的质量大于98.2g D.饱和石灰水的质量小于98.2g
13.若以ω1和ω2分别表示浓度为a mol·L-1和b mol·L-1硫酸的质量分数,且知2a = b,则下列推断正确的是 ( )
A.2ω1=ω2 B.2ω2=ω1 C.ω2<2ω1 D.ω1>ω2>2ω1
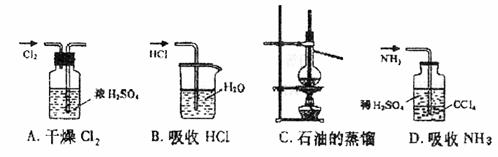 14.用下列实验装置完成对应的实验(部分仪器已省略),能达到实验目的的是 ( )
14.用下列实验装置完成对应的实验(部分仪器已省略),能达到实验目的的是 ( )
12.向存在大量Na+、Cl-的溶液中通入足量的NH3后,该溶液中还可能大量存在的离子组是
( )
A.K+、Br-、CO2-3 B.Al3+、H+、MnO-4
C.NH+4、Fe3+、SO2-4 D.Ag+、Cu2+、NO-3
11.运用周期律分析下列推断,其中错误的是 ( )
A.已知Ba是第六周期IIA族的元素,故Ba(OH)2的碱性比Mg(OH)2的碱性强
B.已知As是第四周期VA族的元素,故AsH3的稳定性比NH3的稳定性强
C.已知Cs的原子半径比Na的原子半径大,故Cs与水反应比Na与水反应强烈
D.已知Cl的核电荷数比Al的核电荷数大,故Cl的原子半径比Al的原子半径小
9.KMnO4、KclO3、KClO均为强氧化剂,在实验室里可代替MnO2,与浓盐酸反应制备Cl2,已知反应:KclO3+HCl→KCl+Cl2↑+H2O(未配平),若用K35ClO3与H37Cl作用,则下列说法中正确的是 ( )
A.该反应中转移电子数为6e- B.KCl只含35Cl
C.生成的KCl中既含35Cl又含37Cl D.生成氯气的式量约为73.3
|
A.p(He)>p(H2)>p(O2) B.p(O2)>p(He)>p(H2)
C.p(H2)>p(O2)>p(He) D.p(H2)>p(He)>p(O2)
8.在标准状况下,将体积为VL的A气体,溶于100.0mL水中,得到密度为ρg·cm-3的溶液,A气体的摩尔质量为Mg·mol-1,则此溶液的物质的量浓度为 ( )
A.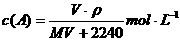 B.
B.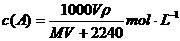
C. D.
D.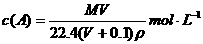
7.两份等体积、等浓度的NaOH溶液,分别与体积相等的MgCl2、AlCl3溶液混合,充分反应后,Mg2+、Al3+均恰好形成沉淀,则原MgCl2、AlCl3溶液中Cl-浓度之比为( )
A.1:1 B.1:2 C.2:3 D.3:2
6.已知:①向KMnO4晶体滴加浓盐酸,产生黄绿色气体;②向FeCl2溶液中通入少量实验
①中产生的气体,溶液变黄色;③取实验②生成的溶液滴在淀粉KJ试纸上,试纸变蓝色;下列判断正确的是 ( )
A.上述实验证明氧化性:KMnO4>Cl2>Fe3+>I2
B.上述实验中,共有两个氧化还原反应
C.实验①生成的气体不能使湿润的淀粉KJ试纸变蓝
D.实验②证明Fe2+既有氧化性又有还原性
5.下列说法中正确的是(NA表示阿佛加德罗常数) ( )
A.1 mol MgCl2中含有的离子数为NA B.0.1 molOH-含NA个电子
C.1.8g重水(D2O)中含NA个中子 D.标准状况下11.2L臭氧中含NA个氧原子
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com