
题目列表(包括答案和解析)
26.(包括2个小题,每空2分,共10分)
(1)氰(CN)2、硫氰(SCN)2的化学性质与卤素(X2)很相似,化学性质上称为拟卤素,如(SCN)2+H2O = HSCN+HSNO。已知阴离子的还原性强弱为Cl<Br<CN<SCN<I-。试写出:
a)(CN)2与KOH溶液反应的化学方程式
b) NaBr和KSCN的混合溶液中加入(CN)2反应的离子方程式为
(2)向amolFeBr2的溶液中通入bmolCl2,当b/a的取值不同时,将发生不同的反应,请按要求写出有关的离子方程式。
a)b/a≤1/2时
b) b/a≥3/2时
c) b/a=1时
25.(10分)用A+、B-、C3+、D、E、F、G和H分别表示含有10个电子的八种微粒(离子或分子),请回答:
(1)A元素是 、B元素是 、C元素是 (用元素符号表示)。
(2)D是由两种元素组成的双原子分子,其分子式是 。
(3)F是由两种元素组成的三原子分子,其分子式是 ,电子式是 。
(4)G分子中含有4个原子,其分子式是 。
(5)E是所有含10个电子微粒中反应活泼性最弱的分子,其分子式为 。
(6)写出一个电离方程,涉及到的微粒均为10个电子 。
24.有一铁的氧化物样品,用140mL 5mol·L-1盐酸可恰好使其完全溶解。所得溶液可吸收标准状况下0.56L氯气,使其中的Fe2+全部转化为Fe3+。该样品可能的化学式为( )
A.Fe4O5 B.Fe5O7 C.Fe2O3 D.Fe3O4
|
23.以下除杂方法(括号内为杂质)中,正确的是 ( )
①CH3COOH(H2O):加浓H2SO4,蒸馏 ②Cl2(HCl):饱和NaCl溶液 ③CO2(HCl):饱和Na2CO3溶液 ④KI(I2):酒精,分液⑤溴苯(溴):NaOH溶液,分液⑥FeCl3(FeCl2):铁屑
A.全部 B.①②③④⑥ C.①②⑤ D.只有②⑤
22.有X、Y两种元素,原子序数≤20,X的原子半径小于Y,且X、Y原子的最外层电子数相同(选项m、n均为正整数)。下列说法正确的是 ( )
A.若X(OH)n为强碱,则Y(OH)n也一定为强碱
B.若HnXOm为强酸,则X的氢化物溶于水一定显酸性
C.若X元素形成的单质是X2,则Y元素形成的单质一定是Y2
D.若Y的最高正价为+m,则X的最高正价一定为+m
21.Cl2在70℃的NaOH水溶液中,能同时发生两个自身氧化还原,反应完全后测得溶液中NaClO与NaClO3的物质的量之比为4:1,则溶液中NaCl与NaClO的物质的量之比为
( )
A.1:1 B.11:2 C.9:4 D.5:1
20.AB3是短周期两种元素形成的化合物,已知B原子比A原子多一个电子层,且AB3分子中所有原子满足8电子结构,则下列说法正确的是 ( )
A.AB3是三氧化硫 B.A是IIIA族元素
C.B原子比A原子多12个电子 D.B的氢化物和A的氢化物都极易溶于水
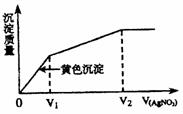
19.往含I-和Cl-的稀溶液中滴入AgNO3溶液,沉淀的
质量与加入AgNO3溶液体积的关系如图所示。则原
溶液中c(I-)/c(Cl-)的比值为 ( )
A.(V2-V1)/V1 B.V1/V2
C.V1/(V2-V1) D.V2/V1
18.下列有关短周期元素的叙述中,肯定正确的是 ( )
A.原子最外层电子只有1个或2个的元素是金属元素
B.16号元素原子的最外层电子数是4号元素原子的最外层电子数的四倍
 C.11号元素与17号元素能形成XY2型的化合物
C.11号元素与17号元素能形成XY2型的化合物
D.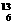 C表示的碳原子核内有6个质子,7个中子
C表示的碳原子核内有6个质子,7个中子
17.A元素的阴离子、B元素的阴离子和C元素的阳离子具有相同的电子层结构,已知A的原子序数大于B的原子序数,则三种离子半径大小的顺序是 ( )
A.rA>rB>rC B.rB>rA>rC C.rC>rA>rB D.rA>rC>rB
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com