
题目列表(包括答案和解析)
27.(16分)归纳整理是科学学习的重要方法之一。在学习了元素周期表之后,有关氧族元素的各种性质,可归纳整理出如下表所示的表格(部分)。
|
性质\元素 |
8O |
16S |
34Se |
52Te |
|
单质熔点(℃) |
-218.4 |
113 |
|
450 |
|
单质沸点(℃) |
-183 |
444.6 |
685 |
1390 |
|
主要化合价 |
-2 |
-2,+4,+6 |
-2,+4,+6 |
|
|
原子半径 |
逐渐增大 |
|||
|
单质与H2反应情况 |
点燃时易化合 |
加热化合 |
加热难化合 |
不能直接化合 |
请根据上表回答下列问题:
(1)硒的熔点范围可能是 _______________
(2)碲的化合价可能有 ________________
(3)硫、硒,碲的氢化物水溶液的酸性由强至弱的顺序是 (填化学式)。
(4)氢硒酸有较强的_________(填“氧化性”或“还原性”),因此放在空气中长期保存易变质,其可能发生的化学方程式为________________________________________________。
 (5)工业上Al2Te3可用来制备H2Te,完成下列化学方程
(5)工业上Al2Te3可用来制备H2Te,完成下列化学方程
式:____A12Te3 + ( )== A1(OH)3↓ + H2Te↑
(6)右图所示为氧族元素单质与H2反应过程中的能量变化示意 图,其中a、b、c、d分别表示氧族中某一元素的单质,△H为相同物质的量的单质与H2反应过程中的能量变化(反应的热效应)。则:b代表 ,d代表 (均写单质名称)。
26.(14分) (1)粉笔的粉末是教室里空气的主要污染源之一,粉笔的主要成分是生石膏
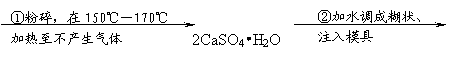 (CaSO4•2H2O),生产过程如下图:
(CaSO4•2H2O),生产过程如下图:
石膏砂 熟石膏 粉笔
回答:
①由熟石膏变成生石膏发生了 变化(选物理、化学)。
②生石膏与熟石膏的组成主要区别在于:
③步骤②中发生的化学方程式是:
④在熟石膏中加入甘油和纯碱可制成“无尘粉笔”,加入甘油是减少粉尘。加入纯碱可提高粉笔的硬度,加入纯碱发生反应的化学方程式是:
⑤有人设想,将无尘粉笔灰回收再制成熟石膏,你认为此法是否经济可行? 。
(2)2004年11月上旬,新疆硫磺沟火区的煤田大火在燃烧了100多年后被扑灭。扑灭煤田深处大火主要采用钻孔、注水、灌浆和表面覆盖泥土等方法。当水注入到高温燃烧的煤上时,发生的化学反应的方程式为: 。
煤是宝贵的化工燃料,在工业上,用碳在高温下还原二氧化硅可制得粗硅的化学反应方程式为: ________________________ 。
13.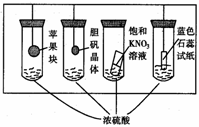 在下图所示的实验装置中,实验进行一段时间后,对观察到的现象叙述不正确的是( )
在下图所示的实验装置中,实验进行一段时间后,对观察到的现象叙述不正确的是( )
A.苹果块会干瘪
B.胆矾晶体表面有“白斑”
C.小试管内有KNO3晶体析出
D.蓝色石蕊试纸变红
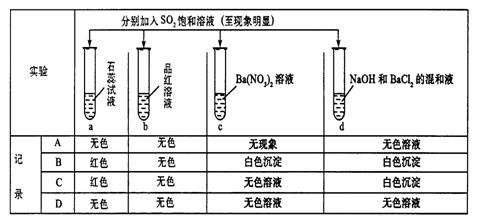
12.下列实验报告记录的实验现象正确的是( )
11.下列叙述正确的是( )
①标准状况下,1molSO2和1molSO3具有相同的体积;②SO2使溴水、高锰酸钾酸性溶液褪色是因为SO2有漂白性;③SO2有漂白性,湿润的氯气也有漂白性,若将SO2和Cl2以等物质的量混合后通入品红溶液中,一定褪色更快;④SO2溶于水,得到的溶液有氧化性,还有还原性;⑤SO2通入Ba(OH)2溶液中,有白色沉淀生成,加入稀硝酸最终沉淀将全部溶解⑥SO2通入BaCl2溶液中无沉淀生成。
A.①② B.③⑤ C.④⑥ D.①③⑥
10.对以下事实解释错误的是( )
A.在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性
B.浓H2SO4和铜片加热既表现出酸性,又表现出强氧化性
C.浓硫酸加热时可与木炭反应,还原产物是CO2、SO2
D.反应CuSO4+H2S==CuS↓+H2SO4能进行,说明CuS既不溶于水,也不溶于稀硫酸
9.下列叙述中,结论(事实)和对应的解释(事实)均不正确的是( )
A.金刚石的熔沸点高于晶体硅,因为C一C键能大于Si一Si键能
B.稀有气体的晶体属于原子晶体,因为其组成微粒是原子,不存在分子间作用力
C.二氧化硅晶体中不存在简单的SiO2分子,因为其晶体是含有硅氧四面体的空间网状结构
D.分子空间构型为正四面体结构的分子中化学键的键角可能是109028’,还可能为60°
8.X、Y、Z、W为四种短周期主族元素。其中X、Z同族,Y、Z同周期,W与X、Y既不同族也不同周期;X原子最外层电子数是核外电子层数的3倍;Y的最高正价与最低负价的代数和为6。下列说法正确的是( )
A.X与W可以形成W2X、W2X2两种化合物
B.Y元素最高价氧化物对应水化物的化学式为H2YO4
C.原子序数由小到大的顺序为W<X<Y<Z
D.Y、Z两元素的简单离子的半径Y>Z
7.根据元素周期表判断,下列叙述中正确的是( )
A.第三周期元素形成的离子半径从左到右逐渐增大
B.所含元素种类超过18种的周期是四、五、六、七周期
C.ⅦA族元素的氢化物中,稳定性最好的其沸点也最高
D.周期表中最活泼的非金属元素位于第15纵行,最高价氧化物对应水化物酸性最强
6.已知原子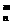 X,则下列论断正确的是(
)
X,则下列论断正确的是(
)
A.这种元素的近似原子量为m B.这种元素的原子量为m+n
C.该原子核内的中子数为n-m D.不能由此确定元素X的原子量
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com