
题目列表(包括答案和解析)
2.下列物质存放方法正确的是( )
A.药品柜的同一层不可存放浓硝酸和浓氨水B.少量的钠保存在无水乙醇中
C.少量白磷保存在二硫化碳中 D.硅酸钠溶液保存在玻璃塞的试剂瓶中
1.用铜锌合金制成的假金元宝欺骗行人的事件屡有发生。下列不易区别其真伪的方法是( )
A.测定密度 B.放入硝酸中 C.放入盐酸中 D.观察外观
26.常温、常压下把1mol由氨气和氧气组成的混合气体通入密封容器中,在催化剂存在下加热使之充分反应后,然后恢复到原来的温度和压强。
(1)写出容器内氨催化氧化及一氧化氮转化为硝酸的化学方程式。
(2)若原混合气体中氧气为x mol,最后在容器内产生的硝酸是y mol,试确定x在不同范围内y =f(x)的函数表达式。
|
x的取值范围 |
y = f (x)的函数表达式 |
|
|
|
|
|
|
|
|
|
|
|
|
 (3)以y为纵轴,x为横轴,在给出的图象纸(小方格)上画出函数图象,并简述
(3)以y为纵轴,x为横轴,在给出的图象纸(小方格)上画出函数图象,并简述
25.某化肥厂用NH3制备NH4NO3,已知由NH3制NO时,产率为96%,NO制HNO3时产率为92%,HNO3与NH3反应生产NH4NO3,则制HNO3所用的NH3质量占总耗NH3质量分数为多少?
24.L、M、R、P、Q分别代表五种含不同化合价的氮元素的物质,A、B分别代表两种含不同化合价的氯元素的物质(每种物质中,氮或氯元素的化合价只有一种),又知物质M中的氮元素的化合价要比物质Q中氮元素的化合价低。在一定条件下,它们会发生如下的转化(关系式未配平)。
①P+A→Q+B ②L+O2→M+H2O ③L+M→R+H2O ①B+H2O→A+O2
(1)若五种氮元素的物质中,有一种是硝酸,则硝酸是 ,理由是 。
(2)反应②必须在催化剂(铂、氧化铁等)作用下,加热到一定温度时方能发生.此反应在化工生产上有重要用途。据此推断在同温、同压下,若物质R的密度比二氧化碳的密度小,则R的化学式为 。
(3)某学生写出下面三个含氮元素的物质的相互转化的关系式
a.M + P→N2O3 + H2O b.N2O +H2O → P + M c.M+L → Q + H2O
其中一定不可能实现的是 ,理由是 。
23.A、B、C、D是四种常见非金属(短周期)单质,这些单质相对分子质量中,B最小,C次之,且室温下,A为固体,B、C、D为气体。
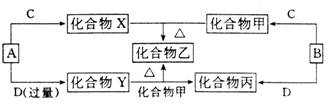
(1)写出下列物质的化学式:A ;B ;C ;D ;X 。
|
 (2)写出Y+甲 乙+丙 的化学方程式 。
(2)写出Y+甲 乙+丙 的化学方程式 。22.根据下列事实完成下列反应的化学方程式:
(1)AsH3是一种很强的还原剂,室温下,它能在空气中自燃,其氧化产物为As2O3,写出反应的化学方程式 。
(2)砷为氮族元素,其氧化物As2O3,俗名砒霜,有剧毒,可用马氏试砷法来检验,其原理是:将锌、盐酸和食物试样混合,其含有砒霜,则会生成砷化氢气体,这一反应的离子方程式是 。
(3)酸雨是由于大气中SO2和NOx(NO和NO2)的含量不断升高,并转变为H2SO4和HNO3(主要是H2SO4)随雨水降落而形成的。为防止污染,硫酸厂用氨水来吸收SO2离子方程式为 ;
硝酸厂可用烧碱溶液来吸收氮的氧化物,如NO2被烧碱吸收生成NaNO3和NaNO2,离子方程式为 ;
也可用氨的催化还原法把氮的氧化物变成氮气,还原1体积NOx需要 体积氨气。对酸雨地区的治理,目前一种比较有效的方法是用直升飞机喷撒白垩粉(主要成分为CaCO3),降解酸雨污染,其离子方程式是 。
21.硝酸与金属反应,其还原产物随金属活泼性和硝酸浓度不同,可分别为N2O、NO、NO2和NH4NO3等。已知6.5g某金属与过量稀硝酸反应(并无气体放出),反应后所得溶液加入过量热碱溶液 可放出一种气体,其体积为560mL(标准状况下)。溶于硝酸的金属是 ,推理过程是
。
20.某学生设计氨催化氧化实验,并将制得的NO进一步氧化为NO2,用水吸收NO2,并检验HNO3的生成。可供选择的固体药品有:NH4Cl、Ca(OH)2、KClO3、MnO2、CaO。可供选择的液体药品有:浓氨水,过氧化氢、浓盐酸、水。可供选择的仪器有:
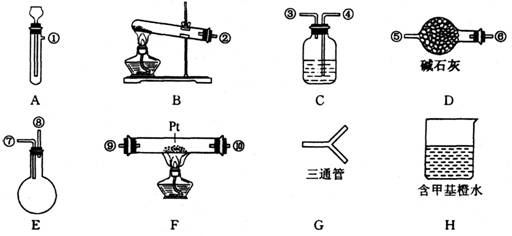
另有铁架台、铁夹、铁圈、乳胶管若干,可供选择。设计实验时,A和B两个制气装置均允许使用两次,其余装置只能使用于次。
(1)氨氧化制NO的化学反应为 ,该反应应在装置 中进行。
(2)为快速制取NH3和O2,制取NH3,的装置最好选择 ,其化学反应方程式为 ;制取O2的装置最好选择 ,其化学反应方程式为 。
(3)各仪器按气流方向连接的正确顺序为 。(按装置先后顺序排列)
(4)装置C的作用是 。
(5)若经充分反应,从H中排出的气体对大气不会造成污染,则装置E的使用方法是 。装置H中溶液显红色,其原因是 。(用化学反应方程式表示)
19.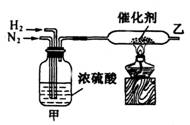 实验室合成氨的装置如下图所示。试回答:
实验室合成氨的装置如下图所示。试回答:
装置甲的作用是① ;② ; ③ ;
从乙处导出的气体是 ;检验产物的简单化学方法是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com