
题目列表(包括答案和解析)
14.08北京卷)(3分)常状况下,X、Y和Z是三种气态单质。X的组成元素是第三周期原子半径最小的元素(稀有气体元素除外);Y和Z均由元素R组成,反应Y+2I-+2H+ I2+Z+H2O常作为Y的临定反应。
(1)Y与Z的关系是(选填字母)_______。 a.同位素 b.同系物 c.同素异形体 d.同分异构体
(2)将Y和二氧化硫分别通入品红溶液,都能使品红褪色。简述用褪色的溶液区别二者的实验方法_________________________________________________________________
________________________________________________________________________。
(3)举出实例说明X的氧化性比硫单质的氧化性强(用化学方程式表示)。
________________________________________________________________________。
(4)气体(CN)2与X化学性质相似,也能与H2反应生成HCN(其水溶液是一种酸)。
①HCN分子中含有4个共价键,其结构式是___________________________________。 ②KCN溶液显碱性,原因是(用离子方程式表示)_____________________________。
 (5)加热条件下,足量的Z与某金属M的盐MCR3(C为碳原素)完全反应生成CR2和MmRn(m、n均为正整数)。若CR2质量为
(5)加热条件下,足量的Z与某金属M的盐MCR3(C为碳原素)完全反应生成CR2和MmRn(m、n均为正整数)。若CR2质量为 1g,MmRn质量为
1g,MmRn质量为 2g,M的相对原子质量为a,则MmRn中m:n=_____________(用含
2g,M的相对原子质量为a,则MmRn中m:n=_____________(用含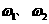 和a的代数式表示)。
和a的代数式表示)。
13.08全国2 ( 15 分)
Q、R、X、Y、Z 为前 20 号元素中的五种, Q 的低价氧化物与X 单质分子的电子总数相等, R 与 Q 同族, Y 和 Z 的离子与 Ar 原子的电子结构相同且Y 的原子序数小于Z。
( l ) Q 的最高价氧化物,其固态属于___________晶体,俗名叫________________;
( 2 ) R 的氢化物分子的空间构型是_______________,属于_____________分子(填“极性”或“非极性” ) ;它与 X 形成的化合物可作为一种重要的陶瓷材料,其化学式是___________________;
( 3 ) X 的常见氢化物的空间构型是__________________;它的另一氢化物X2H4是一种火箭燃料的成分,其电子式是_________________;
( 4 ) Q 分别与 Y、Z 形成的共价化合物的化学式是_________和__________; Q 与 Y 形成的分子的电子式是______________,属于__________分子(填“极性”或“非极性”)。
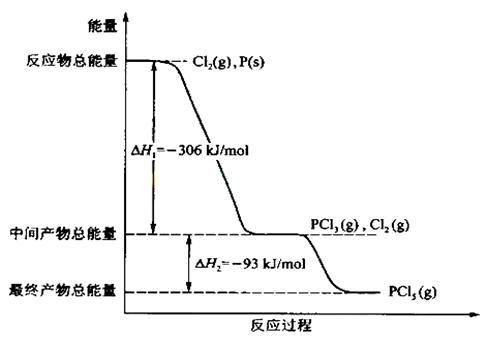
12.(15分) 08全国2 红磷 P (s)和 Cl2(g)发生反应生成 PCl3(g)和 PCl5(g)。反应过程和能量关系如图所示(图中的△H表示生成 l mol 产物的数据)。
根据上图回答下列问题:
( l ) P和CI2反应生成 PC13 的热化学方程式是_______________________________;
( 2 ) PC15分解成 PC13 和 Cl2的热化学方程式是______________________________;上述分解反应是一个可逆反应。温度 Tl 时,在密闭容器中加人 0.80 mol PC15 ,反应达平衡时 PC15 还剩 0.60 mol ,其分解率 al 等于_________________;若反应温度由 Tl 升高到T2,平衡时 PC15 的分解率为a2,a2_________ al (填“大于”、“小于”或“等于”) ;
( 3 )工业上制备 PC15 通常分两步进行,先将 P 和 C12 反应生成中间产物 PC13 ,然后降温,再和Cl2 反应生成 PCl5 。原因是________________________________________
______________________________________________________;
( 4 ) P 和 C12 分两步反应生成 1 mol PC15 的△H3==__________________,一步反应生成 1 molPC15 的△H4____________△H3(填“大于”、“小于”或“等于”)。
(5)PC15 与足量水充分反应,最终生成两种酸,其化学方程式是
________________________________________________________________________。
11、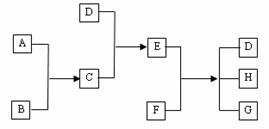 (05全国理综Ⅰ)已知A、B、C、D为气体,E、F为固体,G是氯化钙,它们之间的置换关系如下图所示:
(05全国理综Ⅰ)已知A、B、C、D为气体,E、F为固体,G是氯化钙,它们之间的置换关系如下图所示:
(1)D的化学式(分子式)是______________,
E的化学式(分子式)是____________;
(2)A和B反应生成C的化学方程式是_________________________________________;
(3)E和F反应生成D、H和G的化学方程式是__________________________________。
10、(05天津高考理综)磷在氧气中燃烧,可能生成两种固态氧化物。3.1 g的单质磷(P)在3.2 g氧气中燃烧,至反应物耗尽,并放出X kJ热量。
(1)通过计算确定反应物的组成(用化学式表示)是__________,其相应的质量(g)为_________;
(2)已知单质磷的燃烧热为Y kJ/mol,则1 mol P与O2反应生成固态P2O3的反应热△H=________;
(3)写出1 mol P与O2反应生成固态P2O3的热化学方程式_________________________ _。
9、(06年上海)已知:4NH3十5O2 → 4NO+6H2O
4NO十3O2十2H2O→4HNO3
设空气中氧气的体积分数为0.20,氮气体积分数为0.80,请完成下列填空及计算
(1)amolNO完全转化为HNO3需要氧气_______ mol
(2)为使NH3恰好完全氧化为一氧化氮,氨-空气混合物中氨的体积分数为________(保留2位小数)。
 (3)20.0moL的NH3用空气氧化,产生混合物的组成为:NO18.0mol、O212.0 mol、N2150.0 mol和一定量的硝酸,以及其它成分。(高温下NO和O2不反应)计算氨转化为NO和HNO3的转化率。
(3)20.0moL的NH3用空气氧化,产生混合物的组成为:NO18.0mol、O212.0 mol、N2150.0 mol和一定量的硝酸,以及其它成分。(高温下NO和O2不反应)计算氨转化为NO和HNO3的转化率。
(4) 20.0moL 的NH3和一定量空气充分反应后,再转化为HNO3
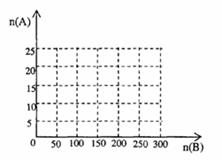
①在下图中画出HNO3的物质的量n(A)和空气的物质的量n(B)关系的理论曲线。
②写出当125≤n(B) ≤ 200时,n(A)和n(B)的关系式_________________________________。
8、(06江苏)下图是部分短周期元素的单质及其化合物的转化关系图(有关反应的条件及生成的H2O已略去),已知:
A、A、B、C、D是非金属单质,其中B、C、D在常温常压下是气体。
B、反应①②是化工生产中的重要反应。
C、化合物E是形成酸雨的污染物之一,化合物K是常用的氮肥。
D、化合物L具有漂白性,可由Cl2与NaOH溶液反应而制得。
E、化合物J由两种元素组成,其相对分子质量为32。
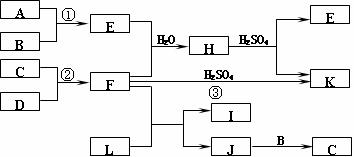
请按要求填空:
⑴反应③的化学方程式________ ______。
⑵C的结构式______________;H的化学式______________。
⑶L的溶液与化合物E反应的离子方程式_______ _______。
 ⑷化合物J的化学式______________。
⑷化合物J的化学式______________。
7、(06四川理综,15分)四川有丰富的天然气资源。以天然气为原料合成尿素的主要步骤如下图所示(图中某些转化步骤及生成物未列出):

请填写下列空白:
(1)已知0.5mol甲烷与0.5mol水蒸汽在t℃、pkPa时,完全反应生成一氧化碳和氢气(合成气),吸收了?kJ热量,该反应的热化学方程式是 。
(2)在合成氨的实际生产过程中,常采取的措施之一是:将生成的氨从混合气体中及时分离出来,并将分离出氨后的氮气和氢气循环利用,同时补充氮气和氢气。请运用化学反应速率和化学平衡的观点说明采取该措施的理由: 。
(3)当甲烷合成氨气的转化率为75%时,以5.60×107L甲烷为原料能够合成 L氨气。(假设体积均在标准状况下测定)
(4)已知尿素的结构简式为H2N--NH2,请写出两种含有碳氧双键的尿素的同分异构体的结构简式: ① ;② 。
6、 (06年江苏)稀薄燃烧是指汽油在较大空/燃比(空气与燃油气的体积比)条件下的燃烧。随着全球能源危机的加剧,稀薄燃烧技术的研究受到了人们的重视,但稀薄燃烧时,常用的汽车尾气净化装置不能有效地将NOx转化为N2。不同空/燃比时汽车尾气中主要污染物的含量变化如右图所示。⑴稀薄燃烧技术除能节约能源外,还具有的优点是
(06年江苏)稀薄燃烧是指汽油在较大空/燃比(空气与燃油气的体积比)条件下的燃烧。随着全球能源危机的加剧,稀薄燃烧技术的研究受到了人们的重视,但稀薄燃烧时,常用的汽车尾气净化装置不能有效地将NOx转化为N2。不同空/燃比时汽车尾气中主要污染物的含量变化如右图所示。⑴稀薄燃烧技术除能节约能源外,还具有的优点是
_________ _ ____(填一项)。排放到大气中的NOx会导致酸雨、________ _______等环境问题(填一项)。
⑵某校化学研究性学习小组的同学在技术人员的指导下,按下列流程探究不同催化剂对NH3还原NO反应的催化性能。
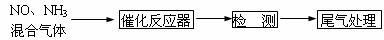
若控制其他实验条件均相同,在催化反应器中装载不同的催化剂,将经催化反应后的混合气体通过滴有酚酞的稀硫酸溶液(溶液的体积、浓度均相同)。为比较不同催化剂的催化性能,需要测量并记录的数据是_____ _________。
⑶若某一催化剂能同时催化NH3等还原性气体与的反应NOx的反应。将该催化剂分别用于催化还原含等物质的量NOx的两种气体:①纯NO气体,②汽车尾气。消耗的物质的量较多的可能是________(填字母),原因是__________________ ________。
A.① B.② C.都有可能
5、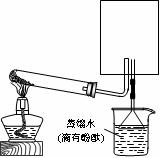 (2007年理综北京卷)(13分)短周期元素的单质X、Y、Z在通常状况下均为气态,并有下列转化关系(反应条件略去):
(2007年理综北京卷)(13分)短周期元素的单质X、Y、Z在通常状况下均为气态,并有下列转化关系(反应条件略去):

已知:a. 常见双原子单质分子中,X分子含共价键最多。
b. 甲分子含10个电子,乙分子含18个电子。
(1)X的电子式是 。
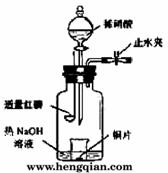
(2)实验室可用下图所示装置(缺少收集装置,夹持固定装置略去)制备并收集甲。
①在图中方框内绘出用烧瓶收集甲的仪器装置简图。
②试管中的试剂是(填写化学式)____________________。
③烧杯中溶液由无色变为红色,其原因是(用电离方程式表示)____________________________________________。
(3)磷在Z中燃烧可生成两种产物,其中一种产物丁分子中各原子最外层不全是8电子结构,丁的化学式是______ ___。
(4)n mol丁与n mol丙在一定条件下反应,生成4n mol乙和另一化合物,该化合物蒸气的密度是相同状况下氢气的174倍,其化学式是______________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com