
题目列表(包括答案和解析)
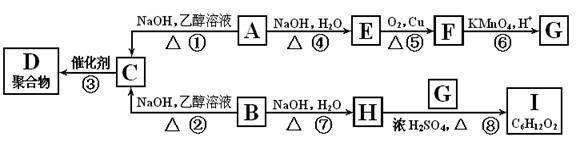
20.(16分)A和B是具有相同碳原子数的一氯代物,A-I转换关系如图所示:
 根据框图回答下列问题;
根据框图回答下列问题;
(1)B的结构简式是 ;
(2)反应③的化学方程式是 ;
(3)上述转换中属于取代反应的是 ;(填写反应序号)
(4)图中与E互为同分异构体的是 ;(填化合物代号)。图中化合物带有的含氧官能团有 种。
(5)C在硫酸催化下与水反应的化学方程式是 ;
(6)I的结构简式是 ;名称是 。
19.(14分)如下图所示的物质的相互转变中,反应①在工业上可用来生产化合物C,反应⑤在工业上可生产化合物J(Na2FeO4),反应①、②、④和⑤均是在水溶液中进行的反应。常温下,D、E、G均是气体,B是无色液体;F的水溶液可作为杀菌消毒剂;H是一种铁矿石的主要成分,它由两种元素组成,且其中铁元素的质量分数为70%。

请回答下列问题:
(1)写出F的化学式: ;
(2)写出G的电子式: ;
(3)反应①的化学方程式为 ;
人们将反应①所涉及的化学工业称为 ;
(4)反应⑤的离子方程式为 ;
高铁酸钠(Na2FeO4)被人们认为是一种“绿色环保高效”的净水剂,其原因为
①Na2FeO4具有强氧化性可杀菌消毒,② 。
18.已知下列反应的热化学方程式为:⑴C(s)+O2(g)=CO2(g) ;ΔH 1=-393.5kJ/mol
⑵CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ;ΔH 2=-870.3kJ/mol
⑶H2(g)+ O2(g)=H2O(l) ;ΔH 3=-285.8kJ/mol
O2(g)=H2O(l) ;ΔH 3=-285.8kJ/mol
则反应2C(s)+2H2(g)+O2(g)=CH3COOH(l) 的ΔH 为
A.488.3 kJ/mol B.-488.3 kJ/mol C.-244.15 kJ/mol D.244.15 kJ/mol
17.测定硫酸铜晶体中含结晶水的实验,造成结果偏高的原因是:
A.坩埚用水洗涤后没有把水烘干直接实验; B.坩埚内壁附有受热不分解的杂质;
C.把加热得到的白色粉末放在空气中冷却; D.晶体中含有少量的NaCl
16.常温下的下列情况中,一定能大量共存于同一溶液中的离子组是
A.使甲基橙呈红色的溶液中:I-、Cl-、NO3-、Na+
B.使石蕊呈蓝色的溶液中:NH4+、Al3+、NO3-、HCO3-
C.由水电离出的c(H+)=1×10 -12mol·L -1的溶液中:K+、Cl-、NO3-、Na+
D.含有大量Al3+的溶液中:K+、Mg2+、Na+、ClO-
15. 阿伏加德罗常数约为6.02×1023mol-1,下列说法一定正确的是
阿伏加德罗常数约为6.02×1023mol-1,下列说法一定正确的是
A.60g SiO2晶体中,含有2×6.02×1023个Si-O键
B.18g D2O(重水)完全电解,转移2×6.02×1023个电子
C.720g C60晶体含有6.02×1023个如图中晶胞单元
D.14g 两种烯烃CnH2n和CmH2m混合物,含有共用电子对数目为3×6.02×1023个
14.早在1807年化学家戴维用电解熔融氢氧化钠制得钠, 4NaOH(熔)  4Na +
O2↑+
2H2O;后来盖·吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为:3Fe+4NaOH
4Na +
O2↑+
2H2O;后来盖·吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为:3Fe+4NaOH Fe3O4+2H2↑十4Na↑。下列有关说法正确的是
Fe3O4+2H2↑十4Na↑。下列有关说法正确的是
A.电解熔融氢氧化钠制钠,阳极发生电极反应为:2OH--2e-=H2↑+O2↑
B.盖·吕萨克法制钠原理是利用铁的还原性比钠强
C.若戴维法与盖·吕萨克法制得等量的钠,则两反应中转移的电子总数也相同
D.目前常用电解熔融氯化钠法制钠(如图),电解槽中石墨极为阳极,铁为阴极
13.铀(U)常见化合价有+4价和+6价,硝酸铀酰[UO2(NO3)2]加热可发生如下反应:UO2(NO3)2 UxOy+NO2↑+O2↑(化学方程式未配平),在600
K时将气体产物集满试管,并倒扣水中,水充满试管。则上述分解反应生成的铀的氧化物化学式为
UxOy+NO2↑+O2↑(化学方程式未配平),在600
K时将气体产物集满试管,并倒扣水中,水充满试管。则上述分解反应生成的铀的氧化物化学式为
 A.UO2 B.UO·UO3 C.UO3 D.UO2·2UO3
A.UO2 B.UO·UO3 C.UO3 D.UO2·2UO3
12. 二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如右下图所示。常温下,S2Cl2遇水易水解,并产生能使品红褪色的气体。下列说法错误的是
二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如右下图所示。常温下,S2Cl2遇水易水解,并产生能使品红褪色的气体。下列说法错误的是
A.S2Cl2的结构式为Cl-S-S-Cl
B.S2Cl2为含有极性键和非极性键的非极性分子
C.S2Br2与S2Cl2结构相似,熔沸点:S2Br2>S2Cl2
D.S2Cl2与H2O反应的化学方程式可能为:
2S2Cl2+2H2O=SO2↑+3S↓+4HCl
11.碳酸氢钠受热容易分解为碳酸钠。现加热5.00 g的碳酸钠和碳酸氢钠的混合物,使碳酸氢钠完全分解,混合物质量减少了0.31g,则原混合物中碳酸钠的质量为
A.3.38 g B.4.58 g C.4.16 g D.4.41 g
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com