
题目列表(包括答案和解析)
6.为了除去FeCl2溶液中混有的少量FeCl3,最好的方法是向此溶液中
A.通入氯气 B.加入H2O2 C.加入Fe D.加入Cu
5.下列操作或仪器的选用正确的是
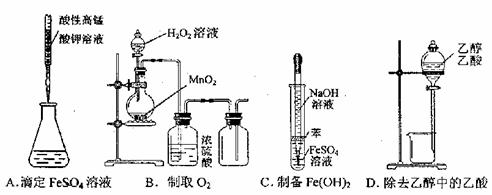
4、下列说法或表示方法正确的是
A、反应物的总能量低于生成物的总能量时,该反应一定不能发生
B、强酸跟强碱反应放出的热量就是中和热
C、由石墨比金刚石稳定可知: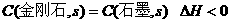
D、在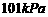 、
、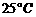 时,
时,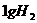 完全燃烧生成气态水,放出
完全燃烧生成气态水,放出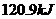 热量,则氢气的燃烧热为241.8
热量,则氢气的燃烧热为241.8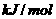
3、在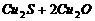
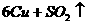 反应中,说法正确的是
反应中,说法正确的是
A、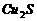 既是氧化剂又是还原剂 B、
既是氧化剂又是还原剂 B、 是氧化产物
是氧化产物
C、氧化剂只有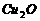 D、生成
D、生成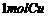 ,转移
,转移 电子
电子
2.据环保部门测定,我国一些大城市的酸雨pH=3.5。在酸雨季节铁制品极易腐蚀,则在其腐蚀中正极发生的反应是
A.2H+ + 2e- = H2↑ B.2H2O + O2 + 4e- = 4OH-
 C.Fe-2e- =
Fe2+ D.4OH--4e- =
2H2O + O2↑
C.Fe-2e- =
Fe2+ D.4OH--4e- =
2H2O + O2↑
1.下列分子的电子式书写正确的是
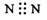
 A.氮气 B.四氯化碳
A.氮气 B.四氯化碳
C.二氧化碳 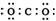 D.氨气
D.氨气 
21.(12分)现有A、B、C、D、E五种强电解质,它们在水中可电离产生下列离子(各种离子不重复)。
|
阳离子 |
H+、Na+、A13+、Ag+、Ba2+ |
|
阴离子 |
OH-、C1-、CO32-、NO3-、SO42- |
已知:①A、B两溶液呈碱性;C、D、E溶液呈酸性。
②A溶液与E溶液反应既有气体又有沉淀产生;A溶液与C溶液反应只有气体产生(沉淀包括微溶物,下同)。
③D溶液与另外四种溶液反应都能产生沉淀;C只能与D反应产生沉淀。
试回答下列问题:
(1)分别写出A、B、C、D、E的化学式:A 、B 、C 、
D 、E ;
(2)写出A、E反应的离子方程式: ;
(3)将C溶液逐滴加入等体积、等物质的量浓度的A溶液中,反应后溶液中各种离子浓度由大到小的顺序为: 。
(4)已知:NaOH(aq)+HNO3(aq)=NaNO3(aq)+H2O(1);△H =-Q kJ·mol-1。
写出B与C稀溶液反应的热化学方程式 。
(5)在100 mL 0.1 mol·L-1 E溶液中,逐滴加入40 mL 1.6 mol·L-1 NaOH溶液,最终得到沉淀物质的量为 mol。
20.(11分)A、B、C、D、E、F六种物质均是由短周期元素组成的中学常见的化学物质。它们之间的转化关系如下图。
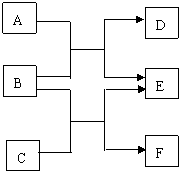
(1)若A、C、E均为氧化物,且E为有毒气体,B、D、F均为非金属单质,且D为气体,则:
① F的晶体类型为_________; 1molC中含有________mol共价键;
②B与C反应生成E和F的化学方程式为____________________________
(2)若A、C、E皆为氢化物,三者皆为极性分子,其中A的相对分子质量最小;D、E、F皆为氧化物,且D、F皆为有毒气体。则:
①A、C、E三种氢化物沸点从高到低的顺序为____________________(填化学式);
②A和F在水溶液中充入O2充分反应生成一种正盐,该反应的化学方程式为_____________________________________________
(3)若B是由短周期元素组成的离子化合物,A、C为氧化物,E为气体单质,D、F是均有三种元素组成的离子化合物,它们的水溶液均呈碱性,相同浓度时D溶液的PH大于F。
①写出B的电子式______________,
②B和C反应生成E和F的化学方程式____________________________,列举该反应的一种用途___________________________。
18.(9分)W、X、Y、Z是原子序数依次增大的同一短周期元素,W、X是金属元素,Y、Z是非金属元素。
(1)W、X各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为:
(2)W与Y可形成化合物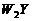 ,该化合物的电子式为
,该化合物的电子式为
(3)证明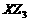 的水溶液pH 7(填>、<或=), 原因是(用离子方程式表示)
的水溶液pH 7(填>、<或=), 原因是(用离子方程式表示)
(4)比较Y、Z气态氢化物的稳定性: > (用分子式表示)
(5)W、X、Y、Z四种元素简单离子的离子半径由大到小的顺序是:
> > > (用离子符号表示)
(6)Z的最高价氧化物为无色液体, 该物质与一定量水混合得到一种稀酸溶液,并放出 Q kJ的热量。写出该反应的热化学方程式:
该物质与一定量水混合得到一种稀酸溶液,并放出 Q kJ的热量。写出该反应的热化学方程式:
19(8分)市场销售的某种食用精制盐包装袋上有如下说明(部分):
|
产品标准 |
 |
|
产品等级 |
一级 |
|
配料 |
食盐、碘酸钾、抗结剂 |
|
碘含量(以I计) |
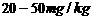 |
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式(将化学计量数填于空白处):
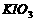 +
+
 +
+ 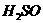 4
=
4
= 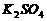 +
+
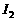 +
+ 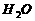
(2)上述反应生成的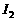 可用四氯化碳检验。向碘的四氯化碳溶液中加入
可用四氯化碳检验。向碘的四氯化碳溶液中加入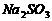 稀溶液,将
稀溶液,将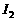 还原,以回收四氯化碳。
还原,以回收四氯化碳。
①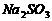 稀溶液与
稀溶液与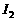 反应的离子方程式是
反应的离子方程式是
②某学生设计回收四氯化碳的操作步骤为:
a、将碘的四氯化碳溶液置于分液漏斗中; b、加入适量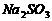 稀溶液;
稀溶液;
c、分离出下层液体。
以上设计中遗漏的操作及在上述操作中的位置是
(3)已知: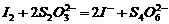
某学生测定食用精制盐的碘含量,其步骤为:
a、准确称取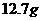 食盐,加适量蒸馏水使其完全溶解;
食盐,加适量蒸馏水使其完全溶解;
b、用稀硫酸酸化所得溶液,加入足量 溶液,使食用盐中
溶液,使食用盐中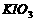 与
与 反应完全;
反应完全;
c、以淀粉溶液为指示剂,逐滴加入物质的量浓度为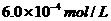 的
的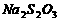 溶液
溶液 ,恰好反应完全。
,恰好反应完全。
①判断c中反应恰好完全依据的现象是
②根据以上实验和包装说明,所测精盐的碘含量是
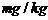
17.(8分)某校综合实践小组用废铁屑制FeCl3,用作印刷电路铜板腐蚀剂,并回收铜。活动过程如下:
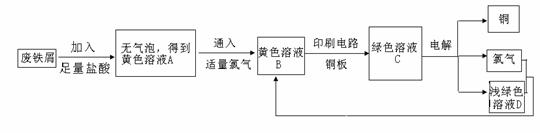
(1) 写出废铁屑与盐酸反应过程中可能发生反应的离子方程式:
(2) ;
;
。
(2)上述电解过程中的阴极材料是
(3)学生甲对黄色溶液A和绿色溶液C进行定性实验,完成下表:
|
编号 |
实验内容 |
实验操作 |
预期现象和结论 |
|
① |
检验黄色溶液A中是否含有Fe2+ |
|
|
|
② |
检验绿色溶液C中是否含有Fe3+ |
|
|
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com