
题目列表(包括答案和解析)
6、2007年3月温家宝总理在十届全国人大五次会议上提出“要大力抓好节能降耗、保护环境”,下列举措与这一主题不吻合的是( )
A.用“绿色化学”工艺,使原料完全转化为产物
B.推广燃煤脱硫技术,防治SO2污染
C.推广垃圾的分类存放、回收、处理
D.大量使用农药化肥提高粮食产量
( 2 ) 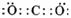
( 3 ) 3Fe3O4 + 8Al  4A12O3 + 9Fe
4A12O3 + 9Fe
( 4 ) 2Al + 2OH-+2H2O = 2A1O2-+3H2↑
( 5 ) 3Fe + 4H2O ( g ) Fe3O4 + 4H2 ↑
Fe3O4 + 4H2 ↑
( 6 )镁带剧烈燃烧,(产生耀眼的白光,)瓶壁或瓶底出现白色固体和黑色颗粒。
2Mg + CO2  2MgO + C
2MgO + C
5.( 14 分,每空 2 分)
4、 (12 分)
( 1 ) ( 6 分) ① b ② c ③ a
( 2 ) ① (1 分) HClO4
② ( 2分)离子键、(极性)共价键 NaClO
③ (2分) SiO2
+ 2C Si +2CO↑
Si +2CO↑
3、(4)2N2H4 (g) +2NO2 (g) = 3N2(g) +4H2O (g) △H = -1153.7 kJ·mol -1 (2分)
N2H4 (g) + 2F2 (g) = N2(g) +4HF (g) △H = -1135 kJ·mol -1 (2分)
2、(14分)(1)C、E、J; (多选不得分,选对几个给几分 ) (3分)
(2)冷却 防止吸水 (2分)
(3)4 , (1+1分)
(4)检验样品中的结晶水是否已经全部除去 (2分)
(5)(W2-W3)/(W2-W1)×100%; (3分)
(6) A、D; (2分)
1、(16分)(1)①碳 铁 (2+2分)
②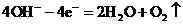 (2分)
(2分)
(2)① (2分)
(2分)
②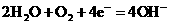 (2分)
(2分)
氧化反应 (1分)
③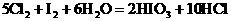 (2分)
(2分)
④13
5.( 14 分)A、B、C、D、E、F 是常见单质,其中 A 是用量最大,应用最广泛的金属;元素 D 是地壳中含量最多的金属元素: D 元素和 E 元素在周期表中相邻, G、 H、l、J、K、L 是常见化合物,其中 G 在常温下是无色液体, H 是黑色晶体,以上物质相互间的转化关系如下图所示:
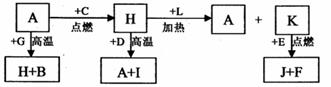
请回答下列问题:
( l )元素 A 在元素周期表中的位置为__________(周期)__________(族)。
( 2 )写出 K 的电子式_______________________________________。
( 3 )写出 H 和 D 反应的化学方程式_______________________________。
( 4 ) D 能与氢氧化钠溶液反应,请写出该反应的离子方程式:_________________。
( 5 )写出 A 与 G 反应的化学方程式____________________________________。
( 6 ) K 与 E 反应时产生的现象有_________________________________________,
该反应的化学方程式为_______________________________________________。
4.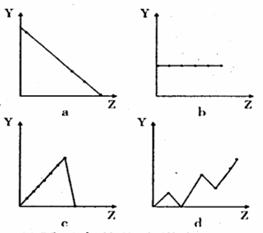 ( 12 分) ( l )右边曲线分别表示元素的某种性质与核电荷数的关系(Z 为核电荷数,Y为元素的有关性质)。把与下面元素有关的性质相符的曲线标号(a、b、c、d )填入相应的空格中:
( 12 分) ( l )右边曲线分别表示元素的某种性质与核电荷数的关系(Z 为核电荷数,Y为元素的有关性质)。把与下面元素有关的性质相符的曲线标号(a、b、c、d )填入相应的空格中:
① IIA 族元素的价电子数___________
② 第3 周期元素的最高化合价______
③ F-、Na+、Mg2+、Al3+的离子半径_
______________________________。
( 2 )元素 X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。己知 Y 元素原子最外层电子数与核外电子总数之比为 3 : 4 ; M 元素原子的最外层电子数与电子层数之比为 4 : 3 ; N-、Z+、X+半径逐渐减小;化合物 XN 常温下为气体。据此回答:
① N 的最高价氧化物的水化物的化学式为_______________。
② 化合物 A、B 均为由上述五种元素中的任意三种组成的强电解质,且两种物质水溶液酸碱性相同,组成元素的原子数目比均为 1 : 1 : 1 , A 溶液中水的电离程度比 B 溶液中水的电离程度小,则化合物 A 中的化学键类型为__________________________,B 的化学式为_________________________________。
③ 工业上制取单质 M 的化学方程式为______________________________________。
0.5H2 (g) + 0.5F2 (g) = HF (g) △H = -269 kJ·mol -1
H2 (g) +0.5O2 (g) = H2 O (g) △H = -242 kJ·mol -1
①肼和NO2反应的热化学方程式_____ _。
②有人认为若用氟气代替二氧化氮作氧化剂,则反应释放的能量更大,肼和氟气反应的热化学方程式: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com