
题目列表(包括答案和解析)
6.下列离子方程式正确的是 ( )
A.二氧化硅与氢氧化钠溶液反应:SiO2+2OH- SiO +H2O
+H2O
B.碳酸钙与盐酸反应:CO +2H+
+2H+ CO2↑+H2O
C.硫酸与氢氧化钡溶液反应:Ba2++OH-+H++SO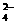
BaSO4↓+H2O
D.铝与氢氧化钠溶液反应:Al +2OH- AlO +H2↑
+H2↑
5.氧化还原反应广泛应用于金属的冶炼。下列说法不正确的是 ( )
A.电解熔融氯化钠制取金属钠的反应中,钠离子被还原,氯离子被氧化
B.湿法炼铜与火法炼铜的反应中,铜元素都发生还原反应
C.用磁铁矿炼铁的反应中,1mol Fe3O4被CO还原成Fe,转移9mole-
D.铝热法还原铁的反应中,放出的热量能使铁熔化
4.有NaCl、FeCl2、FeCl3、MgCl2、AlCl3五种溶液,用一种试剂就可把它们鉴别开来,这种试剂是 ( )
A.盐酸 B.烧碱溶液 C.氨水 D.KSCN溶液
3.微观粒子是化学研究的主要对象。若阿伏加德罗常数为6.02×1023mol-1,下列对粒子数判断正确的是 ( )
A.常温常压下,2.24L CO2气体中含有的分子数为0.1×6.02×1023

 B.2.8g [CH2-CH2 ]n 中含有的碳原子数为0.2×6.02×1023
B.2.8g [CH2-CH2 ]n 中含有的碳原子数为0.2×6.02×1023
C.0.3L 1mol/L Na2SO4 溶液中含有的Na+数为0.3×6.02×1023
D.1.7gNH3中含有的质子数为0.4×6.02×1023
2.生产、生活离不开各种化学物质,下列说法不正确的是 ( )
A.不需要通过化学反应就能从海水中获得食盐和淡水
B.潜水艇在紧急情况下可用过氧化钠供氧
C.氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂
D.工业上常用硅制造光导纤维
1.绿色化学的核心就是利用化学原理从源头上减少和消除工业生产对环境的污染。下列做法不符合绿色化学理念的是 ( )
A.研制水溶剂涂料替代有机溶剂涂料
|
|

|
 D.用反应:2CH2=CH2+O2 2CH2-CH2制备环氧乙烷
D.用反应:2CH2=CH2+O2 2CH2-CH2制备环氧乙烷
22. (8分)某结晶水合物含有两种阳离子和一种阴离子。称取两份质量均为1.96g的该结晶水合物,分别制成溶液。一份加入足量Ba(OH)2溶液,生成白色沉淀,随即沉淀变为灰绿色,最后带有红褐色;加热该混合物,逸出能使湿润的红色石蕊试纸变蓝的气体;用稀盐酸处理沉淀物,经洗涤和干燥,得到白色固体2.33 g。另一份加入含0.001 mol KMnO4的酸性溶液,MnO4-恰好完全被还原为Mn2+。
请回答以下问题:
(1)该结晶水合物中含有的两种阳离子是 和 ,阴离子是 。
(2)试通过计算确定该结晶水合物的化学式。
湖南省绥宁县第二中学2009届高三化学第一次月考
21.(10分)某课外活动小组的同学共同设计了如图所示的实验装置(夹持仪器略),并用其进行下述实验:

(1)实验1:制取并收集H2和Cl2。
①若制取并收集H2,则旋塞K1应该 (填“打开”或“关闭”),旋塞K2应该 (填“打开”或“关闭”),H2 收集在仪器 (填表示仪器的英文字母) 中。
② 若将试管C中加满某种液体,可用于收集Cl2,这种液体最好选用 (填编号)。
a.饱和NaHCO3溶液 b.饱和NaCl溶液 c.NaOH溶液
(2)实验2:验证酸性HCl>H2CO3>C6H5OH。
①若可供选择的试剂有大理石、盐酸、苯酚钠溶液等,在干燥管D中加入混有足量NaHCO3的石棉绒,则苯酚钠溶液应该装入 (填表示仪器的英文字母)中,该仪器内发生反应的离子方程式是 .
 ②在干燥管D中加入混有足量NaHCO3的石棉绒的作用是 。
②在干燥管D中加入混有足量NaHCO3的石棉绒的作用是 。
(3)实验3:用干、湿两个有色布条验证干燥Cl2不具有漂白性而潮湿的
Cl2具有漂白性。
①若用高锰酸钾与浓盐酸反应制取Cl2,实验前先将装置C改用如图
37所示装置,并应在D中加入 (填代号)
a.浓硫酸 b.氯化钙 c.碱石灰 d.碳酸氢钠
②润湿的有色布条应放在 (填表示仪器的英文字母)中,干燥的有色布条应放在 (填表示仪器的英文字母)中。
20.(10分)(1)下列四种实验装置(根据需要可在其中加入液体或固体)

①用于干燥二氧化硫气体的装置有_____________(填字母)。
②装置B除可用于制取CO2、H2,还可制取____________。(写出1种物质的化学式)。
③既能用于收集氯气又能用于收集一氧化氮气体的装置有_______。(填字母)
④当用A装置测量CO2气体体积时,从___________端进气,瓶中所盛的液体为________________(填名称)当用A装置收集氢气时从__________端进气.
(2)下列实验操作或实验事实的叙述不正确的是_____________(填序号)。
A.过滤、蒸发操作过程中都需要用玻璃棒不断搅拌液体。
B.在试管中放入几片碎滤纸片,加入几滴90%的浓硫酸,捣成糊状,微热并冷却后,先滴入几滴CuSO4溶液,再加入过量的NaOH溶液中和至出现Cu(OH)2沉淀。加热至沸腾,可观察到红色沉淀生成。
C.制备硫酸亚铁晶体时,向废铁屑中加入过量稀硫酸,充分反应后,过滤,然后加热蒸干滤液即可得硫酸亚铁晶体
D.测定硫酸铜晶体结晶水含量的实验中,称量操作至少要进行4次。
E.向滴有酚酞的水中加入足量的过氧化钠后可观察到溶液不呈红色.
19、(10分)储氢纳米碳管的研究成功体现了科技的进步,但用电孤法合成的碳纳米管常伴有大量的杂质-碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯。其反应式为:
__C+__K2Cr2O7 +__H2SO4 →__CO2+__K2SO4+__Cr2(SO4)3 +__ H2O
(1) 配平上述反应的化学方程式并标出电子转移方向和数目
(2) 上述反应中氧化剂是______ __(填化学式) 被氧化的元素是____ ____(填元素符号)。
(3) H2SO4 在上述反应中表现出来的性质是____________(填选项编号)
(A) 氧化性 (B) 氧化性和酸性 (C)酸性 (D)还原性和酸性
(4) 若反应中电子转移了0.8mol,则产生的气体在标准状况下的体积为____ ____L。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com