
题目列表(包括答案和解析)
17. (1)一定温度下,把相对分子质量为M的可溶性盐Wg(不含结晶水)溶解在VmL水中,恰好形成饱和溶液(密度为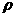 g·cm-3),则溶质质量分数为
,物质的量浓度为
,该温度下此盐的溶解度为
。
g·cm-3),则溶质质量分数为
,物质的量浓度为
,该温度下此盐的溶解度为
。
(2)粗盐经提纯后得到NaCl溶液,再经蒸发、结晶、烘干得精盐。
①蒸发操作中使用到的仪器除铁架台(带铁圈)外,还需要仪器的名称为 。
②该同学将所得精盐配成溶液,用于另一实验。实验中需要用60 mL,1 mol/L-1的NaCl溶液,配制过程中用托盘天平称取的精盐质量为 ,配制该溶液所需的主要玻璃仪器是 。
16. 为确定某含一种溶质形成的溶液的离子组成,进行如下实验:
①测定溶液的pH,溶液显强碱性。
②取少量溶液加入稀盐酸至溶液呈酸性,产生无刺激性、能使澄清石灰水变浑浊的气体。
③在上述溶液中再滴加Ba(NO3)2溶液,产生白色沉淀。
④取上层清液继续滴加Ba(NO3)2溶液至无沉淀时,再滴加Ag NO3溶液,产生白色沉淀。
根据实验以下推测正确的是
A.一定有SO32-离子 B.一定有CO32-SO42-离子
C.不能确定C1-离子是否存在 D.不能确定HCO3-离子是否存在
15.下列离子方程式书写正确的是
A.过量的SO2通人NaOH溶液中:SO2+2OH-=SO32-+H2O
B.向硫酸氢钠溶液中滴入氢氧化钡溶液至pH=7
Ba2++2OH-+2H++SO42- =BaSO4↓+2H2O
C.NaNO2溶液中加入酸性KMnO4溶液:
2MnO4-+5NO2-+6H+=2Mn2++5NO3-+3H2O
D.等物质的量浓度、等体积的NH4HCO3溶液与NaOH溶液相混合:
NH4+ + HCO3- + 2OH- = NH3·H2O + CO32- +H2O
14.已知下列反应:①NH3+H+ NH4+ ②Ag++2NH3
NH4+ ②Ag++2NH3 Ag(NH3)2+ ③Ag++Cl-
Ag(NH3)2+ ③Ag++Cl- AgCl
AgCl
前者都比后者更容易发生。下列事实或现象预期正确的是
A.氯化银可溶于氨水 B.银氨溶液中加入少量氯化钠有白色沉淀
C.银氨溶液中加入盐酸有白色沉淀 D.银氨溶液可在酸性条件下稳定存在
13.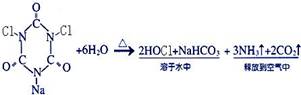 漂白粉和泡腾片用于环境消毒和饮用水消毒
漂白粉和泡腾片用于环境消毒和饮用水消毒
已知泡腾片消毒原理如右图:
下列有关说法不正确的是
A.漂白粉需密闭储存 B.工业上制取漂白粉可将氯气通入石灰乳中制得
C.泡腾片主要成分属于有机物 D.泡腾片分子中氮显+3价
12.水中卤代烷烃有碍健康,将铁加入水体中,大约15天后水中检不出卤代烷烃,涉及的反应中不会产生的物质是
A、卤素单质 B、 Fe2+离子 C、卤素阴离子 D、 烷烃
11.同位素示踪法可用于反应机理的研究,下列反应或转化中同位素示踪表示正确的是
A.2Na218O2 + 2H2O = 4Nal8OH + O2↑
B.2KMnO4 + 5H218O2 + 3H2SO4 = K2SO4 + 2MnSO4 + 518O2↑+ 8H2O
C.NH4Cl + 2H2O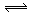 NH3·2H2O + HCl
NH3·2H2O + HCl
D.K37ClO3 + 6HCl = K37Cl + 3Cl2↑+ 3H2O
10.海底黑烟囱可在海底堆积硫化物的颗粒,形成多种金属矿产。若从海底黑烟囱附近的矿产物中分离出富铜矿CuFeS2,可用于冶炼铜,熔炼过程主要反应为:
2CuFeS2─→Cu2S+2FeS+S…………………………… ①
2Cu2S+3O2=2Cu2O+2SO2………………………………… ②
Cu2O+FeS─→Cu2S+FeO……………………………… ③
2FeS+3O2+SiO2─→2FeO·SiO2+2SO2………………… ④
2FeO+SiO2─→2FeO·SiO2……………………………… ⑤
Cu2S+2Cu2O─→6Cu +SO2 ……………………………… ⑥
下列有关说法不正确的是
A.上述反应均属于氧化还原反应 B.该厂可同时建硫酸厂和炼铁厂
C.该厂的原料除富铜矿外,还需空气和硅石 D.反应④转移12e-
9.用6.02×1023表示阿伏加德罗常数的值,下列说法中正确的是( )
A.常温常压下,1mol碳烯(:CH2)所含电子总数为8NA
B.6.8 g熔融的KHSO4中含有6.02×1022个阳离子
C.1 mol CO2与含2 mol NaOH的溶液反应后,溶液中CO32-数为NA
D.用含有0.1molFeCl3的饱和溶液制得的氢氧化铁胶体中,胶粒数等于0.1 NA
8.将25%的硫酸溶液与5%的硫酸溶液等体积混合,所得硫酸溶液的质量分数是
A.等于15% B.大于15% C.小于15% D.无法估算
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com