
题目列表(包括答案和解析)
10.NO2; Br2; HCl; NH3; HCl、CO2; CH4
9. ⑴CaCN2 ⑵
CaCN2 + 3H2O = CaCO3 + 2NH3↑ ⑶ ⑥ ⑦
⑴CaCN2 ⑵
CaCN2 + 3H2O = CaCO3 + 2NH3↑ ⑶ ⑥ ⑦
2NaCl + 2H2O 2NaOH + Cl2↑+ H2↑
2Cl2 + 2Ca(OH)2=CaCl2 + Ca(ClO)2 + 2H2O
1.C 2.B 3.B 4.B 5.D 6.A 7.A 8.D
12.某化工厂生产硫酸,使用一种含SiO2杂质的黄铁矿。经过测试该矿石,发现2.00 g矿石样品在氧气中充分灼烧,残余固体是1.60 g。已知SiO2在高温下不与氧气发生反应;黄铁矿与氧气反应的化学方程式为4FeS2+11O2=2Fe2O3+8SO2 ;生产过程中,FeS2燃烧生成SO2时的转化率是92%,SO2催化氧化生成SO3时的转化率为86%,在吸收塔中SO3与水反应生成H2SO4时的转化率为94%。
(1)该矿石中FeS2的纯度是多少?
(2)由FeS2生成H2SO4的总转化率是多少?
(3)用1t这样的矿石可生产98%的浓硫酸多少吨?
第十章 氮族元素
0.8molHNO3的稀硝酸反应,反应后硝酸和铁均无剩余,且硝酸的还原产物只有NO。据此
回答下列问题:⑴ 甲取样品①,反应后的溶液中铁只以Fe3+离子的形式存在,则样品的
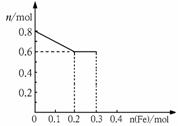 质量为 g。
质量为 g。
⑵ 乙取样品②,反应后的溶液中既含有Fe3+,又含有
Fe2+离子,则样品②的质量(设为ag)范围是 。
|
10.已知固体混合物A由NaHCO3、KHCO3、MgCO3、CaCO3四种物质中的两种混合而成,通过计算和推理回答下列问题:
(1)取A与足量的盐酸反应
①若n(A)为定值,生成气体的量即为定值,则A的组成最多可能有 种。
②若m(A)为定值,生成气体的量即为定值,则A的可能组成是 ; ; 。(可以不填满,也可以补充)
(2)若先将A加热,剩余固体再与足量的盐酸反应,且先后两次产生的气体分别通过足量的澄清的石灰水生成的沉淀均为10.0g,则n(A)= mol.
|
9.某赤铁矿石经处理后检测只含有杂质氧化铜和氧化亚铁,化学研究小组的同学取试样ag,在加热条件下用足量的一氧化碳将其充分还原事,得到金属混合物10克,生成的二氧化碳用过量的石灰水吸收,得到20克沉淀。
(1)a=________
(2)另取ag 上述矿石试样溶于200 mL2.5mol·L-1的硫酸溶液,充分反应后,计算所得溶液中c(H+)(忽略溶液体积的变化。)
(3)将(2)所得溶液以惰性电极电解,当电路中通过0.2mol电子时,停止电解。试通过计算和推理判断电解过程中阴极上是否一定有金属析出。
(4)通过上述方法制得的金属混合物放置一段时间后,发现表面生锈(铜未生锈),取bg加入1L1mol·L-1的硫酸溶液中(整个反应过程中无气体放出),完全溶解,最终溶液中c(Fe3+)=0.1mol·L-1,c(Cu2+)=0.05mol·L-1,则b的范围是________(假设反应后溶液的体积为1L)
8.某学生用NaHCO3和KHCO3组成的某混合物进行实验,测得如下数据(盐酸的物质的量浓度相等)。则下列分析推理中不正确的是( )
|
|
50mL盐酸 |
50mL盐酸 |
50mL盐酸 |
|
m(混合物) |
9.2g |
15.7g |
27.6g |
|
V(CO2)(标况) |
2.24L |
3.36L |
3.36L |
A.盐酸的物质的量浓度为3.0mol·L-1 B.混合物中NaHCO3的质量分数为45.7%
C.加入混合物9.2 g时盐酸过量 D.15.7 g混合物恰好与盐酸完全反应
7.向200ml FeBr2溶液中通入672 ml(标准状况)的氯气,充分反应后,所得溶液中氯离子的浓度等于原溶液中溴离子的浓度,则原溶液中FeBr2的物质的量浓度为( )
A.0.1mol·L-1 B.0.2 mol·L-1 C.0.15mol·L-1 D.0.3 mol·L-1
6.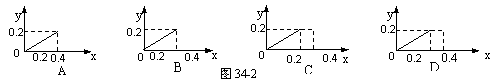 将22.4g铁粉逐渐加入到含HNO30.8mol的稀硝酸中,反应生成的气体的物质的量(y)随消耗铁粉的物质的量(x)变化关系如图34-2,正确的选项是( )
将22.4g铁粉逐渐加入到含HNO30.8mol的稀硝酸中,反应生成的气体的物质的量(y)随消耗铁粉的物质的量(x)变化关系如图34-2,正确的选项是( )
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com