
题目列表(包括答案和解析)
10.(16分)某种含有少量氧化纳的过氧化钠试样(已知试样质量为1.560g、锥形瓶和水的质量为190.720g),利用下图装置测定混合物中Na2O2的质量分数,每隔相同时间读得电子天平的数据如表:
(1)写出Na2O2和H2O反应的化学方程式 。(2)计算过氧化钠质量分数时,必需的数据是 。不必做第6次读数的原因是 。
(3)测定上述样品(1.560g)中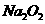 质量分数的另一种方案,其操作流程如下:
质量分数的另一种方案,其操作流程如下:
|
操 作 Ⅰ → 溶液转移 → 操作Ⅱ → 称量
①操作Ⅱ的名称是 。
②需直接测定的物理量是 。
③测定过程中需要的仪器有电子天平、蒸发皿、酒精灯,还需要 、 (固定、夹持仪器除外)。④在转移溶液时,如溶液转移不完全,则Na2O2质量分数的测定结果 (填偏大、偏小或不变)
9.此题包括两小题Ⅰ(8分)下图中A至F是化合物,G是单质.写出A、B、E、F的化学式A _____ B _____ E ______ F ____
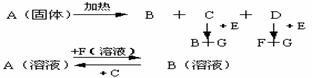
 Ⅱ(8分)X、Y、Z、W四种化合物均由短周期元素组成,其中X含有四种元素,X、Y、Z的焰色反应均为黄色,W为无色无味气体。这四种化合物具有下列转化关系(部分反应物、产物及反应条件已略去)。
Ⅱ(8分)X、Y、Z、W四种化合物均由短周期元素组成,其中X含有四种元素,X、Y、Z的焰色反应均为黄色,W为无色无味气体。这四种化合物具有下列转化关系(部分反应物、产物及反应条件已略去)。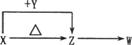 请回答:
请回答:
(1)X与Y在溶液中反应的离子方程式是 。
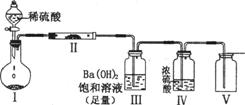
(2)X含有的四种元素之间(二种、三种或四种)可组成多种化合物,选用其中某些化合物利用上图装置(夹持固定装置己略去)进行实验,装置Ⅲ中生成白色沉淀,装置V中可收集到一种无色气体。
装置I中反应的化学方程式是 。
装置Ⅱ中反应的化学方程式是 。
装置Ⅲ中反应的化学方程式是 。
|
|
读数次数 |
质量/g |
|
锥形瓶 +水 +试样 |
第1次 |
192.214 |
|
第2次 |
192.164 |
|
|
第3次 |
192 028 |
|
|
第4次 |
192.010 |
|
|
第5次 |
192.010 |
7.在甲、乙、丙、丁四个烧杯内放入0.1 的钠、氧化钠、过氧化钠和氢氧化钠,然后各加入100
的钠、氧化钠、过氧化钠和氢氧化钠,然后各加入100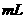 水,搅拌,使固体完全溶解,则甲、乙、丙、丁所得溶液里溶质的质量分数大小的顺序是( )
水,搅拌,使固体完全溶解,则甲、乙、丙、丁所得溶液里溶质的质量分数大小的顺序是( )
A.甲<乙<丙<丁 B. 丁<甲<乙=丙 C. 甲=丁<乙=丙 D.丁<甲<乙<丙
8往含0.2 mol NaOH和0.1 mol Ca(OH)2的溶液中持续稳定地通入CO2气体,当气体为6.72 L(S.T.P)时立即停止,则这一过程中,溶液中离子数目和通入CO2气体的体积关系正确的图象是(气体的溶解忽略不计):
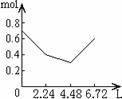
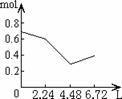
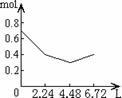
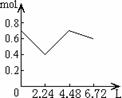
A B C D
6.某学生用NaHCO3和KHCO3组成的某混合物进行实验,测得如下数据(盐酸的物质的量浓度相等),下列分析推理不正确的是:
|
|
50ml盐酸 |
50ml盐酸 |
50ml盐酸 |
|
m(混合物) |
9.2g |
15.7g |
27.6g |
|
V(CO2)(标况) |
2.24L |
3.36L |
3.36L |
A.盐酸的物质的量浓度为3.0mol·L-1
B.根据表中数据可以计算出混合物中NaHCO3的质量分数
C.加入混合物9.2g时盐酸过量
D.15.7g混合物恰好与盐酸完全反应
5.把由Na2CO3·10H2O和NaHCO3组成的混合物7.4g溶于水配成100mL溶液,其中C(Na+)=0.6mol/L,若把等质量的混合物加热到恒重时,残留物的质量是
A.3.18g B.2.12g C.5.28g D.4.22g
4.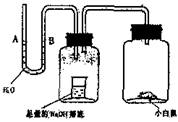 请据图回答,经数小时后,U型管(A)B两处的液面会出现下列哪种情况(实验装置足以维持实验期间小白鼠的生命活动,瓶口密封,忽略水蒸气和温度变化对实验结果的影响)
请据图回答,经数小时后,U型管(A)B两处的液面会出现下列哪种情况(实验装置足以维持实验期间小白鼠的生命活动,瓶口密封,忽略水蒸气和温度变化对实验结果的影响)
(A)A处上升,B处下降 (B)A、B两处都下降
(C)A处下降,B处上升 (D)(A)B两处都不变
2.一定温度下,Wg下列物质在足量氧气中充分燃烧,产物与过量的过氧化钠完全反应,过氧化钠固体增重Wg,符合此要求的是(1)H2 (2)CO (3)CO和H2 (4)HCOOCH3 (5)HOOC-COOH A.全部 B.仅(4)(5) C.仅(1)(2)(3) D.除(5)以外 3. 四种物质①氧化钠、②氢氧化钠、③过氧化钠、④亚硫酸钠。1 mol 上述固体物质,长期放置于空气中,最后质量增加情况是(不考虑潮解因素):( )
A.① = ② > ③> ④ B.① > ③ > ④ > ②
C.② > ① = ③ > ④ D.④ > ② > ③ > ①
1.已知钡的活动性处于钾和钠之间,则下述说法可能实现的是
A.钡可以从氯化钠溶液中置换出钠
B.钡投入到硫酸铜溶液中可得两种沉淀和一种气体
C.钡不能从冷水中置换出氢而得到H2
D.在溶液中钡离子可氧化金属锌
16.(06重庆)设NA代表阿伏加德罗常数,下列说法正确的是
A 5.6g铁与足量盐酸反应转移的电子数为0.3NA
B 100mL 2.0mol/L的盐酸与醋酸溶液中氢离子数均为0.2NA
C 标准状况下,22.4L氦气与22.4L氟气所含原子数均为2NA
D 20g重水(D2O)中含有的电子数为10NA
15、(08广东模拟)设NA代表阿伏加德罗常数的值,下列说法正确的是( )
A.1.8g铵根离子所含的电子数为1.1NA
B.1mol白磷分子所含共价键数为4NA
C.标准状况下,22.4L乙醇所含的分子数必定为NA
D.在电解食盐水的实验中,测得电解后溶液的pH为14,又知电解后溶液总体积为1L,则阴极析出的气体的分子数为0.5NA
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com