
题目列表(包括答案和解析)
13、FeS2的结构类似于Na2O2,是一种过硫化物,与酸反应时生成H2S2,H2S2类似H2O2易分解。实验室用稀盐酸与FeS2颗粒混合,则反应完毕后不可能生成的物质是
A.H2S B.S C.FeS D. FeCl2
12、有一不饱和的NaOH溶液。加入a mol Na2O、b mol Na2O2或c mol NaOH恰好得到NaOH饱和溶液(同一温度下).则a、b、c的关系为
A.a=b=c/2 B.a=b>c/2 C.a=b<c/2 D.a>b>c
11、实验室有一瓶久置的白色K2SO3粉末,为确定其是否被氧化及其成分,元素分析表明粉末中K和S元素的质量比为39 :16,下列结论正确的是
A.根据元素分析推测该粉末为纯净物
B.将粉末溶于水,加入氯化钡,有白色沉淀生成,证明原粉末是K2SO4
C.将粉末加入盐酸中,产生气泡,证明原粉末是K2SO3
D.将粉末溶于水,加氯化钡和过量盐酸,有白色沉淀和气泡生成 ,证明原粉末是K2SO4和K2SO3的混合物
10、某同学用回收的镁铝合金制取氢气。现有l0.8 g镁铝合金,下列说法正确的是
A.常温下与足量18mol/LH2SO4反应,最多可放出0.6 mol H2
B.常温下与足量2mol/LHNO3反应,最少可放出0.45 mol H2
C.常温下与足量2 mol/L H2SO4反应,放出H2的量在0.45 mol-0.6 mol之间
D.常温下与足量2mol/LNaOH反应,放出H2的量在0.45 mol-0.6 mol之间
9、下列离子方程式不正确的是
A.石灰石溶于盐酸:CaCO3+ 2H+=H2O + CO2↑+Ca 2+
B.溴化亚铁溶液中通入足量的氯气:2Fe2+ + 4Br-+ 3Cl2=2Fe3+ +2 Br2 + 6Cl-
C.在硫酸氢钾溶液中加入氢氧化钡溶液至pH=7:
Ba2++2OH-+2H++SO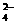 =BaSO4↓+2H2O
=BaSO4↓+2H2O
D.Fe3O4溶于稀HNO3中:Fe3O4 + 8H+ =Fe2+ + 2Fe3+ + 4H2O
8、下列溶液中一定能大量共存的离子组是
A.含有大量Al3+的溶液:Na+、NH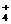 、SO
、SO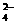 、Cl-
、Cl-
B.pH=1的溶液:Na+、K+、SO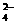 、CO
、CO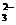
C.含有大量Fe3+的溶液:Na+、Mg2+、NO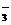 、SCN-
、SCN-
D.含有大量NO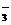 的溶液:H+、Fe2+、SO
的溶液:H+、Fe2+、SO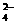 、Cl-
、Cl-
7、设NA为阿伏加德罗常数,下列叙述中正确的是
A.1molCl2与足量铁反应转移的电子数是3NA
B.1mol氧单质含有的原子数是1mol氖气含有的原子数的两倍
C.2.0gD2O中所含中子数为0.1NA
D.标准状况下,11.2L NO与11.2L O2混合后所含分子数小于NA
6、下列有关热化学方程式的叙述正确的是
A.已知2H2(g)+O2(g)=2H2O(l) △H=-571.6 kJ·mol-1,则氢气的燃烧热为285.8
kJ·mol-1
B.已知C(石墨,s)=C(金刚石,s) △H>0,则金刚石比石墨稳定
C.含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则稀醋酸和稀NaOH
溶液反应的热化学方程式为:
NaOH(aq)+CH3COOH(aq)=CH3COONa(aq)+H2O(l) △H=-57.4 kJ·mol-1
D.己知2C(s)+2O2(g)=2CO2(g) △H1;2C(s)+O2(g)=2CO(g) △H2,则△H1>△H2
5、水热法制备Fe3O4纳米颗粒的总反应为:
3Fe2++2S2O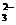 +O2+xOH-=Fe3O4+S4O
+O2+xOH-=Fe3O4+S4O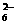 +2H2O
+2H2O
下列说法正确的是
A.硫元素被氧化,铁元素被还原 B.Fe2+、S2O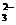 都是还原剂
都是还原剂
C.x=2 D.每生成1mol Fe3O4,则转移电子数为3mol
4、2008年9月25日,我国成功发射“神舟七号”载人飞船,宇航员可以天空行走,这标志着我国在航天领域的重大突破,下列说法正确的是
A.在发射航天飞船发射过程中,会看到有大量红色的烟雾,因为部分的N2O4会转化为NO2,该反应为分解反应,又为氧化还原反应
B.肼(N2H4)是发射航天飞船常用的高能燃料,液态N2O4常作为火箭的推进剂,反应中肼(N2H4)即作氧化剂,又作还原剂
C.火箭燃料肼(N2H4)与液态N2O4反应的产物是对环境无害的氮气和水蒸气,其中氮气是氧化产物,水蒸汽是还原产物
D.火箭燃料肼(N2H4)的结构类似氨,为共价化合物,但1mol N2H4可与2molHCl反应
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com