
题目列表(包括答案和解析)
16.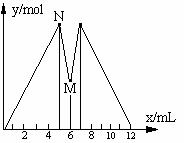 右下图是向MgCl2和AlCl3的混和溶液中加入NaOH溶液和盐酸时,沉淀的物质的量ymol与加入NaOH溶液和盐酸的体积x
mL的关系图,根据图示判断,下列结论中不正确的是( )
右下图是向MgCl2和AlCl3的混和溶液中加入NaOH溶液和盐酸时,沉淀的物质的量ymol与加入NaOH溶液和盐酸的体积x
mL的关系图,根据图示判断,下列结论中不正确的是( )
A、N点时溶液中的溶质只有NaCl
B、M点之前加入的是NaOH溶液,
M点之后加入的是盐酸
C、c(NaOH)=c(HCl)
D、原混合溶液中c(MgCl2):c(AlCl3)=1:2
15.在前一种分散系中慢慢滴加后一种试剂,能观察到先沉淀后变澄清的是
①氯化铝溶液中滴加氢氧化钠溶液②偏铝酸钠溶液中加盐酸
③氢氧化钠溶液中滴加氯化铝溶液④蛋白质溶液中滴入硫酸铜溶液
⑤氯化铝溶液中滴加氨水⑥硝酸银溶液中滴加氨水⑦氢氧化铁胶体滴加硫酸
A. ①②⑥⑦ B. ②③⑤⑦ C. ①②④⑥ D. ③④⑤
14.阿伏加德罗常数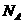 约为
约为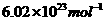 ,下列叙述中正确的是
,下列叙述中正确的是
A. 1 mol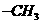 所含的电子数为7
所含的电子数为7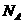
B. 在含196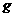
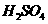 的浓硫酸溶液中加入足量的锌粉使其充分反应,则反应结束时,生成的
的浓硫酸溶液中加入足量的锌粉使其充分反应,则反应结束时,生成的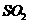 分子数约为
分子数约为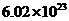 个
个
C. 标准状况下,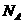 个
个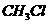 分子具有的体积约为22.4L
分子具有的体积约为22.4L
D. 常温下含有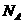 个
个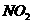 、
、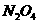 分子的混合气体,温度降至标准状况,其体积约为22.4L
分子的混合气体,温度降至标准状况,其体积约为22.4L
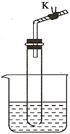
13.设计学生试验要注意安全、无污染、现象明显。根据启普发生器原理,可用底部有小孔的试管制简易的气体发生器(见右图)制取一试管气体。若关闭K,不能使反应停止,可将试管从烧杯中取出,但会有部分气体逸出。下列气体的制取宜使用该装置的是
 A.用二氧化锰(粉末)与双氧水制氧气
A.用二氧化锰(粉末)与双氧水制氧气
B.用锌粒与稀硫酸制氢气
C.用亚硫酸钠(块状)与硫酸制二氧化硫
D.用碳酸钙(块状)与稀硫酸制二氧化碳
12.12、甲、乙、丙、丁分别是Na2SO3、AgNO3、HCl、BaCl2四种无色溶液中的一种,它们两两反应后的现象如下:
甲+乙→沉淀 甲+丙→沉淀 乙+丙→沉淀
丙+丁→沉淀 乙+丁→无色刺激性气味气体,则甲、乙、丙、丁依次是( )
A、Na2SO3 HCl AgNO3 BaCl2
B、BaCl2 Na2SO3 HCl AgNO3
C、BaCl2 Na2SO3 AgNO3 HCl
D、AgNO3 HCl BaCl2 Na2SO3
11、在a L Al2(SO4)3和(NH4)2SO4的混合物溶液中加入b molBaCl2,恰好使溶液中的SO42-离子完全沉淀;如加入足量强碱并加热可得到c molNH3气,则原溶液中的Al3+离子浓度(mol/L) 为
A.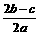 B.
B.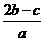 C、
C、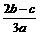 D.
D.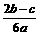
10.将1.12g铁粉加入到25ml 2mol/L的氯化铁溶液中,充分反应后,其结果是
A.铁有剩余,溶液呈浅绿色,氯离子浓度基本不变。
B.往溶液中加入无色KSCN溶液,不显色。
C.亚铁离子与铁离子物质的量之比为6 :1
D.氧化产物与还原产物物质的量之比2 :5
9.下列离子方程式中不正确的是( )
A、向Ba(OH)2溶液中逐滴加入H2SO4溶液至刚好沉淀完全:
Ba2++2OH-+2H++SO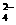 ===BaSO4↓+2H2O
===BaSO4↓+2H2O
B、用Pt电极电解MgCl2溶液:2Cl-+2H2O 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
C、碳酸氢钠溶液与硫酸氢钠溶液反应:HCO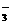 +H+===CO2↑+H2O
+H+===CO2↑+H2O
D、石灰石溶于醋酸: CaCO3+2CH3COOH===2CH3COO-+Ca2++CO2↑+H2O
8.在溶液中加入足量Na2O2后仍能大量共存的离子组是
A.NH4+、Ba2+、Cl-、NO3- B.K+、AlO2-、Cl-、SO42-
C.Ca2+、Mg2+、NO3-、HCO3- D.Na+、Cl-、CO32-、SO32-
7.现有200mL氯化镁和氯化镁的混合溶液,其中镁离子浓度为0.2mol/L,氯离子浓度为1.3mol/L。要使镁离子转化为氢氧化镁沉淀并镁离子和铝离子分离开来,至少需要4mol/L的氢氧化钠溶液
A.140ml B.120ml C.100ml D.80ml
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com