
题目列表(包括答案和解析)
24.(8分)从香料八角中提取的莽草酸是合成治疗禽流感的药物--达菲(Tamiflu)的原料之一,达菲是抗禽流感病毒特效药物。
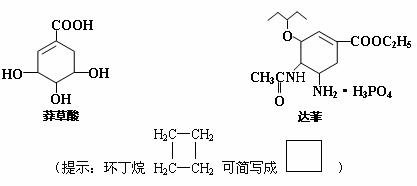
(1)莽草酸中含有的官能团有 ;(写名称)
(2)根据达菲分子的结构推测它可能发生的反应类型有: ;
(3)请写出莽草酸与乙醇反应的化学方程式(有机物用结构简式表示):
____________________________________________;
23.(5分)在一定条件下,在一个容积固定的反应器中,有一可左右滑动的密封隔板,两侧进行如图所示的反应(均加有适量的新型固体催化剂,其体积可忽略不计)
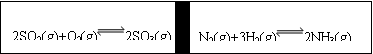
⑴若起始时两边分别投入2 mol SO2、1 mol O2;1 mol N2、3 mol H2,达到平衡后,隔板能否处于中央 (填“是”或“否”)。
⑵若起始时投入2 mol SO2、1 mol O2;1 mol N2、2 mol H2,达到平衡后,隔板仍处于中央,则SO2的转化率和N2的转化率之比为 (填数字);
⑶若起始时投入2 mol SO2、1 mol O2;1 mol N2、a mol H2、0.1 mol NH3,起始时右侧体积小于左侧体积,当a值在一定范围内变化时,均可通过调节反应器温度,使左右两侧反应都达到平衡,且平衡时隔板处于中央,此时SO2的转化率与N2的转化率之比为5:1,求a的取值范围 。
22.(5分)某未知溶液X中可能含有K+、Fe2+、NH4+、Cl-。检验其中是否含有K+,通常有如下两套实验方案。
方案一:焰色反应法
用洁净的玻璃棒蘸取未知液X置于酒精灯外焰上灼烧,观察到火焰呈黄色,则证明其中不含K+。对上述实验过程中的错误和疏漏之处加以纠正、补充:
、 。
方案二:亚硝酸钴钠法
在CH3COOH酸化的溶液中,K+与亚硝酸钴钠[Na3Co(NO2)6]反应生成黄色沉淀[K2NaCo(NO2)6],该原理可用于K+的检验。注意:NH4+也能与Na3Co(NO2)6生成黄色沉淀,会干扰K+离子的检验。
请你利用上述反应原理设计一个实验方案,检验未知溶液X中是否含有K+。
21.(9分)下图为某些常见物质之间的转化关系。已知:A、B、I中含有相同的阳离子且都是XY2型化合物,I是常用的干燥剂,单质F常用作自来水消毒。
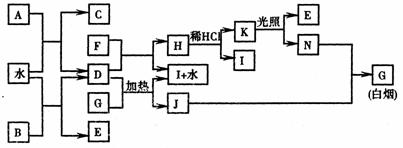
请按要求填空:
(1) A的电子式是 、B的电子式是 、
K的结构式是 、C的结构式是 ;
(2) D与G反应的化学方程式是 ;
(3 含1mol N的稀溶液与足量稀氢氧化钠溶液完全中和,放出57.3kJ的热量,则表示该反应中和热的热化学方程式为: 。
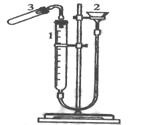
20.(12分)利用右图装置测定金属镁的相对原子质量。请根据要求回答有关问题:(所提供试剂有:0.48克镁带、18.4mol·L-1的H2SO4、2.0 mol·L-1的H2SO4)
实验方法如下:
⑴加药品前要检查该装置的气密性,较简便单的方法是:
。
⑵气密性检验后,按以下步骤进行实验,请回答有关问题:
①装硫酸。取下试管,加入 mol/L的H2SO4且体积应大于 ml。
②放置镁条。为保证产生的氢气不泄漏,应将镁条放置在 。
③记下量气管起始读数V1。
④将试管竖直,使镁条滑到试管中与酸反应;
⑤记下镁条反应完后的量气管读数V2。如何读数才能减少误差 。
⑶经测定镁与酸反应产生H2的体积为V L(已折算成标准状况),则镁的相对原子质量的表达式为(相对原子质量用M表示): 。
⑷如果测得的值比实际值偏大,请你分析产生误差偏大的可能原因(假设在测得外界温度、压强以及在换算、计算过程中都没有错误。至少写2条)
① ② 。
19.(9分) 请按要求填空:
⑴用已准确称量的1.06gNa2CO3固体配制0.100 mol·L-1Na2CO3溶液100mL,所需要的仪器为: ;
⑵除去KCl溶液中的SO42-离子,依次加入的试剂为(填溶质的化学式): ;
⑶如何判断SO42-离子已沉淀完全? 。
18.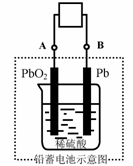 电瓶车所用电池一般为铅蓄电池,这是一种典型的可充电电池,电池总反应式为:
电瓶车所用电池一般为铅蓄电池,这是一种典型的可充电电池,电池总反应式为:
Pb+PbO2+4H++2SO42- 2PbSO4+2H2O
2PbSO4+2H2O
则下列说法正确的是:
A.充电时:阳极反应是4OH--4e-=O2↑+2H2O
B.放电时:正极反应是Pb-2e-+SO42- PbSO4
PbSO4
C.充电时:铅蓄电池的负极应与充电器电源的正极相连
D.放电时:电子流动方向由B到A
第Ⅱ卷(选择题 共56分)(答案填在答题卡上)
17. t℃时,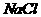 的溶解度为a g,取该温度下的饱和氯化钠溶液V
mL,测得其密度为
的溶解度为a g,取该温度下的饱和氯化钠溶液V
mL,测得其密度为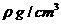 ,则下列表达式正确的是
,则下列表达式正确的是
A. 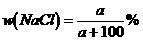
B. 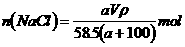
C. 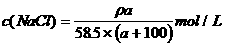
D. 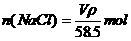
16.下列叙述正确的是
A.常温下,0.01mol/LCH3COOH与pH=12的NaOH溶液混合,若混合后c(CH3COO-)>c(Na+),则混合液一定呈碱性
B.常温下,将等体积0.01mol/LHCl与pH=12的氨水混合,则混合液的pH=7
C.0.1mol/L的某二元弱酸盐Na2A溶液中,c(Na+)=2c(H2A)+2c(HA‑)+2c(A2-)
D.将5 mL 0.02mol/L的H2SO4与5 mL 0.02mol/LNaOH溶液充分混合,若混合后溶液的体积为10mL,则混合液的pH=2
15.一定能在下列溶液中大量共存的离子组是
A.水电离产生的c(H+)=1×10-12mol/L溶液:NH4+、Na+、Cl-、I-
B.能使pH试纸变深蓝色的溶液中:Na+、AlO2-、S2-、CO32-
C.含有大量Fe3+的溶液:HCO3-、Cu2+、K+、Br-
D.澄清透明的无色溶液中:ClO-、SCN-、Al3+、SO42-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com