
题目列表(包括答案和解析)
25、(10分)将某有机物样品3.0g通入足量的氧气后充分燃烧,在120℃条件下将燃烧后的气体通入足量的浓H2SO4中,浓H2SO4增重1.8g,然后将气体再通入足量的氢氧化钡溶液中,可得到沉淀19.7g(不考虑溶解的沉淀物),此时还有标准状况下的气体2.24L,该气体能用于抢救危重病人。实验测得该有机物蒸气的密度是相同条件下氦气的15倍。求该有机物的分子式和通入氧气的总体积(标准状况)?
24、(10分)某制糖厂以甘蔗为原料制糖,同时得到大量的甘蔗渣,对甘蔗进行综合利用,不仅可以提高经济效益,而且还能防止环境污染。现按下列方式进行综合利用,回答问题。
|
|
|
||||||

 甘蔗渣 处理
水、△
酒化酶
甘蔗渣 处理
水、△
酒化酶

 催化剂
催化剂
在人体中 缓慢氧化 催化氧化
 C
△
C
△
|





 H
+D
新制Cu(OH)2
E 浓H2SO4 F
H
+D
新制Cu(OH)2
E 浓H2SO4 F
△浓H2SO4
已知F、H均是具有香味的液体,F为E的三聚合物,并具有特殊的6元环状对称结构。
⑴ A的名称 ;H的名称 ;
 ⑵
D
E的化学反应方程式 ;
⑵
D
E的化学反应方程式 ;
 ⑶ G H的化学反应方程式
;
⑶ G H的化学反应方程式
;
 ⑷
E
G的反应类型
。
⑷
E
G的反应类型
。
23、(10分)有甲基、苯基、羟基、羧基四种基团,在它们两两组合形成的化合物中:
(1)能使石蕊试液变色的是 (只需写出一种物质的结构简式,下同);
(2)能与溴水反应的是 ;
(3)催化氧化后产物能与新制氢氧化铜反应的是 ;
(4)能与氯化铁溶液反应的是 ;
(5)不同情况下与氢氧化钠反应能生成两种盐的是 。
22、(8分)麻醉剂的发现和使用,是人类医疗史上了不起的一项成就,它可使患者在接受治疗时感觉不到疼痛。
(1)笑气是人类最早应用于医疗的麻醉剂之一,它可由NH4NO3在微热条件下分解产生,产物除N2O外还有一种,此反应的化学方程式为 。有关理论认为N2O与CO2分子具有相似的结构(包括电子式),则其空间构型是 型,N2O为 分子(极性或非极性)
(2)另一种常用麻醉剂氯仿,常因保存不慎而被氧化,产生剧毒光气(COCl2):2CHCl3+O2 2HCl+2COCl2,为了防止事故,使用前可用于检验氯仿是否变质的试剂是
。
A.淀粉一碘化钾溶液 B.NaOH溶液 C.酚酞溶液 D.硝酸酸化的AgNO3溶液
21、(10分)在一定条件下,金属单质X和非金属单质Y能够反应,生成化合物Z,Z能与水发生水解反应生成气体G和白色沉淀P(如下框图所示),已知气体G与空气之密度比约为1.17。请填空:
⑴ 组成单质X和Y的元素分别属第 族和第 族;
⑵ Z与水发生水解反应方程式 ;
⑶ 每生成1mol的化合物Z,反应中转移 mol的电子。

20、(12分)工业制纯碱,是向饱和食盐水中通入氨气和二氧化碳,获得碳酸氢钠晶体,它的反应原理可用下列化学方程式表示:
NH3+CO2+H2O=NH4HCO3……………………………………①
NH4HCO3+NaCl(饱和)=NaHCO3↓+NH4Cl………………②
将所得碳酸氢钠晶体加热分解后即可得到纯碱。请回答:
(1)工业所制纯碱中常含有少量的氯化钠杂质,其原因 ;
(2)现有甲、乙、丙三个小组的学生,欲测定某工业纯碱样品中Na2CO3的质量分数,分别设计并完成实验如下。
甲组:取10.00g样品,利用下图所示装置,测出反应后装置C中碱石灰的增重为3.52g。
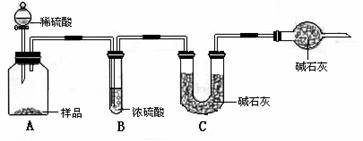
乙组:取10.00g样品,配成1000mL溶液,用碱式滴定管量取25.00mL放入锥形瓶中,加入甲基橙作指示剂,用0.150mol·L-1的标准盐酸溶液滴定至终点(有关反应为Na2CO3+2HCl=2CaCl2+H2O+CO2↑)。完成三次实验后,消耗盐酸体积的平均值为30.00mL。
丙组:取10.00g样品,向其中加入过量的盐酸,直至样品中无气泡冒出,加热蒸发所得物并在干燥器中冷却至室温后称量。反复加热、冷却、称量,直至所称量的固体质量几乎不变为止,此时所得固体的质量为10.99g。
请分析、计算后填表:
|
分析与 计算 分组 |
计算样品中碳酸钠 的质量分数 |
对实验结果 的评价 |
实验失败的主要原因 及对结果的影响 |
|
甲组 |
|
失败 |
|
|
乙组 |
|
成功 |
|
|
丙组 |
|
成功 |
|
19、(8分)指出在使用下列仪器(已经洗涤干净)或用品时的第一步操作:
(1)石蕊试纸(检验气体): 。
(2)容量瓶: 。
(3)酸式滴定管: 。
(4)集气瓶(收集氯化氢): 。
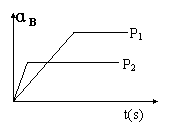
18、A(g)+2B(g)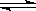 X C(g)的可逆反应,在不同压强(P1、P2)下测得B的转化率跟反应时间的关系如图所示,下列结论正确的是
X C(g)的可逆反应,在不同压强(P1、P2)下测得B的转化率跟反应时间的关系如图所示,下列结论正确的是
A.P1>P2 X>3 B.P1<P2 X>3
C.P1<P2 X<3 D.P1>P2 X<3
第二卷 (非选择题共78分)
17、由下列各物质所配成的0.2mol/L溶液中,离子浓度大小排列正确的是:
A.NH4Cl溶液中:C(Cl-)>C(NH4+)>C(H+)>C(OH-)
B.Na2CO3溶液中:C(Na+)>C(CO32-)>C(HCO3-)>C(H+)>C(OH-)
C.NaHCO3溶液中:C(Na+)>C(HCO3-)>C(CO32-)>C(OH-)>C(H+)
 D.(NH4)2SO4溶液中:C(NH4+)>C(SO42-)>C(OH-)>C(H+)
D.(NH4)2SO4溶液中:C(NH4+)>C(SO42-)>C(OH-)>C(H+)
16、下列关于铜电极的叙述正确的是
A.铜锌原电池中铜是正极 B.用电解法精炼粗铜时,粗铜作阴极
C.在镀件上电镀铜时,可用金属铜作阳极 D.电解稀硫酸制H2、O2时,铜作阳极
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com