
题目列表(包括答案和解析)
17. (7分)用37%,密度为1.19 g·cm-3的浓盐酸配制0.1 mol·L-1的稀盐酸500 mL,请回答: ⑴所需浓盐酸的体积为 mL; ⑵此实验配制稀盐酸,除玻璃棒、胶头滴管、试剂瓶外,还需的仪器有 、__________和 。
⑶如果在配制时,第一次加水量太少,搅拌时间较长,对配制溶液的浓度有什么影响? (“偏高”“偏低”或“无影响“)
16. 在反应3BrF3+5H2O=HBrO3+9HF+Br2+O2↑,若有0.3molH2O被氧化,则被水还原的BrF3的物质的量是 A.0.15mol B.0.2mol C.0.3mol D.0.4mol
第Ⅱ卷(非选择题 共86分)
15. 根据相关化学原理,下列判断正确的是 ( )A.若X是原子晶体,Y是分子晶体,则熔点:X<Y B.若A2 + 2D- = 2A- + D2,则氧化性:D2 > A2 C.若R2-和M+的电子层结构相同,则原子序数:R<M D.若金刚石质量为12g,则共价键总数为4NA
14. 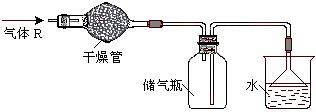 在实验室里可按图所示的装置来干燥、收集气体R,多余的气体R可用水吸收,则R是
(
)
A.HCl
在实验室里可按图所示的装置来干燥、收集气体R,多余的气体R可用水吸收,则R是
(
)
A.HCl
B.Cl2
C.CO
D.NH3
13. 第28届国际地质大会提供的资料显示,海底有大量的天然气水合物,可满足人类1000年的能源需要。天然气水合物是一种晶体,晶体中平均每46个水分子构建成8个笼,若晶体中每8个笼只有6个容纳了CH4分子,另外2个笼被游离H2O分子填充,则天然气水合物的平均组成可表示为 ( ) A.CH4·8H2O B.CH4·14H2O C.CH4·(23/3)H2O D.CH4·6H2O
12. 在下列化学反应中,既有离子键、极性键、非极性键断裂,又有离子键、极性键、非极性键形成的是 ( ) A.CaC2 + 2H2O → Ca(OH)2 + HC≡CH ↑ B.2Na2O2 + 2H2O=4NaOH + O2↑
C.MgCl2 + 2NaOH=Mg(OH)2↓+2NaCl D.2NaOH+Cl2=NaCl+NaClO+H2O
11. 对于某些离子的检验及结论一定正确的是 ( ) A.加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32¯ B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42¯ C.加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+ D.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,不一定有Ba2+
10. 水的状态除了气、液和固态外,还有玻璃态。它是由液态水急速冷却到165K时形成的,玻璃态的水无固定形状,不存在晶体结构,且密度与普通液态水的密度相同。有关玻璃态水的叙述正确的是 ( )A.水由液态变为玻璃态,体积缩小 B.水由液态变为玻璃态,体积膨胀 C.玻璃态是水的一种特殊状态 D.玻璃态水是分子晶体
9. 下列有关叙述正确的是 ( ) A.电解质的导电性和金属晶体的导电性都随温度的升高而降低 B.“加碘食盐”、“高钙牛奶”、“含氟牙膏”、“富硒营养品”等等,这里的碘、钙、氟、硒指的是分子 C.“冰,水为之,而寒于水”说明相同质量的水和冰,水的能量高 D.用“摩尔”(而不用“个”)计量微观粒子与用“纳米”(而不用“米”)计量原子直径,计量思路都是扩大单位
8. 下列保存物质的方法正确的是 ( ) A.氢氟酸保存在玻璃瓶中 B.氯水应保存在棕色的细口瓶中 C.NaOH溶液存放在配有磨口玻璃塞的棕色玻璃瓶中 D.金属锂应保存在煤油中防止被氧化
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com