
题目列表(包括答案和解析)
6.温度相同、浓度均为0.2 mol/L的①(NH4)2SO4、②NaNO3、③NH4HSO4、④NH4NO3、
⑤ ⑥CH3COONa溶液,它们的pH值由小到大的排列顺序是
⑥CH3COONa溶液,它们的pH值由小到大的排列顺序是
A. ③①④②⑥⑤ B. ①③⑥④②⑤
C. ③②①⑥④⑤ D. ⑤⑥②④①③
5.室温下,在强酸性和强碱性溶液中都不能大量共存的离子组是
A.NH+4、Cu2+、Cl-、NO-3 B.K+、Na+、SO2-3、S2-
C.K+、Na+、AlO-2、SO2-4 D.Ba2+、Fe2+、NO-3、Br-
4.下列描述中,不符合生产实际的是
A.电解熔融的氧化铝制取金属铝,用铁作阳极 B.电解法精炼粗铜,用纯铜作阴极
C.电解饱和食盐水制烧碱,用涂镍碳钢网作阴极 D.在镀件上电镀锌,用锌作阳极
2.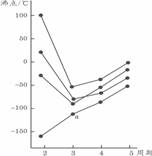 右图中每条折线表示周期表ⅣA-ⅦA中的某一族元素氢化物的沸点变化,每个小黑点代表一种氢化物,其中a点代表的是
右图中每条折线表示周期表ⅣA-ⅦA中的某一族元素氢化物的沸点变化,每个小黑点代表一种氢化物,其中a点代表的是
A.H2S B.HCl C.PH3 D.SiH4 3.下列有关叙述正确的是
A. “神舟六号”飞船返回舱的表层采用高温时自动烧蚀的耐高温、抗氧化的新型无机非金属材料带走热量从而保证内部温度不致过高。
 B.“加碘食盐” “含氟牙膏”“富硒营养品” “高钙牛奶”“加铁酱油”等等,这里的碘、氟、硒指的是分子,钙、铁则分别是钙离子和铁离子。
B.“加碘食盐” “含氟牙膏”“富硒营养品” “高钙牛奶”“加铁酱油”等等,这里的碘、氟、硒指的是分子,钙、铁则分别是钙离子和铁离子。
C. 右图是反应物和生成物的能量变化示意图,则其可能发生的反 应的热化学方程式可表示为:
2 A(g)+ B(g) = 2 C(g);△H=Q kJ·mol-1(Q<0 )
D.电解水制取氢气和氧气时,通常加入硫酸钠等强电解质,这说明强电解质的导电性比弱电解质的强
1.一种新型材料B4C,它可用于制作切削工具和高温热交换器。关于B4C的推断正确的是
A.B4C是一种分子晶体 B.B4C是一种离子晶体
C.B4C是一种原子晶体 D.该分子是有4个硼原子和1个碳原子构成
24.(10分)将Na2O2和NaHCO3固体混合物置于密闭容器中加充分反应,放出气体后冷却。加热时可能发生的反应如下:
2 Na2O2+2NaHCO3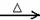 2NaOH+2Na2CO3+O2↑
2NaOH+2Na2CO3+O2↑
2 Na2O2+4NaHCO3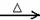 4Na2CO3+O2↑+2H2O
4Na2CO3+O2↑+2H2O
2NaHCO3 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
(1)若固体混合物的质量为m,反应后冷却再称其质量减少了△m。设NaHCO3、Na2O2的物质的量分别为a,b,试确定下列条件下△m的取值范围(用含m的代数式表示)。
①当a/b≤1时,△m取值范围是
②当1<a/b≤2时,△m取值范围是
③当a/b>2时,△m取值范围是
(2)若m=14.52g,△m=1.28g时,向反应后的残留固体内滴加2.00mol/L盐酸140.0mL,可产生标准状况下的气体 L。
23.(8分)将一定量的氯酸钾与3.48g二氧化锰组成的混合物加热一段时间后共收集到氧气0.336L(标准状况),然后将残留固体加入到足量浓盐酸中共热,使之与浓盐酸充分反应,再将生成的气体全部通入到100ml 1mol/L的溴化亚铁溶液中,有一半的溴离子被氧化成单质。求氯酸钾的分解率。
22.(10分)下图表示各物质之间的转化关系。已知:
Ⅰ.A是无色液体,L是不溶于稀硝酸的白色沉淀,E、F、H、J、X、Y、Z是气体;
Ⅱ.G、X、Y、Z是单质,其它是化合物,其中Y呈黄绿色、H呈红棕色,E和F都极易溶解于水,二者相遇会有白烟生成;
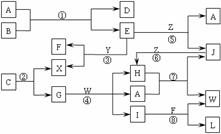 Ⅲ.B和C都是由一种金属与一种非金属元素组成的化合物,其中非金属元素相同且质量分数都是28%,组成B的金属元素原子核外的K层和M层电子数相同。
Ⅲ.B和C都是由一种金属与一种非金属元素组成的化合物,其中非金属元素相同且质量分数都是28%,组成B的金属元素原子核外的K层和M层电子数相同。
请按要求填空:
(1)写出下列物质的化学式:B___________,C___________;
(2)上述反应中属于置换反应的是_________;不属于氧化还原反应的是__________;(填写反应代号)
(3)反应④的离子方程式为:_____________________________________________。
21.Ⅰ.(10分)下表是元素周期表的前三周期,用相应的化学用语回答下列问题:
|
|
|
|
|
|
|
|
|
|
a |
|
|
b |
c |
d |
e |
|
|
f |
|
g |
|
|
|
|
|
(1)g的单质能与f元素的最高价氧化物对应的水化物的溶液反应,请写出该反应的离子方程式 。
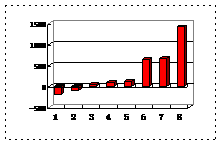
(2)第三周期8种元素按单质熔点(℃)大小顺序的柱形图(上左图),其中序列“2”代表 ,“8”代表 。
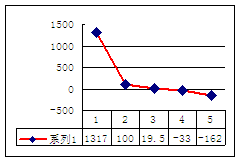
(3)a、b、c、d、e的氢化物的沸点直角坐标图(上右图),序列“5”氢化物的化学式为 ,序列“1”的氢化物的电子式: 。
Ⅱ.(10分)已知氨分子内键与键的夹角约为107º18’。从反应NH3 +H+→NH4+可知:NH4+中有一根键比较特殊,其结构可表示为A式。但是,虽然有一根键形成过程与众不同,而其结果是完全相同的,都是N、H原子间共用一对电子,键与键的夹角均为109º28’。故NH4+的结构也可表示为B式。
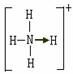
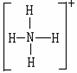
A式 B式
(1)还有一些你熟悉的分子或离子中,也存在上述特殊共价键,如: 等。
(在下列微粒中选择填空:[Ag(NH3)2]+,PCl5,Fe(SCN)3,NH3·H2O ,H3O+)
(2)写出H3O+的电子式 ;
你认为H3O+中键与键的夹角与下列哪个角度最接近?
A.120º B.109º28’ C.107º18’ D.60º
(3)氮化硼(BN)是一种新型无机非金属材料,它有两种晶型:金刚石晶型和石墨晶型。其中,金刚石晶型的氮化硼材料具有硬度大、熔点高等特性,它的结构中也含有上述特殊共价键。则:在金刚石晶型的氮化硼中,每个硼原子与 个氮原子以B─N键连接,原子间相互连接的最小的环上有 个氮原子和 个硼原子。
20.(12分)已知A、B、C、D的组成元素都属于短周期,其中A、D为单质,B、C为化合物,它们之间的简单转化关系如图所示。请按要求写出有关反应式,是离子反应的只写离子方程式:
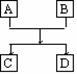 (1)若A、D的组成元素同主族:
(1)若A、D的组成元素同主族:
①B是水:__________________________________________。
②B、C均为氧化物(反应有重要的工业价值):
____________________________________________,工业价值是:_________________。
(2)若A、D的组成元素不同主族:
①B是水且水是还原剂:__________________________________________;
B是水且水是氧化剂(反应有重要的工业价值):
____________________________________________,工业价值是:_________________。
②B、C均为氧化物:____________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com