
题目列表(包括答案和解析)
18.容积相同的甲、乙密闭容器,甲为恒容、乙为恒压,分别充入
2 molSO2和1 mol
O2,同时发生反应: 2SO2(g)+O2(g) 2SO3(g),同温度下分别达到平衡,测得甲中SO2的转化率为25%,下列说法中正确的是
2SO3(g),同温度下分别达到平衡,测得甲中SO2的转化率为25%,下列说法中正确的是
A.反应过程中甲容器中的反应速率比乙中的大
B.甲容器反应达到平衡时所需时间比乙容器少
C.乙容器中SO2的转化率大于25%
D.平衡时,乙容器中SO2、O2、SO3的浓度之比一定为2:1:2
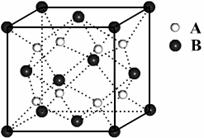
17.某离子晶体的晶体结构中最小重复单元如右图所示:A为阴离子,在正方体内,B为阳离子,分别在顶点和面心,则该晶体的化学式为
A.B2A B.BA2
C.B7A4 D.B4A7
16.下列离子方程式中不正确的是
A.向Ba(OH)2溶液中逐滴加入H2SO4溶液至刚好沉淀完全:
Ba2++OH-+H++SO =BaSO4↓+H2O
=BaSO4↓+H2O
B.用Pt电极电解MgCl2溶液:2Cl-+2H2O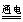 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
C.碳酸氢钠溶液与硫酸氢钠溶液反应:HCO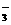 +H+=CO2↑+H2O
+H+=CO2↑+H2O
 D.石灰石溶于醋酸:CaCO3+2CH3COOH=2CH3COO-+ Ca2++CO2↑+H2O
D.石灰石溶于醋酸:CaCO3+2CH3COOH=2CH3COO-+ Ca2++CO2↑+H2O
15.下列说法可以实现的是:①酸性氧化物均能与碱发生反应;②盐溶液与弱酸反应可以生成强酸;③发生复分解反应,但产物既没有水生成,也没有沉淀和气体生成;④两种酸溶液充分反应后,所得溶液呈中性;⑤有单质参加反应,但该反应不是氧化还原反应
A.②③④⑤ B.①③④⑤ C.①②③⑤ D.①②③④⑤
14.在一定条件下,硫酸铵的分解反应为:4(NH4)2SO4=N2↑+6NH3↑+3SO2↑+SO3↑+7H2O当有n mol电子转移时,下列说法不正确的是
A.有2n mol (NH4)2SO4分解 B.有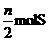 原子被还原
原子被还原
C.生成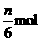 氧化产物 D.生成7n mol H2O
氧化产物 D.生成7n mol H2O
13.A、B、C、D、E五种短周期元素。A、B、C位于同一周期相邻位置,A和C的原子序数之比为3∶4,A、B、C分别与D形成的化合物分子中都含有10个电子。E的原子结构示意图中从内到外各层的电子数之比为1∶4∶1。则下列叙述中正确的是
A.A和C形成的某种化合物能与E的单质在一定条件下发生置换反应
B.实验室制备B、D两种元素形成的化合物发生的反应属于氧化还原反应
C.由A、C原子和B、D原子分别构成的分子都是极性分子
D.由A、B、C、D四种元素组成的化合物中不可能含有离子键
12.在下列化学反应中,既有离子键、极性键、非极性键断裂,又有离子键、极性键、非极性键形成的是
|
C.Mg3N2 + 6H2O=3Mg(OH)2↓+2NH3↑ D.NH4Cl +NaOH === NaCl + H2O + NH3 ↑
11.有X、Y、Z、M四种金属,已知:X可以从Y的盐溶液中置换出Y;X和Z作原电池电极时,Z为正极;Y和Z的离子共存于电解液中,Y离子先放电;M的离子氧化性强于Y的离子。则这四种金属的活动性由强到弱的顺序是
A.X>Y>Z>M B.X>Z>M>Y C.M>Z>X>Y D.X>Z>Y>M
10.某溶液中含有CH3COO-、SO42-、SO32-、HCO3-、CO32-等五种离子。将过量的Na2O2固体加入其中后,仍能大量存在的离子是
A.CH3COO-、SO42-、CO32- B.SO42-、SO32-、CO32-
C.SO32-、HCO3- D.CH3COO-、SO42-、HCO3-
9.某学生欲完成2HCl+2Ag=2AgCl↓+H2↑反应,设计了下列四个实验,你认为可行的实验是

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com