
题目列表(包括答案和解析)
1.2-甲基丁烷与氯气发生取代反应,所得一氯取代物可能有
A.一种 B.两种 C.三种 D.四种
29、I、(5分).烧过菜的铁锅未及时洗净(残液中含NaCl),第二天便出现红棕色锈斑(该锈斑为Fe(OH)3失水的产物)。试用有关电极反应式、离子方程式和化学方程式表示Fe(OH)3的生成过程。
(1)负极:_______________________;
(2)正极:_______________________;
(3)离子方程式:_________________;
(4)化学方程式:_________________;
(5)总方程式:___________________。
Ⅱ(7分)、将洁净的金属片A、B、C、D分别放置在浸有盐溶液的滤纸上面并压紧(如图所示)。在每次实验时,记录电压表指针的移动方向和电压表的读数如下:

|
金属 |
电子流动方向 |
电压(V) |
|
A |
A→Cu |
+0.78 |
|
B |
Cu→B |
-0.15 |
|
C |
C→Cu |
+1.35 |
|
D |
D→Cu |
+0.30 |
已知:构成两电极的金属活泼性相差越大,电压表的读数越大。
请依据表中数据判断:
(1)______金属可能是最强的还原剂;______金属一定不能从硫酸铜溶液中置换出铜。
(2)若滤纸不用盐溶液浸润而改用NaOH溶液浸润,则在滤纸上能看到有蓝色沉淀析出的是________(填字母)金属。其对应的原电池的电极反应式为:
负极____________________________,正极______________________________。
28、(06江苏25)(10分)利用太阳光分解水制氢是
未来解决能源危机的理想方法之一。某研究小组设计
了如右图所示的循环系统实现光分解水制氢。反应
过程中所需的电能由太阳能光电池提供,反应体系
中I2和Fe3+等可循环使用。
⑴写出电解池A、电解池B和光催化反
应池中反应的离子方程式。
⑵若电解池A中生成3.36 L H2(标准状况),
试计算电解池B中生成Fe2+的物质的量。
⑶若循环系统处于稳定工作状态时,电解池A中流
入和流出的HI浓度分别为a mol·L-1和b mol·L-1,
光催化反应生成Fe3+的速率为c mol·min-1,循环
系统中溶液的流量为Q(流量为单位时间内流过的溶液体积)。试用含所给字母的代数式表示溶液的流量Q。
27、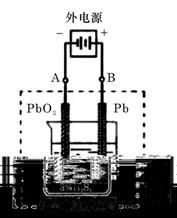 I、(06北京卷)(9分)铝和氢氧化钾都是重要的工业产品。请回答:
(1)工业冶炼铝的化学方程式是__________________________.
(2)铝与氢氧化钾溶液反应的离子方程式是_________________________.
(3)工业品氢氧化钾的溶液中含有某些含氧酸杂质,可用离子交换膜法电解提纯。
电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示.
I、(06北京卷)(9分)铝和氢氧化钾都是重要的工业产品。请回答:
(1)工业冶炼铝的化学方程式是__________________________.
(2)铝与氢氧化钾溶液反应的离子方程式是_________________________.
(3)工业品氢氧化钾的溶液中含有某些含氧酸杂质,可用离子交换膜法电解提纯。
电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示.
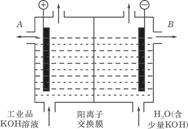 ①该电解槽的阳极反应式是____________________________.
②通电开始后,阴极附近溶液pH会增大,请简述原因________________________
①该电解槽的阳极反应式是____________________________.
②通电开始后,阴极附近溶液pH会增大,请简述原因________________________
___________________________________________________________________________
③除去杂质后的氢氧化钾溶液从溶液出口______(填写“A”或“B”)导出
Ⅱ(06重庆理综27).(14分)(请在答题卡上作答)
铅蓄电池是典型的可充型电池,它的正负极格板是惰性材料,电池总反应式为:
Pb+PbO2+4H++2SO2-4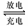 2PbSO4+2H2O
2PbSO4+2H2O
请回答下列问题(不考虑氢、氧的氧化还原):
(1) 放电时:正极的电极反应式是______________;电解液中H2SO4的浓度将变________;当外电路通过1 mol电子时,理论上负极板的质量增加________g。
(2) 在完全放电耗尽PbO2和Pb时,若按题27图连接,电解一段时间后,则在A电极上生成__________、B电极上生成________,此时铅蓄电池的正负极的极性将________________________。
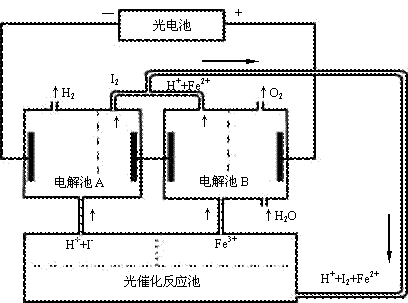
13.25℃将两个铜电极插入含有一定量硫酸钠的饱和溶液中进行电解。通电一段时间后,阴极上析出a mol气体,同时有wgNa2SO4·10H2O晶体析出,则溶液中该溶质的质量分数为(C )
 ,
,
 .
.
. 第Ⅱ卷(非选择题,共60分)
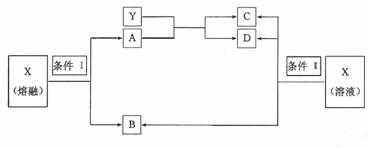 二、26(14分)已知A、B、C、D、X、Y六种物质均由短周期元素组成,其中X为常见离子化合物,它们之间的转换关系如下图所示
二、26(14分)已知A、B、C、D、X、Y六种物质均由短周期元素组成,其中X为常见离子化合物,它们之间的转换关系如下图所示
(1)已知条件I和条件II相同,则该反应条件为
(2)物质X的电子式为
(3)写出B与Ca(OH)2反应的化学方程式
(4)写出X在条件II下反应生成B、C、D的离子方程式
(5)写出实验室制B的化学方程式,并标出电子转移方向、数目
(6)请简述鉴定物质X的实验方法: .
。
11.(06广东16)某可充电的锂离子电池以LiMn2O4为正极,嵌入锂的碳材料为负极,含Li+导电固体为电解质。放电时的电池反应为:Li+LiMn2O4==Li2Mn2O4。下列说法正确的是
A.放电时,LiMn2O4发生氧化反应 B.放电时,正极反应为:Li++LiMn2O4+e-==Li2Mn2O4
C.充电时,LiMn2O4发生氧化反应 D.充电时,阳极反应为:Li++e-==Li
12(2000全国17)下列关于胶体的叙述不正确的是
A.布郎运动是较体微粒特有的运动方式,可以据此把胶体和溶液、悬浊液区别开来
B.光线透过胶体时,胶体发生丁达尔现象
C.用渗析的方法净化胶体时,使用的半透膜只能让较小的分子、离子通过
D.胶体微粒具有较大的表面积,能吸附阳离子或阴离子,故在电场作用下会产生电泳现象
10.(2000 全国18)下列关于实验现象的描述不正确的是
A.把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡
B.用锌片做阳极,铁片做做阴极,电解氯化锌溶液,铁片表面出现一层锌
C.把铜片插入三氯化铁溶液中,在铜片表面出现一层铁
D.把锌粒放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出速率加快
8、(06四川理综11)下列描述中,不符合生产实际的是
A、电解熔融的氧化铝制取金属铝,用铁作阳极 B、电解法精炼粗铜,用纯铜作阴极
C、电解饱和食盐水制烧碱,用涂镍碳钢网作阴极 D、在镀件上电镀锌,用锌作阳极
9(06上海13)将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是
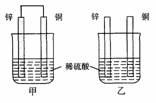 A.两烧杯中铜片表面均无气泡产生 B.甲中铜片是正极,乙中铜片是负极
A.两烧杯中铜片表面均无气泡产生 B.甲中铜片是正极,乙中铜片是负极
C.两烧杯中溶液的pH均增大 D.产生气泡的速度甲比乙慢
7. (06天津理综12)我国首创的海洋电池以铝板为负极,铂网为正极,海水为电解质溶液,空气中的氧气与铝反应产生电流。电池总反应为:4Al+3O2+6H2O=4Al(OH)3,下列说法不正确的是
A.正极反应为:O2+2H2O+4e-=4OH- B.电池工作时,电流由铝电极沿导线流向铂电极
C.以网状的铂为正极,可增大与氧气的接触面积 D.该电池通常只需要更换铝板就可继续使用
6.(06全国理综I 9)把分别盛有熔融的氯化钾、氯化镁、氯化铝的三个电解槽串联,在一定条件下通电一段时间后,析出钾、镁、铝的物质的量之比为:
A.1:2:3 B.3:2:1 C.6:3:1 D.6:3:2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com