
题目列表(包括答案和解析)
8.下列依据热化学方程式得出的结论正确的是
A.已知2H2(g) +O2(g)=2H2O(g); △H=-483.6kJ·mol-1
则2g氢气燃烧生成液态水时放热为241.8 kJ·mol-1
B.已知C(石墨,s)=C(金刚石,s),△H>0 则金刚石比石墨稳定
C.已知2C(s)+2O2(g)=2CO2(g);△H1 2C(s)+O2(g)=2CO(g);△H2,则△H1>△H2
D.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l); △H=-57.6 kJ·mol-1
则含20.0gNaOH的稀溶液和稀盐酸完全中和,放出28.7kJ的热量
7.NA表示阿伏加德罗常数,下列叙述正确的是
A.如果5.6LN2含有n个氮分子,则阿伏加德罗常数一定约为4n
B.46gNO2和N2O4混合气体中含有原子数为3NA
C.含有1mol碳原子的金刚石,C-C共价键数为2NA
D.常温下1mol氯气与熟石灰完全反应转移电子数为2NA
6.在元素周期表短周期中的X和Y两种元素可组成化合物XY3,下列说法正确的是( )
A.XY3晶体一定是离子晶体
B.若Y的原子序数为n,X的原子序数一定是n±4
C.X和Y可属于同一周期,也可属于两个不同的周期
D.X和Y一定不属于同一主族
5.下列括号内所选试剂达不到检验效果的是
A.K2SO3溶液是否被氧化(BaCl2)溶液 B.FeSO4溶液是否变质(KSCN溶液)
C.KI溶液是否被氧化(淀粉溶液) D.Na2O2粉末是否完全变质(H2O)
4.下列事实不能用平衡移动原理解释的是
A.在H2S溶液中滴加NaOH,S2-浓度增大
B.加催化剂在一定条件下使N2和H2转化为NH3
C.加压有利于SO2与O2反应生成SO3
D.可用浓氨水和氢氧化钠固体来快速制取氨气
3.下列解释不科学的是
A.“水滴石穿”主要是溶解了CO2的雨水与CaCO3长期作用下成了Ca(HCO3)2的缘故
B.长期盛放NaOH溶液的滴瓶不易打开,是因为NaOH与瓶中的CO2反应导致瓶内气体减少形成“负压”的缘故。
C.严格地讲,“通风橱”是一种不负责任的污染手段,因为实验产生的有害气体没有得到转化或吸收
D.“雨后彩虹”、“海市蜃楼”,既是一种自然现象又是光学现象,也与胶体的知识有关。
2.氧化还原反应在生产、生活中具有广泛的用途。下列生产、生活中的事例不包含氧化还原反应的是
A.金属冶炼 B.点制豆腐 C.食物腐败 D.燃放鞭炮
1.伊朗核问题已引起国际社会的普遍关注,所谓浓缩铀就是提取一定浓度的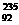 U,下列有关
U,下列有关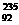 U的说法中,正确的是
U的说法中,正确的是
A.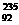 U不具有放射性 B.铀元素的相对原子质量为235
U不具有放射性 B.铀元素的相对原子质量为235
C.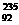 U与
U与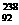 U互为同素异形体 D.
U互为同素异形体 D.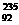 U原子核内中子数为143,核外电子数为92
U原子核内中子数为143,核外电子数为92
22、(每格2分,共6分) 已知水在25℃和95℃时,其电离平衡曲线如右图所示:
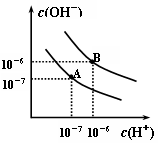 (1)则25℃时水的电离平衡曲线应为 ,(填“A”或 “B”)。
(1)则25℃时水的电离平衡曲线应为 ,(填“A”或 “B”)。
(2)25℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的 pH=7,则NaOH溶液与H2SO4溶液的体积比为____________。
(3)95℃时,若100体积pH1=a的某强酸溶液与1体积pH2 =b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH 1与强碱的pH 2之间应满足的关系是__ ___。
注意:(2)(3)必须有计算过程,否则本小题不得分。
泰兴市第二高级中学高三暑期检测
化学答题 纸
纸
|
三 |
四 |
五 |
六 |
总分 |
|
|
|
|
|
|
泰兴市第二高级中学高三暑期检测
21、(6分)碘盐是日常生活中必不可少的调味品,我国强制推广食用加碘盐。根据GB5461--《国家食用盐标准》,碘元素含量为20-50mg/kg为合格。质量监督部门为检测某品牌加碘盐是否合格,进行了如下实验:称取250g 某品牌加碘盐样品,在酸性条件下用足量KI溶液将其中IO3-全部转化成I2,生成的I2再用0.010mol/L的硫代硫酸钠溶液滴定,滴定到终点时用去12mL。
有关反应如下:
①IO3-+5I-+6 H+ 3I2+3H2O
3I2+3H2O
②I2+2S2O32- 2I-+S4O62-
2I-+S4O62-
(1)用硫代硫酸钠溶液滴定I2时,应用_________作指示剂,滴定到终点的现象是________;(每格各1分)
(2)试通过计算说明该加碘食盐是否为合格产品(写出具体的计算过程)。(4分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com