
题目列表(包括答案和解析)
21.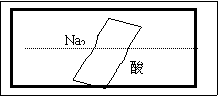 (8分)某研究性学习小组在整理实验室化学试剂时,发现一盛有无色溶液的试剂瓶,标签破损,如右图。某同学根据中学化学知识,对该试剂可能是什么物质的溶液进行了如下猜想和验证,选择你认为完全正确(包括猜想物质的化学式、检验需要的试剂、操作、现象及结论)的选项
(8分)某研究性学习小组在整理实验室化学试剂时,发现一盛有无色溶液的试剂瓶,标签破损,如右图。某同学根据中学化学知识,对该试剂可能是什么物质的溶液进行了如下猜想和验证,选择你认为完全正确(包括猜想物质的化学式、检验需要的试剂、操作、现象及结论)的选项
(多选倒扣分)。
|
序号 |
猜想物质的化学式 |
检验需要的试剂 |
操作、现象及结论 |
|
A |
Na2SO4 |
稀盐酸、氯化钡溶液 |
取少量该溶液于试管中,滴入稀盐酸,若无明显现象,再滴入氯化钡溶液,如果产生白色沉淀,则原溶液是Na2SO4。 |
|
B |
Na2CO3 |
稀盐酸、澄清的石灰水、品红溶液 |
取少量该溶液于试管中,滴入稀盐酸,如果产生的气体不能使品红溶液褪色而能使澄清的石灰水变浑浊,则原溶液是 Na2CO3。 |
|
C |
Na2SO3 |
稀盐酸、澄清的石灰水 |
取少量该溶液于试管中,滴入稀盐酸,如果产生无色气体能使澄清的石灰水变浑浊,则原溶液一定是Na2SO3。 |
|
D |
Na2SiO3 |
过量稀盐酸 |
取少量该溶液于试管中,滴入稀盐酸,产生白色胶状沉淀,盐酸过量时沉淀溶解,则原溶液是Na2SiO3溶液。 |
|
E |
Na2S2O3 |
稀盐酸 |
取少量该溶液于试管中,滴入稀盐酸,如果溶液变浑浊(或产生淡黄色沉淀),并产生无色有剌激性气味的气体,则原溶液是Na2S2O3溶液。 |
除上述五种可能之外,写出你认为还有可能物质的化学式(1种): 。22. (4分)下面是某研究性学习小组对蜡烛及其燃烧的研究报告,请你完成该实验报告:
|
探究步骤 |
实验现象 |
结论或产生这一现象的原因 |
|
①将一小块蜡烛放入水中 |
|
结论:
|
|
②燃着时 |
有明亮火焰 |
|
|
③刚吹灭时 |
|
原因: |
20.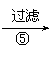
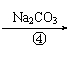
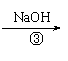
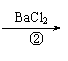
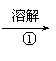 (8分)为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
(8分)为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
称取粗盐 滤液
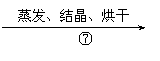

精盐
 (1)判断BaCl2已过量的方法是____________________________。
(1)判断BaCl2已过量的方法是____________________________。
(2)第④步中,相关的离子方程式是_______________________。
(3)若先用盐酸调pH值再过滤,将对实验结果产生影响,
其原因是_______________ ______________。
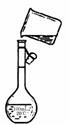
(4)为检验精盐纯度,需配制150 mL.0.2 mol/L NaCl(精盐)溶液,
右图是该同学转移溶液的示意图,图中的错误是_____________________________________________________。 100 mL容量瓶
19.NO和CO都是汽车尾气里有害物质,它们缓慢的起反应生成N2和CO2,对此反应,下列叙述正确的是
A.使用催化剂增大CO转化率 B.改变压强对反应速率无影响
C.降低压强能增大NO转化率 D.升高温度能加大反应速率
第Ⅱ卷(非选择题,共83分)
18.据权威刊物报道,1996年科学家在宇宙中发现H3分子。甲、乙、丙、丁四位学生对此报道的认识正确的是
A.甲认为上述发现绝对不可能,因为H3分子违背了共价键理论
B.乙认为宇宙中还可能存在另一种氢单质,因为氢元素有三种同位素必然有三种同素异形体
C.丙认为H3分子实质上是H2分子与H+以特殊共价键结合的产物,应写成H3+
D.丁认为如果上述的发现存在,则证明传统的价键理论有一定的局限性有待继续发展
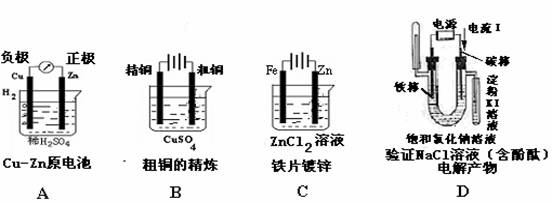
17.下图有关电化学的图示,完全正确的是( )
16.下列各组离子,在指定的环境中一定能大量共存的是
A.在c(H+)/c(OH-)=1×1012的溶液中:I-、Cl-、HCO3-、Na+
B.在能使pH试纸变红色的溶液中:Na+、S2-、NO3-、CO32-
C.在加入铝粉能产生H2的溶液中:NH4+、Fe2+、SO42-、Cl-、
D.由水电离出的c(H+)=1×10-12mol·L-1的溶液中:K+、Cl-、NO3-、Na+
15.科学家在高压下成功地将CO2转化为具有类似SiO2结构的晶体,下列关于CO2的原子晶体的说法正确的是
A.CO2的分子晶体转化为原子晶体是化学变化
B.CO2的原子晶体和分子晶体实际上是同种物质
C.CO2的原子晶体和分子晶体具有相同的物理性质
D.在CO2的原子晶体中,每一个C原子周围结合4个O原子
14.最近,中国科大的科学家们将C60分子组装在一单层分子膜表面,在-268℃时冻结分子的热振荡,并利用扫描隧道显微镜首次“拍摄”到能清楚分辨碳原子间单、双键的分子图像。下列化合物分子中一定既含单键又含双键的是
A.CO2 B.C2H4O C.COCl2 D.H2O2
13.某元素的某种含氧酸的阴离子符号是RO3-,则该元素的气态氢化物的化学式可能是
A.HR B.H2R C.RH3 D.RH4
12.盖斯定律认为:不管化学过程是一步完成或分数步完成,整个过程的总热效应相同。已知:H2O(g)=H2O (l) △H1=-Q1 kJ/mol
C2H5OH(g)=C2H5OH (l) △H2=-Q2 kJ/mol
C2H5OH (g)+3O2(g)=2CO2(g)+3H2O(g) △H3=-Q3 kJ/mol
若使23 g酒精液体完全燃烧,最后恢复到室温,则放出的热量为 (单位均为kJ)
A.Q1+Q2+Q3 B.0.5(Q1+Q2+Q3)
C.1.5Q1-1.5Q2+0.5Q3 D.1.5Q1-0.5Q2+0.5Q3
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com