
题目列表(包括答案和解析)
9.设NA表示阿伏加德罗常数,下列有关说法正确的是
A.7.8 g Na2O2含有的阴离子数目为0.2 NA
B.2.24L(标准状况)Cl2与足量NaOH溶液在常温下反应.转移的电子数为0.1NA
C.常温常压下,NA个氢分子与NA个氦分子含有的质子数相同
D.2 L 0.3mol/L的K2CO3溶液中含CO32-离子数目为0.6NA
8.有一瓶无色溶液,可能含有K+、Al3+、Mg2+、NH4+、Cl-、SO42-、HCO3-、MnO4-离子中的几种。为确定其成分,做如下实验:①取部分溶液,加入适量Na2O2固体,产生无色无味的气体和白色沉淀,再加入足量的NaOH溶液后白色沉淀部分溶解;②另取部分溶液,加入HNO3酸化的Ba(NO3)2溶液,有白色沉淀产生。下列推断正确的是
A.肯定有Al3+、Mg2+、NH4+、Cl- B.肯定有Al3+、Mg2+、SO42-
C.肯定没有K+、HCO3-、MnO4- D.肯定有Al3+、Mg2+、HCO3-
7.根据陈述的知识,类推得出的结论正确的是
A.镁条在空气中燃烧生成的氧化物是MgO,则钠在空气中燃烧生成的氧化物是Na2O
B.乙烯可使酸性高锰酸钾溶液褪色,则丙烯也可以使其褪色
C.CO2和SiO2 化学式相似,则CO2与SiO2的物理性质也相似
D.金刚石的硬度大,则C60的硬度也大
6.氮化铝(AlN)广泛应用于电子陶瓷等工业领域。在一定条件下,AlN可通过反应:
Al2O3+N2+3C 2AlN+3CO合成。下列叙述正确的是
2AlN+3CO合成。下列叙述正确的是
A.上述反应中,N2是还原剂,Al2O3是氧化剂
B.上述反应中,每生成1 mol AlN需转移3 mol电子
C.AlN中氮的化合价为+3
D.AlN的摩尔质量为41 g
5.向下列元素的氯化物的水溶液中,用长胶头滴管滴加适量的NaOH溶液,一定看不到白色沉淀的是
A.铁 B.铝 C.镁 D.铜
4.下列除去杂质的实验方法正确的是
A.除去CO中少量O2:通过灼热的Cu网后收集气体
B.除去K2CO3中少量NaHCO3:置于坩埚中加热
C. 除去N2中少量NH3,可通过水洗后收集气体
D. 可用铁粉除去FeCl3溶液中的少量的CuCl2
3.下列实验操作完全正确的是
|
编号 |
实验 |
操作 |
|
A |
钠与水反应 |
用镊子从煤油中取出金属钠,切下绿豆大小的钠,小心放入装满水的烧杯中 |
|
B |
配制一定浓度的氯化钾溶液1000mL |
准确称取氯化钾固体,放入到1000ml的容量瓶中,加水溶解,振荡摇匀,定容 |
|
C |
为确证NaHCO3固体中是否含Na2CO3 |
取少量待检固体溶于水中,滴加少量BaC12溶液,观察是否有白色沉淀生成 |
|
D |
取出分液漏斗中所需的上层液体 |
下层液体从分液漏斗下端管口放出,关闭活塞,换一个接收容器,上层液体继续从分液漏斗下端管口放出 |
2.在一定条件下,下列物质①CO2,②Cl2,③浓硝酸,④NH3,⑤FeCl3,其中能跟某些金属、非金属、酸、碱都能发生反应的是
A.①④ B.②③ C.①④⑤ D.②③⑤
1.海水是一个巨大的化学资源库,下列有关海水综合利用的说法正确的是 ( )
A.海水中含有钾元素,只需经过物理变化就可以得到钾单质
B.海水蒸发制海盐的过程中发生了化学变化
C.从海水中可得到NaCl,电解熔融NaCl可制备Cl2
D.利用潮汐发电是将化学能转化为电能
26.(15分)⑴ 下表是在1.013×105Pa下测得的几种物质的沸点:
|
结构简式 |
沸点/℃ |
结构简式 |
沸点/℃ |
|
CH3CH3 |
-88.6 |
CH2=CH2 |
-103.7 |
|
CH3CH2CH3 |
-42.2 |
CH2=CHCH3 |
-47.4 |
|
CH3CH2CH2CH3 |
-0.5 |
CH3CH2CH=CH2 |
-6.3 |
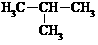 |
-11.7 |
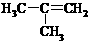 |
-6.9 |
|
CH3CH2CH2CH2CH3 |
36.1 |
CH3CH2CH2CH=CH2 |
30 |
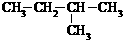 |
|
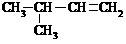 |
20.1 |
从表中数据分析,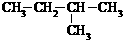 在1.013×105Pa、25℃时的状态是 (填气态、液态或固态)。
在1.013×105Pa、25℃时的状态是 (填气态、液态或固态)。
⑵ 石油裂解是一个复杂的过程,其产物为混合物。例如:
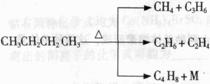
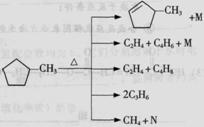
① 上述烷烃和环烷烃裂解反应中,产物M的化学式为 ,N的化学式为 。
② 下列关于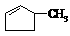 的说法正确的是 。
的说法正确的是 。
A.可用溴水区别 和
和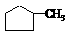
B.等质量的 和
和 完全燃烧时的耗氧量相同
完全燃烧时的耗氧量相同
C. 可与水以任意比互溶
可与水以任意比互溶
⑶ 工业上裂解反应的产物都是气态小分子烷烃和烯烃的混合物,将它们逐一分离的方法是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com