
题目列表(包括答案和解析)
2、下列各图为元素周期表的一部分,表中的数字为原子序数,其中M为37的是

1、下列关于环境问题的说法不正确的是
A、在燃煤中加入 可以减少
可以减少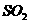 的排放
的排放
B、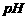 在5.6-7.0之间的降水通常称为酸雨
在5.6-7.0之间的降水通常称为酸雨
C、合成材料废弃物造成了严重的环境问题,“白色污染”即是其中最突出的例子
D、废旧电池渗出的重金属离子会造成地下水和土壤的污染
29.(衍生物)(18分)双酚-A的二甲基丙烯酸酯是一种能使人及动物的内分泌系统发生紊乱,导致生育及繁殖异常的环境激素,其结构简式为:
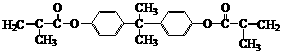
它在一定条件下水解可生成双酚-A和羧酸H两种物质。
I.(1)双酚-A的分子式为_____________;下列关于它的叙述中正确的是_________(填写字母)。
A.与苯酚互为同系物
B.可以和Na2CO3溶液反应,放出CO2气体
C.分子中最多有8个碳原子在同一平面上
D.1 mol双酚-A与浓溴水反应,最多可以消耗Br2的物质的量为4 mol
(2)下列物质中与双酚-A互为同异构体的是_________(填写字母)。
A.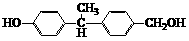 B.
B.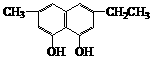
C.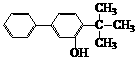 D.
D.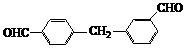
II.已知与(CH3)3COH结构相似的醇不能被氧化为醛或酸。羧酸H可以由以下途径制得(有的反应条件没有标出):

(3)C的结构简式_________________________。
(4)G中所含官能团为_________________(填名称),⑤的反应类型为______________。
(5)反应③的化学方程式为______________________________________。
(6)羧酸H与甲醇反应后得到的酯,能形成一种高分子化合物,可用于制造高级光学仪器透镜,请写出该酯在一定条件下生成此高分子化合物的化学反应方程式:
____________________________________________________。
28、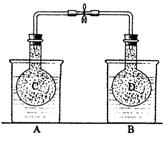 (12分)如下图所示,在25℃时,在烧杯A中装有50.0 mL水,烧杯B中装有0.50
mol/L盐酸50.0 mL,把NO2和N2O4的混和气体盛在两个连通的烧瓶C、D里,然后用夹子夹住橡皮管,把C烧瓶放人A烧杯中,D烧瓶放人B烧瓶中。
(12分)如下图所示,在25℃时,在烧杯A中装有50.0 mL水,烧杯B中装有0.50
mol/L盐酸50.0 mL,把NO2和N2O4的混和气体盛在两个连通的烧瓶C、D里,然后用夹子夹住橡皮管,把C烧瓶放人A烧杯中,D烧瓶放人B烧瓶中。
往A烧杯中加入50.0 g NH4NO3粉末搅拌使其完全溶解,
往B烧杯中加入2.0 g NaOH固体搅拌并使其溶解后。回答下列问题:
(1)烧杯A中温度(填“升高”、“降低”或“不变”)__________;
烧杯B中温度(填“升高”、“降低”或“不变”)__________。
(2)已知在NO2生成N2O4的可逆反应里,正反应是放热反应,逆反应是吸热反应:
2NO2(g) 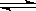 N2O4(g)
N2O4(g)
从上面实验可知C烧瓶内混和气体颜色(填“变浅”、“变深”或“不变”)______;D烧
瓶内混和气体颜色(填“变浅”、“变深”或“不变”)_______________。
(3)用pH试纸测定烧杯A中溶液的pH可知其pH(填“大于7”、“等于7”或“小于7”)_________,
导致该溶液pH这一变化的原因可用离子方程式表示如下:____________________________________.
(4)若实验测得B烧杯中酸碱中和反应放热1.4325 kJ,则NaOH溶液和HCl溶液发生中
和反应的热化学方程式为_______________________________。
(5)若起始时在D烧瓶中充入m g N2O4,此时测得烧瓶中压强为1.01×105Pa,当可逆反
应:N2O4(g) 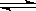 2NO2达到化学平衡状态时压强变为1.515×105Pa,则平衡混和气体
2NO2达到化学平衡状态时压强变为1.515×105Pa,则平衡混和气体
的平均相对分子质量为:______________。(精确到小数点后两位)
27、(16分)(2008·河南五市二模)(图框、电化学或碱金属)以海水中常见物质A为原料可以发展很多工业,下图中包含了中学课本中介绍的几种基本工业生产,请根据各物质之间的转化关系回答下列问题。
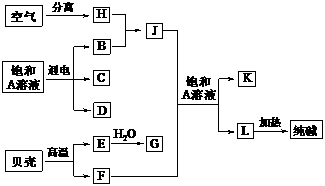
(1)C和D、C和G反应都可以制取消毒剂。写出C和D反应制取的消毒剂的离子方程式和将F和J通入A的饱和溶液中,反应的化学方程式为_______________________;
__ ________。
(2)工业上电解B溶液制得一系列化工原料,写出其电解的化学方程式,并标出电子转移的方向和数
目
。
(3)鉴定K中阳离子的实验方法和现象__________________________________;
____ ________________________。
(4)写出K电子式___ __ ____,J的空间构型为___________形
(5)L溶液的中各离子浓度由大到小的关系是________________________,
L的用途为_________________(任填两项)。
26、(15分)请按要求填空:
(1)下列实验操作或对实验事实的叙述正确的是 (填序号)(10分)
①用稀HNO3清洗做过银镜反应实验的试管;
②配制浓硫酸和浓硝酸的混合酸时,将浓硫酸沿器壁慢慢加入到浓硝酸中,并不断搅拌;
③用碱式滴定管量取20.00 mL 0.1000 mol/L KMnO4溶液;
④用托盘天平称取10.50 g干燥的NaCl固体;
⑤配制Al2(SO4)3溶液时,加入少量的稀硫酸;
⑥用瓷坩埚高温熔融Fe(CrO2)2和Na2CO3的固体混合物;
⑦向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液,以制备Fe(OH)3胶体;
⑧除去碱式滴定管尖嘴的气泡:弯曲胶管使尖嘴斜向上,挤压玻璃珠,将气泡从尖嘴赶出;
⑨银镜反应:在试管中加入AgNO3溶液,滴人氨水至沉淀溶解,加入乙醛溶液,在酒精灯上加热
⑩油脂皂化后可用渗析的方法使高级脂肪酸钠和甘油充分分离
(2)、(10分)某固体混合物可能含有MgCO3、Al2(SO4)3、Na2SO4、Ba(NO3)2、AgNO3和CuSO4。将该混合物进行如下实验,根据所给实验现象完成表格(对于能确定的物质在相应位置写化学式,暂不能确定的物质在相应位置填“无”):
(1)将少许混合物放入水中得到无色溶液和白色沉淀。
|
肯定存在的物质 |
肯定不存在的物质 |
理由 |
|
|
|
|
(2)取溶液进行焰色反应,火焰呈黄色;
|
肯定存在的物质 |
肯定不存在的物质 |
理由 |
|
|
|
|
(3)取白色沉淀加入稀盐酸,沉淀完全溶解并放出气体。
|
肯定存在的物质 |
肯定不存在的物质 |
理由 |
|
|
|
|
(4)通过上述实验仍无法确定的物质是______________。
13.一定量的铁、铝合金与300ml 2mol/L硝酸完全反应生成3.36LNO(标况)和三价铁盐、铝盐等,再向反应后的溶液中加入3mol/L的NaOH溶液,使铝、铁元素完全沉淀下来,则所加NaOH溶液的体积是( )
A、450ml B、 150ml C、200ml D、无法计算
第II卷
12.设NA为阿伏加德罗常数,下列说法正确的是( )
A.58.5 g氯化钠中约含有6.02×1023个氯化钠分子
B.含有2NA个阴离子的CaC2,在标准状况下,能产生约44.8 L的乙炔气体
C.在含4 mol Si-O键的石英晶体中,氧原子的数目为4NA
D.12.5 mL 16 mol/L浓硫酸与足量铁反应,转移电子数为0.2NA
11.(氧化还原)铀(U)常见化合价有+4价和+6价,硝酸铀酰[UO2(NO3)2]加热可发生如下反应:UO2(NO3)2 UxOy+NO2↑+O2↑(化学方程式未配平),在600 K时将气体产物集满试管,并倒扣水中,水充满试管。则上述分解反应生成的铀的氧化物化学式为( )
UxOy+NO2↑+O2↑(化学方程式未配平),在600 K时将气体产物集满试管,并倒扣水中,水充满试管。则上述分解反应生成的铀的氧化物化学式为( )
A.UO2 B.UO1·UO3 C.UO3 D.UO2·2UO3
10.已知A、B、C、D、E是核电荷数依次增大的五种短周期主族元素,原子半径按D、E、B、C、A的顺序依次减小,B和E同主族,下列推断不正确的是( )
A.A、B、D不可能在同周期
B.D一定在第二周期
C.A、D可能在同一主族
D.C和D的单质可能化合为离子化合物
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com