
题目列表(包括答案和解析)
2、下列各图为元素周期表的一部分,表中的数字为原子序数,其中M为37的是

1、下列关于环境问题的说法不正确的是
A、在燃煤中加入 可以减少
可以减少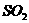 的排放
的排放
B、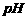 在5.6-7.0之间的降水通常称为酸雨
在5.6-7.0之间的降水通常称为酸雨
C、合成材料废弃物造成了严重的环境问题,“白色污染”即是其中最突出的例子
D、废旧电池渗出的重金属离子会造成地下水和土壤的污染
20、
 (15分)已知
(15分)已知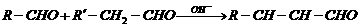 ,有机物
,有机物
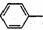
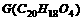 是一种酯,合成路线如下:
是一种酯,合成路线如下:
|
|||||
|
 |
||||
|


|

|
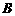


|
|


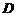 --
--
 --
--
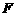 ---
---

请回答下列问题:
(1)指出反应类型:反应① ,反应②
(2)A的结构简式是:
F的结构简式是:
(3)B转化为C的化学方程式是(有机物用结构简式表示):
(4)写出有机物C的所有同时含碳碳双键、苯环和羧基的另外三种同分异构体(不包括有机物C本身):
|




19、(17分)某校学生课外活动小组的同学设计如下图所示实验装置,用来验证一氧化碳具有还原性。回答下列问题:

(1)装置B中最适宜的试剂是 ,其作用是
(2)装置C的作用是
,若实验中没有装置C,则不可以证明 具有还原性,原因是:
具有还原性,原因是:
(3)装置D中黑色固体为 ,反应的化学方程式为
(4)根据实验中的 现象,可证明CO具有还原性,有关反应的化学方程式是
(5)若要根据装置F中出现的现象确认一氧化碳具有还原性,应在上图装置
与 之间连接下图中的 装置(填序号)。

|

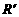
18、(12分)市场销售的某种食用精制盐包装袋上有如下说明(部分):
|
产品标准 |
 |
|
产品等级 |
一级 |
|
配料 |
食盐、碘酸钾、抗结剂 |
|
碘含量(以I计) |
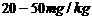 |
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式(将化学计量数填于空白处):
 +
+
 +
+ 
 +
+
 +
+ 
(2)上述反应生成的 可用四氯化碳检验。向碘的四氯化碳溶液中加入
可用四氯化碳检验。向碘的四氯化碳溶液中加入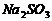 稀溶液,将
稀溶液,将 还原,以回收四氯化碳。
还原,以回收四氯化碳。
①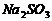 稀溶液与
稀溶液与 反应的离子方程式是
反应的离子方程式是
②某学生设计回收四氯化碳的操作步骤为:
a、将碘的四氯化碳溶液置于分液漏斗中;
b、加入适量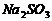 稀溶液;
稀溶液;
c、分离出下层液体。
以上设计中遗漏的操作及在上述操作中的位置是
(3)已知: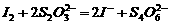
某学生测定食用精制盐的碘含量,其步骤为:
a、准确称取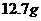 食盐,加适量蒸馏水使其完全溶解;
食盐,加适量蒸馏水使其完全溶解;
b、用稀硫酸酸化所得溶液,加入足量 溶液,使食用盐中
溶液,使食用盐中 与
与 反应完全;
反应完全;
c、以淀粉溶液为指示剂,逐滴加入物质的量浓度为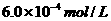 的
的 溶液
溶液 ,恰好反应完全。
,恰好反应完全。
①判断c中反应恰好完全依据的现象是
②根据以上实验和包装说明,所测精盐的碘含量是
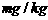
17、(16分)W、X、Y、Z是原子序数依次增大的同一短周期元素,W、X是金属元素,Y、Z是非金属元素。
(1)W、X各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为:
(2)W与Y可形成化合物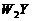 ,该化合物的电子式为
,该化合物的电子式为
(3)证明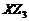 为共价化合物的方法是
为共价化合物的方法是
(4)比较Y、Z气态氢化物的稳定性: > (用分子式表示)
(5)W、X、Y、Z四种元素简单离子的离子半径由大到小的顺序是 > >
> (用离子符号表示)
(6)Z的最高价氧化物为无色液体, 该物质与一定量水混合得到一种稀酸溶液,并放出
该物质与一定量水混合得到一种稀酸溶液,并放出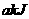 的热量。写出该反应的热化学方程式:
的热量。写出该反应的热化学方程式:
16、氧化铁和氧化铜混合物mg,加 盐酸溶液
盐酸溶液 ,恰好完全溶解,若mg的该混合物在过量氢气流中加热充分反应,冷却后剩余固体质量为
,恰好完全溶解,若mg的该混合物在过量氢气流中加热充分反应,冷却后剩余固体质量为
A、 B、
B、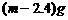
C、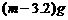 D、无法确定
D、无法确定
第II卷(非选择题 共60分)
15、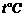 时,将
时,将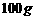 某物质A的溶液蒸发掉
某物质A的溶液蒸发掉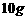 水,恢复至
水,恢复至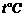 ,析出
,析出 晶体;再蒸发掉
晶体;再蒸发掉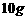 水,恢复至
水,恢复至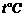 ,又析出
,又析出 晶体。下列说法中正确的是
晶体。下列说法中正确的是
A、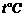 时,原溶液可能是饱和溶液
时,原溶液可能是饱和溶液
B、由于缺少条件,无法求出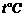 时A的溶解度
时A的溶解度
C、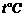 时,A的溶解度一定为75g
时,A的溶解度一定为75g
D、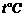 时,原溶液的质量分数为:
时,原溶液的质量分数为:
14、下列除去杂质的方法中,正确的是
A、除去铜粉中混有的铁:加足量稀硝酸,过滤
B、除去 中少量的CO:通过足量灼热的
中少量的CO:通过足量灼热的 粉末
粉末
C、除去 溶液中的少量
溶液中的少量 :加适量
:加适量 溶液,过滤
溶液,过滤
D、除去 中的少量的
中的少量的 :通过足量的饱和碳酸氢钠溶液
:通过足量的饱和碳酸氢钠溶液
13、某化学课外活动小组甲同学欲制备收集A气体,乙同学欲制备收集B气体(制备方法、装置、试剂的化学式均相同)。甲采用排水法却收集到B气体,乙用排空气法却得A气体。下列关于A、B两种气体的叙述不正确的是
A、B气体只能通过人工合成
B、A、B气体分子中均含有极性共价键
C、A、B均不属于酸酐
D、A、B气体相对分子质量之差为16
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com