
题目列表(包括答案和解析)
9、有以下七种饱和溶液①Ba(NO3)2 ②Ca(OH)2 ③Na2SiO3 ④CaCl2 ⑤Na2CO3 ⑥NaAlO2 ⑦NH3和NaCl,分别持续通入CO2,最终得到沉淀或析出晶体的是 A.③④⑥ B.①③⑥ C.③⑤⑥⑦ D.③⑥
8、某溶液中可能存在Br-、CO32-、SO32-、Al3+、I-、Mg2+、Na+等7种离子中的几种。现取该溶液进行实验,得到如下实验现象:①向溶液中滴加足量氯水后,溶液变橙色,且有无色气泡冒出;②向所得橙色溶液中加入足量BaCl2溶液,无沉淀生成;③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色。据此可以推断,该溶液中肯定不存在的离子是 A.Al3+、Mg2+、I-、SO32- B.Mg2+、Na+、CO32-、I- C.Al3+、Na+、SO32-、I- D.Al3+、CO32-、Br-、SO32-
7、化合物甲是由氟元素和氧元素形成的一种不稳定的物质,10mL甲气体可分解成15mL O2和10mL F2(气体都在同温同压下测定)。下列关于化合物甲的说法正确的是 A.该化合物的分子式为O2F2 B.其电子式可表示为F:O:O:O:F C.甲具有很强的氧化性 D.甲中氧元素的化合价为-2价
6、下列所指物质是纯净物的是 A 红磷在氯气中燃烧所得到的产物 B 从市场上购得的漂白粉 C 实验室用KMnO4固体和浓盐酸反应,从气体发生装置中导出的气体 D 氟气与氢气等物质的量混和后置于阴凉处片刻之后
5、20世纪80年代后,人们发现和证实了碳的另一类单质,它们是由一系列偶数个碳原子组成的分子,其中C60(足球烯,分子中含有30个双键)最具代表性。下图所示为n个C60连接而成的物质X。下列有关说法不正确的是
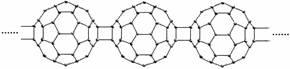
A.X难溶于水 B.一定条件下X可与H2发生加成反应
C.X是碳的一种同素异形体 D.X的摩尔质量为720n
4、已知下列物质的名称和化学式分别是:
|
名称 |
硫代硫酸钠 |
多硫化钙 |
过氧化钡 |
超氧化钾 |
|
化学式 |
Na2S2O3 |
CaSx |
BaO2 |
KO2 |
试综合上述命名规律,分析思考后回答:K2CS3应命名为:
A.三硫代碳酸钾 B.多硫碳酸钾
C.过硫碳酸钾 D.超硫碳酸钾
3、下列说法均摘自某科普杂志,你认为无科学性错误的是 ①铅笔芯的原料含重金属铅,儿童在使用时不可用嘴吮咬铅笔,以免引起铅中毒;②一氧化碳有毒,生有煤炉的居室,可放置数盆水,这样可有效地吸收一氧化碳,以防煤气中毒;③“汽水”浇灌植物有一定道理,其中二氧化碳的缓释,有利于作物的光合作用;④硅的提纯与应用,促进了半导体元件与集成芯片业的发展,可以说:“硅是信息技术革命的催化剂” A.①③ B.③④ C.①④ D.②③
2、“加碘食盐”、“高钙牛奶”、“含氟牙膏”等商品中的碘、钙、氟是指 A.原子 B.单质 C.元素 D.分子
1、每个人都应懂得防火知识,并学会火灾时如何逃走。例如,当高层楼房下层起火,火势凶猛无法扑灭时,下列逃生措施中正确的是( )
①沿楼梯迅速下楼; ②用湿毛巾堵住口鼻;
③匍匐前进,寻找安全出口; ④封闭房门;
⑤迅速转移到阳台,用绳索下坠; ⑥跳楼。
A、①②③④ B、③④⑤⑥ C、①②④⑤ D、②③④⑤
24.(12分)
将4 mol
SO3气和4 mol
NO置于2
L容器中,一定条件下发生如下可逆反应(不考虑NO2和N2O4之间的相互转化): 2SO3(g) 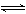 2SO2+O2 2NO+O2
2SO2+O2 2NO+O2 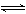 2NO2
2NO2
(1)当上述系统达到平衡时,O2和NO2的物质的量分别为n(O2)=0.1 mol、n(NO2)=3.6 mol,则此时SO3气体的物质的量为 。
(2)当上述系统达到平衡时,欲求其混合气体的平衡组成,则至少还需要知道两种气体的平衡浓度,但这两种气体不能同时是SO3和 ,或NO和 (填它们的分子式)。
(3)若在另外一个2 L的容器中只发生反应2NO+O2 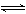 2NO2,其中NO、O2、NO2的起始浓度依次是0.2 mol/L、0.1 mol/L、0.2 mol/L,当反应达到平衡时,各物质的浓度可能是 (填字母代号)
。
2NO2,其中NO、O2、NO2的起始浓度依次是0.2 mol/L、0.1 mol/L、0.2 mol/L,当反应达到平衡时,各物质的浓度可能是 (填字母代号)
。
A、c(NO)=0.35 mol/L或c(NO)=0.09 mol/L B、c(NO2)=0.4 mol/L
C、c(NO2)=0.35 mol/L D、c(O2)=0.2 mol/L或c(NO)=0.4 mol/L
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com