
题目列表(包括答案和解析)
15.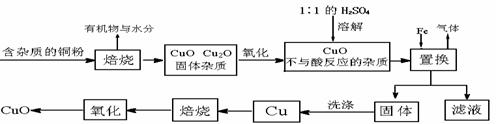 (14分)CuO在工业上有重要用途。以下是用铜粉氧化法生产CuO的流程图:
(14分)CuO在工业上有重要用途。以下是用铜粉氧化法生产CuO的流程图:
回答下列问题:
(1)写出溶解过程中的离子方程式_____________________________________。
(2)1∶1的H2SO4是用1体积98% H2SO4与1体积水混合而成。实验室中配制该硫酸溶液所需的玻璃仪器除玻璃棒外,还需要______________、________________。
(3)该工艺的置换过程中产生的气体除H2外还可能含有一定量的酸性气体,该气体是_______(写分子式),应加以回收处理。
(4)已知氧化亚铜(Cu2O)与稀H2SO4反应有CuSO4和Cu生成。假设焙烧后固体只含铜的氧化物,为检验该固体成分,下列实验设计合理的是________(选填序号)。
(a)加入稀H2SO4,若溶液呈蓝色,说明固体中一定有CuO
(b)加入稀H2SO4,若有红色沉淀物,说明固体中一定有Cu2O
(c)加入稀HNO3,若有无色气体(随即变成红棕色)产生,说明固体中有Cu2O
(d)加入稀HNO3,若全部溶解,说明固体中没有Cu2O
(5)不考虑生产中的损耗,要计算铜粉中Cu的含量,需要测定的数据是____________ __ _和________ _ __________(用文字表示)。
14、将2.7g Al与100mL 2 mol/L H2SO4溶液充分反应后,再慢慢滴入25mL
4mol/LNaOH溶液,其结果是
A.所得溶液的pH<7 B.溶液中有较多Al(OH)3沉淀
C.取少量所得溶液,加NaHCO3,无明显现象发生
D.另取少量所得溶液,加入几滴浓NaOH溶液,有白色沉淀
第Ⅱ卷(非选择题 共72分)
13、已知在pH值为4左右的环境中,Cu2+、Fe2+几乎不水解,而Fe3+几乎完全水解。工业上制CuCl2是将浓盐酸用蒸气加热到80℃左右,再慢慢加入粗氧化铜(含少量杂质FeO),充分搅拌使之溶解。欲除去溶液中的杂质离子,下述方法中可行的是( )
A.加入纯Cu将Fe2+还原为Fe
B.向溶液中通入H2S使Fe2+沉淀
C.向溶液中通入Cl2,再通入NH3,调节pH值为4左右
D.向溶液中通入Cl2,再加入纯净的CuO粉末调节pH值为4左右
11、R2O8n-离子在一定条件下可以把Mn2+离子氧化为MnO4-,若反应后R2O8n-离子变为RO42-离子,又知反应中氧化剂与还原剂的物质的量之比为5:2,则n的值是:
A.1 B.2 C.3 D.4
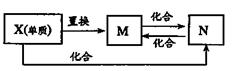 12、右图中,M、N为含X元素的常见化合物。则X元素可能为
12、右图中,M、N为含X元素的常见化合物。则X元素可能为
A.Fe B.Cu
C.N D.C
10、Na2FeO4是一种高效多功能水处理剂,应用前景广阔。一种制备Na2FeO4的方法可用化学方程式表示如下:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,对此反应下列说法中不正确的是( )
A.Na2O2在反应中只作氧化剂
B.O2是氧化产物
C.Na2FeO4既是氧化产物又是还原产物
D.2mol FeSO4发生反应时,共有8mol电子转移
题意。错选、多选不给分,若有两个答案只选一个且正确给2分)
9、下列离子方程式不正确的是 ( )
A.NaHSO4溶液中滴入Ba(OH)2溶液至中性:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O
B.向氯化铝溶液中加入过量氨水:Al3++3NH3·H2O==Al(OH)3↓+3NH4+
C.Ca(HCO3)2溶液中加入过量KOH溶液:Ca2+ + HCO3-+OH-==CaCO3↓+ H2O
D.Fe(OH)3溶于过量的HI溶液:2Fe(OH)3+6H++2I-=2Fe2++I2+6H2O
8、将一定量Fe和Fe2O3的混合物放入2mol/L的HNO3溶液25mL中,反应完全后,无固体剩余,生成224mL NO气体(标准状况),再向反应后的溶液中加入1mol/L的NaOH溶液,要使铁元素全部沉淀下来,所加NaOH溶液的体积最少是
A.40mL B.45mL C.50mL D.无法确定
7、世界著名的科技史专家、英国剑桥大学的李约瑟博士考证说:“中国至少在距今3000年以前,就已经使用玻璃了。”下列有关玻璃的说法不正确的是
A.制普通玻璃的原料主要是纯碱、石灰石和石英
B.玻璃在加热熔化时有固定的熔点
C.普通玻璃的成分主要是硅酸钠、硅酸钙和二氧化硅
D.盛放烧碱溶液的试剂瓶不能用玻璃塞,是为了防止烧碱跟二氧化硅生成硅酸钠而使瓶塞与瓶口粘在一起
6、下列各组离子在溶液中能大量共存,当溶液呈强酸性时,有气体产生;而当溶液呈强碱性时,又能生成沉淀。该组离子可能是 ( )
A.Na+、Cu2+、NO3一、CO32一 B.NH4+、K+、Cl一、HCO3一
C.Mg2+、NH4+、SO42一、Cl一 D.Fe2+、Na+、SO42一、NO3一
5、下列实验操作完全正确的是
|
编号 |
实验 |
操作 |
|
A |
钠与水反应 |
用镊子从煤油中取出金属钠,切下绿豆大小的钠,小心放入装满水的烧杯中 |
|
B |
配制一定浓度的氯化钾溶液1000mL |
准确称取氯化钾固体,放入到1000ml的容量瓶中,加水溶解,振荡摇匀,定容 |
|
C |
为确证NaHCO3固体中是否含Na2CO3 |
取少量待检固体溶于水中,滴加少量BaC12溶液,观察是否有白色沉淀生成 |
|
D |
取出分液漏斗中所需的上层液体 |
下层液体从分液漏斗下端管口放出,关闭活塞,换一个接收容器,上层液体继续从分液漏斗下端管口放出 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com