
题目列表(包括答案和解析)
15. 下列比较中,可能正确的是
A.同温度同物质的量浓度时,HF比HCN易电离,则NaF溶液的 pH 比 NaCN 溶液大
B.0.2 mol•L-l NH4Cl 和 0.l mol•L-l NaOH 溶液等体积混合后:
c(NH4+) > c (Cl―) > c (Na+) > c (OH-) >c (H+)
C.物质的量浓度相等的 H2S 和 NaHS 混合溶液中:
c (Na+) +c(H+) = c (S2―) +c (HS―)+c (OH―)
D.相同物质的量浓度的下列溶液中,①NH4Al(SO4)2、②NH4Cl、③CH3COONH4、④NH3·H2O;
c(NH4+) 由大到小的顺序是:①>②>③>④
14.可逆反应a A(s)+b B(g) c C(g)+d
D(g),反应过程中,当其它条件不
c C(g)+d
D(g),反应过程中,当其它条件不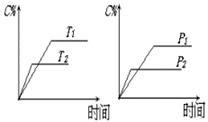 变时,C的百分含量(C%)与温度(T)和压强(P)的关系如右图,下列叙述正确的是
变时,C的百分含量(C%)与温度(T)和压强(P)的关系如右图,下列叙述正确的是
A、达到平衡后,加入催化剂则C%增大
B、达到平衡后,若升高温度,平衡向左移动
C、化学方程式中b >c +d
D、达平衡后,增加A的量,有利于平衡向右移动
13.铜的冶炼大致可分为:(1)富集:将硫化物矿进行浮选; (2)焙烧:主要反应为:2CuFeS2 +4O2 = Cu2S+3SO2 +2FeO(炉渣); (3)制粗铜:在1200℃发生的主要反应为:2Cu2S +3O2 = 2Cu2O +2SO2;2Cu2O + Cu2S =6Cu +SO2↑; (4)电解精炼。 下列说法正确的是
A.上述灼烧过程的尾气均可直接排入到空气中
B.由6mol CuFeS2 生成6molCu,上述共消耗15molO2
C.在反应2Cu2O + Cu2S =6Cu +SO2↑中,作氧化剂的只有Cu2O
D.电解精炼时,粗铜应与外电源负极相连
12.下列离子方程式正确的是
A. 把少量SO2通入Ca(ClO)2溶液中:
SO2+H2O +Ca2++ 2ClO- = 2HClO +CaSO3 ↓
B. 向NaHSO4溶液中逐滴加入Ba(OH)2溶液至溶液呈中性
2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O
C.Ca(HCO3)2溶液中加入足量的Ba(OH)2溶液:
Ca2++2HCO3-+2OH-==CaCO3↓+CO32-+2H2O
D.过量的Cl2通入FeBr2的溶液中:2Fe2++4Br-+3Cl2==2Fe3++6Cl-+2Br2
11.下列说法中,不正确的是
A. 用惰性电极电解CuSO4溶液(足量)过程中,溶液的颜色逐渐变浅,pH逐渐增大
B. 在正常情况下,人体血液的pH应保持弱碱性范围,为了维持人体细胞内的酸碱平衡,人需要选择不同的酸性食物或碱性食物来加以控制。
C. 在由水电离出的c(OH-)=1×10-12mol·L-1的溶液中,Al3+不可能大量存在
D. 室温下pH=6的酸性溶液中,可能存在NH3·H2O分子
10.用NA表示阿伏加德罗常数,下列说法正确的是
A.18g D2O含有的电子数为10NA
B.同温、同压下,相同体积的氧气和氩气所含的原子数相等
C.标准状况下,11.2L以任意比例混合的氮气和氧气所含的原子数为NA
D.1mol Na2O2与水完全反应时转移电子数为2NA
9. 某研究性学习小组,为研究光化学烟雾消长规律,在一烟雾实验箱中,测得烟雾的主要成分为RH(烃)、NO、NO2、O3、PAN(CH3COOONO2),各种物质的相对浓度随时间的消失,记录于右图,根据图中数据,下列推论最不合理的是
某研究性学习小组,为研究光化学烟雾消长规律,在一烟雾实验箱中,测得烟雾的主要成分为RH(烃)、NO、NO2、O3、PAN(CH3COOONO2),各种物质的相对浓度随时间的消失,记录于右图,根据图中数据,下列推论最不合理的是
A.NO的消失的速率比RH快
B.NO转化为NO2
C.RH和NO2转化为PAN和O3
D.O3转化为PAN
8.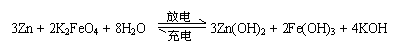 高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电
电压。高铁电池的总反应为
下列叙述不正确的是
A.放电时每转移3 mol电子,正极有1mol K2FeO4被氧化
B.充电时阳极反应为:Fe(OH)3 -3e- + 5 OH- = FeO + 4H2O
+ 4H2O
C.放电时负极反应为:Zn-2e- +2OH-= Zn(OH)2
D.放电时正极附近溶液的碱性增强
7.以下物质的制备原理错误的是( )
A. 无水氯化镁的制备 :MgCl2·6H2O MgCl2+ 6H2O
MgCl2+ 6H2O
B. 铝的制备:2Al 2O3(熔融)
 4Al+3O2↑
4Al+3O2↑
C. 烧碱的制备:2NaCl+2H2O 2NaOH +H2↑+ Cl2↑
2NaOH +H2↑+ Cl2↑
D. 漂白粉的制备: 2Ca(OH)2+ 2Cl2 = Ca(ClO)2 +CaCl2+2H2O
6.类推的思维方法在化学学习与研究中常会产生错误的结论,因此类推的结论最终要经过实践的检验才能确定其正确与否。下列几种类推结论中正确的是
A.由2Cu + O2 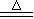 2CuO,可推出Cu + S
2CuO,可推出Cu + S 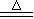 CuS
CuS
B.相同温度下,CaCO3的溶解度比Ca(HCO3)2的溶解度小,则Na2CO3的溶解度也小于
NaHCO3的溶解度
C.由氢化物的稳定性H2O>NH3,推测氢化物的稳定性也是H2S>PH3
D.CO2与Na2O2反应生成Na2CO3和O2,故SO2与Na2O2反应生成Na2SO3和O2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com