
题目列表(包括答案和解析)
1.在浓盐酸中H3AsO3与SnCl2反应的离子方程式为:
3SnCl2+12Cl-+2H3AsO3+6H+=2As+3SnCl62-+6M。关于该反应的说法中正确的组合是
① 氧化剂是H3AsO3;② 还原性:Cl->As;③ 每生成7.5gAs,还原剂失去的电子为0.3 mol;④ M为OH-;⑤ SnCl62-是氧化产物。
A.①③⑤ B.①②④⑤ C.①②③④ D.只有①③
22、(10分)钠是活泼金属,受热后与氧气剧烈反应,发出黄色火焰,生成一种淡黄色固体-过氧化钠。课本在生成物过氧化钠旁注明,指的“是反应的主要产物,由于空气中还有其它成分,因此可能还有一些同时发生的其它反应”。某校化学兴趣小组同学据此进行了有关探究。
[猜想]钠在空气中燃烧,生成过氧化钠、氧化钠,还有氮化钠。
[查阅资料]氮化钠与水反应能生成氢氧化钠和氨气。
[实验]①取11.5 g钠单质放在一块薄铁皮上,上扣一玻璃罩(玻璃罩内为干燥且无酸性气体的空气),用酒精灯加热薄铁皮,钠燃烧;
②将燃烧产物投入水中,得到0.224 L(折算成标准状态)气体和1000 mL溶液;
③经检验,该气体为纯净的氧气;
④从1000 mL溶液中取出25.00mL溶液,滴加2滴酚酞试液,加入1.00 mol·L-1HCl溶液至13.50 mL时恰好红色褪去。
[结论](1)通过计算确定钠的燃烧产物中是否含有氮化钠。
(2)计算钠在空气中燃烧产物中各成分的物质的量之比。
21、(12分)已知单质铁溶于-定浓度的硝酸溶液中反应的离子方程式为:
aFe+bNO3-+cH+=dFe2++fFe3++gNO↑+hN2O↑+kH2O(化学计量数a-k均为正整数)。
回答下列问题:
(1)根据反应中氮、氢、氧三种元素的原子个数守恒,可得c、g、h的关系式是(用-个代数式表示。下同) 。
(2)根据反应中离子的电荷守恒,可得b、c、d、f的关系式是 。
(3)根据反应中电子转移的总数相等,可得d、f、g、h的关系式是 。
(4)若a=12,且铁和稀硝酸恰好完全反应,则b的取值范围是 ;c的取值范围是 。
20、(10分)100mL某无色透明溶液中可能含有Fe3+、Ag+、Al3+、Ba2+、Mg2+、K+、Na+等阳离子。进行下述实验(所加试剂均过量)
(1)根据下图推断:溶液中一定存在的阳离子除Al3+和Mg2+外还有 ;溶液中一定还大量存在阴离子,则其可能是 ;
(2)反应①、②的离子方程式分别为:
① 、 ;
② ;
(3)若实验中测得白色沉淀C和固体F的质量分别为13.6g和5.1g,则原溶液中Mg2+离子的物质的量浓度为 。

19、(10分)三氟化氮(NF3)是一种新型电子材料,它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有: HF、 NO 和 HNO3 ,请根据要求回答下列问题:
(1)反应过程中,被氧化与被还原的元素的物质的量之比为_______________。
(2)写出该反应的化学方程式,并标出电子转移的方向和数目:
______________________________________________________________________。
若反应中生成0.2 mol HNO3,转移的电子数目为______________________个。
(3)NF3是一种无色、无臭的气体,但一旦NF3在空气中泄漏,还是易于发现。你判断该气体泄漏时的现象是 。
(4)一旦NF3泄漏,可以用NaOH溶液喷淋的方法减少污染,其产物除NaNO2、NaF、H2O外。还肯定有______ ______(填化学式)。
18、(12分)铁是人体必须的微量元素,治疗缺铁性贫血的常见方法是服用补铁药物。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。
某同学为了检测“速力菲”药片中Fe2+的存在,设计并进行了如下实验:
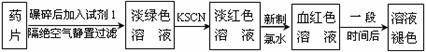
(1) 试剂1是 ,加入新制氯水后溶液中发生的离子反应方程式是:
, ;
(2) 加入KSCN溶液后,在未加新制氯水的情况下,溶液中也产生了红色,其可能的原因是 ;
(3) 在实验中发现放置一段时间,溶液的颜色会逐渐褪去。为了进一步探究溶液褪色的原因,甲、乙、丙三位同学首先进行了猜想:
|
编号 |
猜
想 |
|
甲 |
溶液中的+3价Fe又被还原为+2价Fe |
|
乙 |
溶液中的SCN-被过量的氯水氧化 |
|
丙 |
新制的氯水具有漂白性,将该溶液漂白 |
基于乙同学的猜想,请设计实验方案,验证乙同学的猜想是否正确。写出有关的实验操作、预期现象和结论。(不一定填满,也可以补充)
|
编号 |
实验操作 |
预期现象和结论 |
|
① |
|
|
|
|
|
|
|
|
|
|
17、(10分)科学家预测“氢能”将是未来最理想的新能源。请回答下列问题:
(1)实验测得,1克氢气燃烧生成液态水放出142.9 kJ热量,则表示氢气燃烧热的热化学方程式为 。
A.2H2(g) + O2(g) = 2H2O(l); △H =-142.9 kJ/mol
B.H2(g) + 1/2O2(g) = H2O(l); △H =-285.8 kJ/mol
C.2H2(g) + O2(g) = 2H2O(l);△H =-571.6 kJ/mol
D.H2(g) + 1/2O2(g) = H2O(g);△H = -285.8 kJ/mol
(2)根据“绿色化学”的思想,为了制备H2,某化学家设计了下列化学反应步骤:
①CaBr2+H2O CaO+2HBr ②2HBr+Hg
CaO+2HBr ②2HBr+Hg HgBr2+H2↑
HgBr2+H2↑
③HgBr2+CaO HgO+CaBr2 ④2HgO
HgO+CaBr2 ④2HgO 2Hg+O2↑
2Hg+O2↑
上述过程的总反应可表示为 。
(3)利用核能把水分解,制出氢气,是目前许多国家正在研究的课题。下图是国外正在研究中的一种流程(硫-碘热循环法),其中用了过量的碘。

请写出反应①的化学方程式: 。
用硫-碘热循环法制取氢最大的优点是 。
(4)也有人认为利用氢气作为能源不太现实。你的观点呢?请说明能够支持你的观点的两点理由
。
16.同位素示踪法可用于反应机理的研究,下列反应或转化中同位素示踪表示正确的
是( )
A.2Na218O2 + 2H2O = 4Nal8OH + O2↑
B.2KMnO4 + 5H218O2 + 3H2SO4 = K2SO4 + 2MnSO4 + 518O2↑+ 8H2O
C.NH4Cl + 2H2O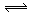 NH3·2H2O + HCl
NH3·2H2O + HCl
D.K37ClO3 + 6HCl = K37Cl + 3Cl2↑+ 3H2O
选择题答案表:
第Ⅱ卷(共64分)
15.下列反应的离子方程式正确的是( )
A.少量二氧化硫气体通入到漂白粉溶液中;Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO
B.向Fe(OH)3中加入氢碘酸:Fe(OH)3+3H+ =Fe3++3H2O
C.等物质的量浓度、等体积的NH4HCO3溶液与NaOH溶液相混合:
NH4+ + HCO3- + 2OH- = NH3·H2O + CO32- +H2O
D.向硫酸氢钠溶液中滴入氢氧化钡溶液至pH=7
Ba2++2OH-+2H++SO42- =BaSO4↓+2H2O
14.高铁酸钾 (K2FeO4)是一种新型、高效、多功能水处理剂,是比Cl2、O3、ClO2、KMnO4氧化更强,无二次污染的绿色水处理剂。工业是先制得高铁酸钠,然后在低温下,在高铁酸钠溶液中加入KOH至饱和就可析出高铁酸钾(K2FeO4)。湿法制备的主要反应方程为:2Fe(OH)3 +3ClO -+4OH- =2FeO42- +2Cl- +5H2O ,干法制备的主要反应方程为:2FeSO4 +6Na2O2 = 2Na2FeO4 +2Na2O +2Na2SO4 +O2↑下列有关说法不正确的是( )
 A.高铁酸钾中铁显+3价
A.高铁酸钾中铁显+3价
B.湿法中每生成1mol Na2FeO4 转移3mol电子
C.干法中每生成1mol Na2FeO4 转移4mol电子
D.K2FeO4处理水时,不仅能消毒杀菌,还能除去水体中的H2S、NH3等,生成的Fe(OH)3还能吸附水中的悬浮杂质
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com