
题目列表(包括答案和解析)
9.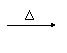 下述有机物的变化中,属于消去反应的是 ( )
下述有机物的变化中,属于消去反应的是 ( )
A.CH3CH2CH2OH +CuO CH3CH2CHO +H2O + Cu
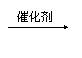
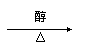 B.CH3-C≡CH+HCl
CH3CCl==CH2
B.CH3-C≡CH+HCl
CH3CCl==CH2
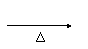
C.CH3CH2CH2Cl+NaOH CH3CH==CH2+NaCl+H2O
 |
|||
|
|||
D.CH3CH2CH2Cl+NaOH CH3CH2CH2OH+NaCl
8.大气污染物氟里昂-12的化学式是CF2Cl2,下面关于氟里昂-12的说法正确的是( )
A.没有固定的熔沸点 B.分子中的碳原子是不饱和的
C.属于正四面体的空间结构 D.只有一种结构
7.能说明苯分子的平面正六边形的结构中,碳碳键不是单、双键交替的事实是
A.苯的一元取代物无同分异构体 B.苯的邻位二元取代物只有一种
C.苯的间位二元取代物只有一种 D.苯的对位二元取代物只有一种
6.与氢气完全加成后,不可能生成2,2,3-三甲基戊烷的烃是
A.(CH3)3 C-CH=CH2 B.CH2==C(CH2CH3)C (CH3)3
C.HC≡CCH(CH3)C(CH3)3 D.(CH3)3CC(CH3)==CHCH3
5.甲烷中的碳原子是sp3杂化,下列用*表示碳原子的杂化和甲烷中的碳原子杂化状态相同的是 ( )
A.CH2=CHC*H2CH3 B.C*H2=CHCH3
C.CH2=C*HCH3 D.CH2=C*H2
4.下列分子中,含有极性共价键且呈正四面体结构的是 ( )
A.氨气 B.二氯甲烷 C.四氯甲烷 D.白磷
3.键线式可以简明扼要的表示碳氢化合物,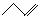 种键线式物质是
( )
种键线式物质是
( )
A.丁烷 B.丙烷 C.1-丁烯 D.丙烯
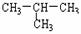 1.下列物质属于同分异构体的一组是
1.下列物质属于同分异构体的一组是
A.CH4与C2H4 B. 与 CH3-CH2-CH2-CH3
C.C2H6与C3H8 D. O2与O3
2.下列物质分子的电子式正确的是 ( )
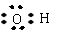
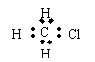
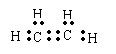 A.CH3Cl
B.羟基
A.CH3Cl
B.羟基
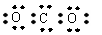
C.CO2 D.C2H4
23.(13 分 )
金属 (M) 的腐蚀是因为发生反应: M-ne-→Mn+。金属腐蚀造成很大的经济损失,甚至超过自然灾害,其中钢铁锈蚀最为严重,寻求防止钢铁腐蚀的方法意义重大。
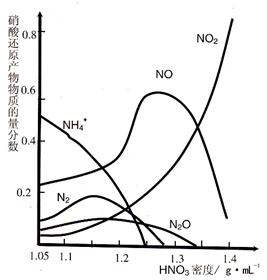 一种钢铁防腐的方法是将钢铁放在冷的浓硝酸中浸泡。但是加热或在稀 HNO3中,铁与硝酸会不断反应。不同浓度的 HNO3 与铁反应的还原产物很复杂,其分布曲线如图。
一种钢铁防腐的方法是将钢铁放在冷的浓硝酸中浸泡。但是加热或在稀 HNO3中,铁与硝酸会不断反应。不同浓度的 HNO3 与铁反应的还原产物很复杂,其分布曲线如图。
(1) 钢铁在冷的浓硝酸中浸泡能防腐的原因是:
。
(2)工业上一般不用冷浓硝酸进行铁表面处理,其可能的原因是:
。
(3)由图示可知,密度等于1.35 g·mL-1的硝酸与铁反应时,其还原产物主要是 ;足量的铁与一定量的浓硝酸反应时,反应过程中可能的气体产物有 ;还原产物中NH4+的物质的量分数随 而增大;请用一句话概括该图反映出的基本结论: 。
(4)m mol 铁与极大量的密度为1.35 g·mL-1的硝酸溶液完全反应放出n L气体(体积在标准状况下测定),此时溶液中Fe元素的存在方式是 , n 的值最接近 (填字母编号)。
A.22.4m B.33.6m C.44.8m D.67.2m
(5)除了上述处理的方法外,下列方法也能起到防腐作用的是 (填字母编号)
A.在铁中掺入铬、镍等金属,改变其内部结构,制成不锈钢
B.在铁制品表面镀锌
C.提高铁中含碳量,制成生铁
D.将水库铁闸门与直流电源的负极相连
22.(10分)
重晶石(BaSO4)难溶于水,要转化成BaCO3再制备其他钡盐。工业上一般采用高温煅烧还原法;实验室可以采用沉淀转化法。
●高温煅烧还原法
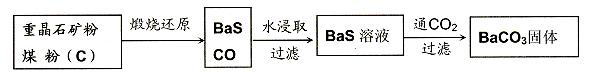
(1)煅烧还原的热化学方程式为:
有关的数据:Ba(s)+S(s)+2O2(g)=BaSO4(s);△H= -1473.2 kJ·mol-1
C(s)+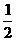 O2(g)=CO(g);△H= -110.5 kJ·mol-1
O2(g)=CO(g);△H= -110.5 kJ·mol-1
Ba(s)+S(s)=BaS(s);△H= -460kJ·mol-1
(2)经检验BaS的水溶液呈碱性,原因是(用离子方程式表示)
●沉淀转化法
向BaSO4沉淀中加入饱和Na2CO3溶液时,会有如下转化:
BaSO4(s)+CO32―(aq) BaCO3(s)+SO42―(aq)(平衡常数K=0.042)。
BaCO3(s)+SO42―(aq)(平衡常数K=0.042)。
BaSO4沉淀转化为BaCO3沉淀的做法是把BaSO4置于一定量的饱和Na2CO3溶液中浸泡,再充分搅拌,弃去上层清液;如此处理多次,可使BaSO4全部转化为BaCO3。
(3)向足量BaSO4沉淀中加入一定量 c mol/L Na2CO3溶液,充分搅拌后溶液中SO42―的浓度是多少?(写出计算过程,结果用含c的代数式表示)
(4)现有0.40 mol BaSO4,欲使之全部转化为BaCO3。若每次用1.00 L 2.0 mol·L-1饱和Na2CO3溶液处理,至少需要处理 次。
(5)从“绿色化学”角度分析,用饱和Na2CO3溶液沉淀转化法的优点是
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com