
题目列表(包括答案和解析)
21.电瓶车所用电池一般为铅蓄电池,是一种典型的可充电
电池,如右图所示。电池总反应式为: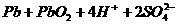
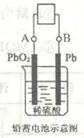

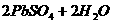 ,则下列说法正确的是
,则下列说法正确的是
A.放电时:电流方向由B到A
B.放电时;正极反应是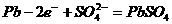
C.充电时:铅蓄电池的负极应与充电器电源的正极相连
D.充电时:阳极反应是
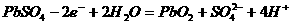
20.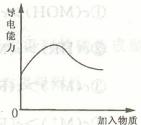 下列实验结果符合右边图像所示关系的是
下列实验结果符合右边图像所示关系的是
A.将CO2通入KAlO2溶液
B.H2O2溶液中加入少量MnO2
C.向浓的CH3COOH溶液中不断加水
D.将氨气通人醋酸溶液中
19.根据相关化学原理,下列推断正确的是
A.若弱酸HA的酸性强于弱酸HB,则同浓度钠盐溶液的pH:NaA<NaB
B.若x原子的质子数为a,中子数为b,则X的质量数为:a-b
C.若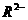 离子和
离子和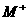 离子的电子层结构相同,则
离子的电子层结构相同,则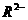 和
和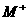 的化学性质相同
的化学性质相同
D.若有反应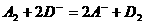 ,则氧化性:D2>A2
,则氧化性:D2>A2
18.下图是红磷P(s)和Cl2 (g)发生反应生成PCl3 (g)和PCl5 (g)的反应过程和能量关
系图。
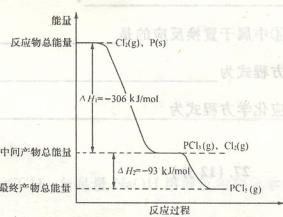
其中PCl5(g)分解成PCl3(g)和C12的反应是一个可逆反应。温度t℃时,在密闭
容器中加入0.6 mo1 PCl5,达平衡时PCl5还剩0.45 mol,其分解率为a。则下列推断
不正确的是
A.a等于25%
B.若升高温度,平衡时PCl5的分解率小于a
C.若起始时加入0.6mol PCl3和0.6 mol Cl2,以相同的条件进行反应,则平
衡时PCl3转化率为3a
D.其他条件不变,增大压强,PCl5的转化率小于a
17.下列各项操作中,不发生“先产生沉淀,然后沉淀又溶解”现象的是:①向饱和
碳酸钠溶液中通入过量的CO2 ②向Fe(OH)3胶体中逐滴加入过量的稀硫酸 ③
向AgNO3溶液中逐滴加入过量氨水 ④向硅酸钠溶液中逐滴加入过量的盐酸
A.①② B.①③ C.①④ D.②③
16.下列说法不正确的是
A.100℃时,纯水中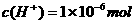 ·
·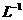 ,pH小于7,此时纯水显酸性
,pH小于7,此时纯水显酸性
B.pH=12的烧碱和氢氧化钡溶液,二者物质的量浓度之比为2:l
C.pH=3的盐酸与pH=5的硫酸等体积混合,pH=3.3
D.0. 1 mol·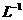 CH3COOH溶液中,c(CH3COOH)>c(CH3CO
CH3COOH溶液中,c(CH3COOH)>c(CH3CO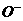 )
)
15.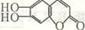 中草药秦皮中含有的七叶树内酯,具有抗菌作用。有关七
中草药秦皮中含有的七叶树内酯,具有抗菌作用。有关七
叶树内酯的下列说法正确的是
A.化学式为C10H6O4 B.加入浓溴水后有白色沉淀生成
C.只能发生取代反应 D.可与NaOH溶液反应,且1 mol该物质消耗2 mol NaOH
14.下列说法正确的是
A.冰、水和水蒸气中都存在氢键
B.除稀有气体外的非金属元素都能生成不同价态的含氧酸
C.若ⅡA某元素的原子序数为m,则同周期IIIA元素的原子序数有可能为m+11
D.干冰升华时分子内共价键会发生断裂
12.下列实验方案可行的是
A.鉴别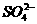 加入BaCl2溶液,再加稀盐酸,观察沉淀是否消失
加入BaCl2溶液,再加稀盐酸,观察沉淀是否消失
B.证明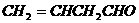 中一定有碳碳不饱和键:滴人KMnO4酸性溶
中一定有碳碳不饱和键:滴人KMnO4酸性溶
液,看紫红色是否褪去
C.量取14.80mLlmol·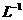 NaOH溶液:选用25mL碱式滴定管
NaOH溶液:选用25mL碱式滴定管
D.检验溶液中一定有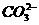 加入稀盐酸,将产生的气体通人澄清石灰水
加入稀盐酸,将产生的气体通人澄清石灰水
 13.用高铁酸钠(Na2FeO4)对河湖水消毒是城市饮水处理的新技术。已知反应:
13.用高铁酸钠(Na2FeO4)对河湖水消毒是城市饮水处理的新技术。已知反应:
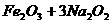
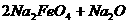 下列说法正确的是
下列说法正确的是
A.Na2O2既是氧化剂又是还原剂
B.在Na2FeO4中Fe为+4价,具有强氧化性。能消毒杀菌
C.3 mol Na2O2发生反应,有12 mol电子转移
D. Na2FeO4既是氧化产物又是还原产物
11.下列离子方程式正确的是
A.向100 mL 3 mol·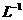 FeBr2溶液中通入标准状况下4.48 L C12
FeBr2溶液中通入标准状况下4.48 L C12
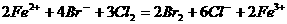
B.硫酸铜溶液中加入硫化钠溶液: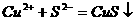
 C.碳酸氢铵溶液中加入足量氢氧化钠:
C.碳酸氢铵溶液中加入足量氢氧化钠: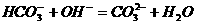
D.以石墨为电极电解MgCl2溶液: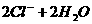
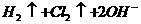
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com