
题目列表(包括答案和解析)
(二)实验探究
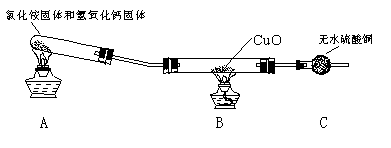 该小组成员设计实验探究氨气还原性及其产物,实验装置(夹持及尾气处理装置未画出)图如下:
该小组成员设计实验探究氨气还原性及其产物,实验装置(夹持及尾气处理装置未画出)图如下:
(1)该装置在设计上有一定的缺陷,为确保实验结果的准确性,你对该装置的改进措施是 。
(2)利用改进后的装置进行实验,观察到CuO变为红色物质,无水CuSO4变蓝,同时生成一种无污染的气体。请写出NH3与CuO反应的化学方程式
(一)制取氨气
(1)实验室常用加热氯化铵固体和氢氧化钙固体的混合物来制取氨气,写出反应的化学方程式 。
(2)实验室还可在 (填一种试剂)中滴加浓氨水的方法快速制取少量氨气。
15.(14分)某校化学研究性学习小组的同学在学习了氨的性质后讨论:运用类比的思想,既然氨气具有还原性,能否象H2那样还原CuO呢?他们设计实验制取氨气并探究上述问题。请你参与该小组的活动并完成下列研究:
14.把一定量的锌与100 mL 18.5 mol/L的浓硫酸充分反应后,锌完全溶解,同时生成气体Y 33.6L(在标准状况下.)。将反应后的溶液稀释到1 L,测得溶液的pH=1,则下列叙述正确的是( )
A.气体Y是SO2和H2的混合物 B.气体Y中SO2和H2的体积比为4:1
C.反应中共消耗锌87.5g D.反应中共转移电子3 mol
第Ⅱ卷(非选择题 共72分)
13.固体A的化学式为NH5,它的所有原子的最外层都符合相应稀有气体原子的最外电子层结构,则下列有关说法中,不正确的是( )
A.NH5中既有离子键又有共价键
B.NH5的熔沸点高于NH3
C.1 molNH5中含有5 mol N-H键
D.NH5固体投入少量水中,可产生两种气体
12.钢铁“发蓝”是将钢铁制品浸到某些氧化性的溶液中,在钢铁的表面形成一层四氧化三铁的技术过程。其中一种办法是将钢铁制品浸到亚硝酸钠和浓氢氧化钠的混合溶液中加热到130℃反应。其过程可以用如下化学方程式表示:
① 3Fe+NaNO2+5NaOH = 3Na2FeO2+H2O+NH3↑;
② 6Na2FeO2+NaNO2+5H2O = 3 Na2Fe2O4+ NH3↑+7NaOH;
③ Na2FeO2+ Na2Fe2O4+2H2O = Fe3O4+4NaOH;
下列说法不正确的是( )
A.该生产过程会产生污染 B.反应②中的氧化剂是NaNO2
C.反应①②③均是氧化还原反应
D.整个反应过程中每有16.8gFe参加反应转移0.8mol电子
11.美国“海狼”潜艇上的核反应堆内使用了液体铝钠合金(单质钠和单质铝熔合而成)作载热介质,有关说法不正确的是( )
A.原子半径:Na<Al
B.铝钠合金若投入一定的水中可得无色溶液,则n(Al)≤n(Na)
C.铝钠合金投入到足量氯化铜溶液中,肯定有氢氧化铜沉淀也可能有铜析出
D.m g不同组成的铝钠合金投入足量盐酸中,若放出的H2越多,则铝的质量分数越小
10. 奥运会会标是五环旗,假定奥运五环旗中的每一环表示一种物质,
奥运会会标是五环旗,假定奥运五环旗中的每一环表示一种物质,
相连环物质间一定条件下能发生常见反应,不相连环物质间不能
发生反应。且四种反应中必须包含化合反应、置换反应及复分解
反应,适合的一组是( )
|
选项 |
蓝 |
黑 |
红 |
黄 |
绿 |
|
A |
SiO2 |
CuSO4溶液 |
O2 |
NaOH溶液 |
Ag |
|
B |
O2 |
稀H2SO4 |
CO2 |
Fe |
NaOH溶液 |
|
C |
O2 |
稀H2SO4 |
Al(OH)3 |
NH3 |
NaOH |
|
D |
Mg |
CO2 |
KOH溶液 |
Al |
Fe2O3 |
9.下列离子方程式书写正确的是( )
A.石灰乳与Na2CO3溶液混合:Ca2++CO32-=CaCO3↓
B.NH4HSO3溶液与足量的NaOH溶液混合加热:
NH4++HSO3-+2OH- NH3Ÿ+SO32-+2H2O
NH3Ÿ+SO32-+2H2O
C.酸性条件下KIO3溶液与KI溶液发生反应生成I2:IO3-+5I-+6H+=3I2+3H2O
D.AgNO3溶液中加入过量的氨水:Ag++NH3·H2O=AgOH +NH4+
8.下列各组物质的无色溶液,不用其它试剂即可鉴别的是( )
①KOH Na2SO4 AlCl3 ②NaHCO3 Ba(OH)2 H2SO4
③HCl NaAlO2 NaHSO4 ④Ca(OH)2 Na2CO3 BaCl2
A.①② B.②③ C.①③④ D.①②④
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com