
题目列表(包括答案和解析)
5、在由水电离产生的 /L的溶液中,一定能大量共存的离子组是
/L的溶液中,一定能大量共存的离子组是
① 、
、 、
、 、
、 ②
② 、
、 、
、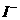 、
、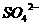 ③
③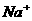 、
、 、
、 、
、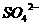
④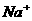 、
、 、
、 、
、 ⑤
⑤ 、
、 、
、 、
、
A.①③ B.③⑤ C.③④ D.②⑤
4、最近,科学家用一种称为“超酸”的化合物H(CB11H8Cl60)和C60反应,得到一种新型
离子化合物[HC60]+[CB11H6Cl2]-。这个很陌生物质生成的反应原理与我们中学化学中某个
反应原理相类似。该反应是
A. B.
B.
C. D.
D.
化学试卷共6页 第1页
3、三氟化氮(NF3)是无色无味的气体,它是由NH3和F2直接反应制得的:
 ,下列有关叙述错误的是
,下列有关叙述错误的是
A.F2氧化性比NF3强 B.NF3和NH4F都是还原产物
C.NF3是极性分子 D.NF3中的N是一3价
2、上世纪20年代,有人预言的O4分子,最近由意大利一所大学的科学家制造出了这种空
间结构对称的新型氧分子,你认为该氧分子
A.与O2是同分异构体 B.与O3是同素异形体
C.是一种新的氧化物 D.该分子摩尔质量为64克
1、下列分子结构中,原子的最外层电子不能都满足8电子稳定结构的是
A.CS2 B.PCl3 C.NO2 D.CCl4
14.周期表前20号元素中有A、B、C、D、E五种元素。已知它们都不是稀有气体元素,且原子半径依次减小,其中A和E同族,A与C、B与E原子的电子层数都相差2,A、B原子最外层电子数之比为1 : 4。
(1)写出元素符号:B 、D 、E 。
(2)A和C能以原子数1 : 1形成一种化合物,写出该化合物的化学式:
13.X、Y、Z三种元素位于周期表前20号元素之中。
已知:①XY2加水生成Y2Z2和化合物D;
②X的氧化物加水也生成D;
③Y的氧化物有两种。
请填空:(1)X、Y、Z的元素符号为X ,Y ,Z 。
(2)反应①的化学方程式为 。
(3)反应②的化学方程式为 。
12.右表是元素周期表的一部分。

(1)表中元素⑩的氢化物的化学式为 ,此氢化物的还原性比元素⑨的氢化物的还原性 (填强或弱)
(3)俗称为“矾”的一类化合物通常含有共同的元素是
(4)已知某些不同族元素的性质也有一定的相似性,如元素③与元素⑧的氢氧化物有相似的性质。写出元素③的氢氧化物与NaOH溶液反应的化学方程式
又如表中与元素⑦的性质相似的不同族元素是 (填元素符号)
11. X、Y、Z为三个不同短周期非金属元素的单质。在一定条件下有如下反应: (气),
(气), (气)。请针对以下两种不同情况回答:
(气)。请针对以下两种不同情况回答:
(1)若常温下X、Y、Z均为气体,且A和B化合生成固体C时有白烟产生,则:
<1>Y的化学式是_________;
<2>生成固体C的化学方程式是_______________________________________。
(2)若常温下Y为固体,X、Z为气体,A在空气中充分燃烧可生成B,则:
<1>B的化学式是__________;
<2>向苛性钠溶液中通入过量的A,所发生反应的离子方程式是
_____________________________________________;
<3>将Y与(1)中某单质的水溶液充分反应可生成两种强酸,该反应的化学方程式是________________________________________。
10.1919年,Langmuir提出等电子原理:原子数相同、电子总数相同的分子,互称为等电子体。等电子体的结构相似、物理性质相近。
(1)根据上述原理,仅由第2周期元素组成的共价分子中,互为等电子体的是:
和 ; 和 。
(2)此后,等电子原理又有所发展。例如,由短周期元素组成的微粒,只要其原子数相同,各原子最外层电子数之和相同,也可互称为等电子体,它们也具有相似的结构特征。在短周期元素组成的物质中,与NO2-互为等电子体的分子有: 、 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com