
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
2.НгДЅЗЈЩњВњH2SO4ЕФЙ§ГЬжаЃЌЖдЗЯЦјЁЂЗЯвКЁЂЗЯдќКЭЁАЗЯШШЁБЕФДІРэе§ШЗЕФЪЧ
ЂйЮВЦјгУАБЫЎДІРэ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁ ЂкЮлЫЎгУЪЏЛвШщДІРэ
ЂлЗЯдќгУРДдьЫЎФрЁЂСЖЬњЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЂмЩшжУЁАЗЯШШЁБЙјТЏВњЩњеєЦјЃЌЙЉШШЛђЗЂЕчЁЃ
AЃЎжЛгаЂйЂкЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎжЛгаЂйЂлЂмЁЁЁЁЁЁЁЁЁЁЁЁ CЃЎжЛгаЂйЂкЂлЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎШЋВП
1ЃЎЙигкЕчНтNaClШмвКЃЌЯТСаа№Ъіе§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁ)
AЃЎЕчНтЪБдкбєМЋЕУЕНТШЦјЃЌдквѕМЋЕУЕНН№ЪєФЦ
BЃЎШєдкбєМЋИННќШмвКжаЕЮШыKIШмвКЃЌШмвКГЪзиЩЋ
CЃЎШєдквѕМЋИННќЕФШмвКжаЕЮШыЗгЬЊЪдвКЃЌШмвКГЪЮоЩЋ
DЃЎЕчНтвЛЖЮЪБМфКѓЃЌНЋШЋВПЕчНтвКзЊвЦЕНЩеБжаЃЌГфЗжНСАшКѓШмвКГЪжаад
52.ВтСПвЛЖЈжЪСПЕФТСаПКЯН№гыЧПЫсШмвКЗДгІВњЩњЧтЦјЕФЬхЛ§ЃЌПЩвдЧѓЕУКЯН№жаТСКЭаПЕФжЪСПЗжЪ§ЃЎЯжгаЯТСаЪЕбщгУЦЗЃКжабЇЪЕбщГЃгУвЧЦїЁЂ800mLЩеБЁЂ100mLСПЭВЁЂЖЬОБВЃСЇТЉЖЗЁЂЭЭјЁЂТСаПКЯН№бљЦЗЁЂХЈбЮЫс(УмЖШ1.19gЃЏ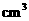 )ЁЂЫЎЃЎ
)ЁЂЫЎЃЎ
(1)ЧыЩшМЦвЛИіФмВтСПвЛЖЈСПКЯН№гыН№ЪєЗДгІЗХГіЦјЬхЕФзАжУРД(ЛЭМ)ЃЎ
(2)ВЙГфЯТСаЪЕбщВНжшЃЌжБЕНЗДгІПЊЪМНјаа(ЬњМмЬЈКЭЬњМаЕФАВзАПЩЪЁТд)ЃЎ
ЂйЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
ЂкЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃЂлЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЂмЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(3)КЯН№бљЦЗгУЭЭјАќЙќЕФФПЕФЪЧЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ 9дТ26ШеЭъГЩЃЁЃЁЃЁ
51.Ш§ХЉЮЪЬтЪЧеўИЎКЭЩчЛсЙизЂЕФЮЪЬтЃЌЛЏЗЪЪЧЭСЕиЕФгЊбјЦЗЁЃФГХЉзЪЩЬЕъГіЪлвЛжжЛЏЗЪЃЌЦфгааЇГЩЗжЮЊТШЛЏяЇЃЌЯжгћВтЖЈИУжжЛЏЗЪжаЕЊдЊЫиЕФжЪСПЗжЪ§ЃЌЩшМЦЪЕбщВНжшШчЯТ(дгжЪжаВЛКЌЕЊдЊЫиЃЌЧвдгжЪОљВЛгыбЮЫсЛђЧтбѕЛЏФЦШмвКЗДгІ)ЃК
ЂйХфжЦ1.00mol/LЕФHClШмвККЭ1.00mol/LЕФNaOHШмвКЃЛ
ЂкУПДЮШЁ1.00gДЫЛЏЗЪбљЦЗЃЌШмгк20mLеєСѓЫЎжаЃЛ
ЂлМгШы30.00mL1.00mol/LЕФNaOHШмвКЃЌНЋЗДгІКѓЕФШмвКМгШШжѓЗадМ1ЗжжгЃЌРфШДжСГЃЮТЃЛ
ЂмЁЁЁЁЁЁЁЁЃЛ
ЂнжиИДЂкЂлЂмВНВйзї1Ѓ2ДЮЃЛ
ЂоМЧТМећРэЪЕбщЫљЕУЪ§ОнЃЌМЦЫуИУЛЏЗЪжаЕЊдЊЫиЕФжЪСПЗжЪ§ЁЃ
ЧыЛиД№ЯТСаЮЪЬтЃК
(1)аДГіВНжшЂмжаЕФЪЕбщФкШн ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃЌаДГіЪЕбщВНжшЂмжаЕФРызгЗНГЬЪНЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(2)ЯТСавЧЦїжаЃЌХфжЦбЮЫсКЭЧтбѕЛЏФЦШмвКЖМФмгУЕНЕФЪЧ(ЁЁЁЁ )
A.ВЃСЇАєЁЁЁЁЁЁ B.ЭаХЬЬьЦНЁЁ ЁЁЁЁC.ЩеБЁЁЁЁЁЁ D.ТЉЖЗ
(3)ВНжшЂнЕФЪЕбщФПЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(4)ХфжЦБОЪЕбщЫљашЕФ1.00mol/LЕФбЮЫсКЭ1.00mol/LЕФNaOHШмвКДгНкдМЛЏбЇвЉЦЗЕФНЧЖШГіЗЂЃЌзюКУгІбЁгУЕФШнСПЦПЙцИёЗжБ№ЮЊЁЁЁЁЁЁЁЁ (ЬюзжФИбЁЯю)ЁЃ
A.50mLЃЌ50mLЁЁ B. 150mLЃЌ100mLЁЁ C. 100mLЃЌ150mLЁЁ D. 250mLЃЌ500mL
(5)ШєвдVx(mL)БэЪОЪЕбщЫљВтЖЈЯћКФбЮЫсЪ§ОнЕФЦНОљжЕЃЌИУЛЏЗЪбљЦЗжаЕЊдЊЫиЕФжЪСПЗжЪ§МЦЫуБэДяЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ(ВЛашвЊЛЏМђ)
50.ЙЄвЕжЦДПМюЕФЕквЛВНЪЧЭЈЙ§БЅКЭЪГбЮЫЎЁЂАБКЭЖўбѕЛЏЬМжЎМфЕФЗДгІЃЌжЦШЁЬМЫсЧтФЦОЇЬхЁЃИУЗДгІдРэПЩвдгУвдЯТЛЏбЇЗНГЬЪНБэЪОЃЌДЫЗДгІЪЧЗХШШЗДгІЁЃ
 ЁЁЁЁЁЁЁЁ
NH3 + CO2 + H2O + NaCl(БЅКЭ)ЁЁЁЁЁЁ NaHCO3(ОЇЬх)Ё§+ NH4Cl
ЁЁЁЁЁЁЁЁ
NH3 + CO2 + H2O + NaCl(БЅКЭ)ЁЁЁЁЁЁ NaHCO3(ОЇЬх)Ё§+ NH4Cl
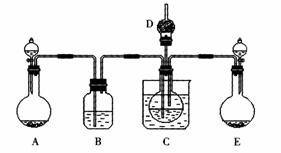
ЁЁ (1)ФГаЃбЇЩњЪЕбщаЁзщРћгУЩЯЪіЗДгІдРэЃЌЩшМЦШчЭМЫљЪОзАжУЃЌжЦШЁЬМЫсЧтФЦОЇЬхЁЃCЩеБжаЪЂгаБљЫЎЃЌDжазАгаеКЯЁСђЫсЕФЭбжЌУоЃЌЭМжаМаГжзАжУвбТдШЅЁЃ
|
 ЁЁ
fЃЎБЅКЭТШЛЏФЦШмвКЁЃ
ЁЁ
fЃЎБЅКЭТШЛЏФЦШмвКЁЃ
ЂйAжажЦБИЦјЬхЪБЃЌЫљашвЉЦЗЪЧ(бЁЬюзжФИДњКХ)ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛ
ЂкBжаЪЂгаБЅКЭЬМЫсЧтФЦШмвКЃЌЦфзїгУЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛ
ЂлдкЪЕбщЙ§ГЬжаЃЌЯђCжаЭЈШыЦјЬхЪЧгаЯШКѓЫГађЕФЃЌгІЯШЭЈШыЦјЬхЕФЛЏбЇЪНЮЊЁЁЁЁЁЁ ЃЛ
ЂмМьбщDГіПкДІЪЧЗёгаАБЦјвнГіЕФЗНЗЈЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁ (2)ИУаЁзщЭЌбЇЮЊСЫВтЖЈCжаЫљЕУОЇЬхЕФЬМЫсЧтФЦЕФДПЖШ(МйЩшОЇЬхжаВЛКЌЬМЫсбЮдгжЪ)ЃЌНЋОЇЬхГфЗжИЩдяКѓЃЌГЦСПжЪСПЮЊwgЁЃдйНЋОЇЬхМгШШЕНжЪСПВЛдйБфЛЏЪБЃЌГЦСПЫљЕУЗлФЉжЪСПЮЊngЁЃШЛКѓНјааШчЫљЪОЪЕбщЃК
 ЁЁ
ЁЁ
ЂйдкВйзїIIжаЃЌЮЊСЫХаЖЯМгШыТШЛЏИЦШмвКЪЧЗёЙ§СП,Цфжае§ШЗЕФЪЧ(бЁЬюзжФИађКХ)ЁЁЁЁ ЃЛ
AЃЎдкМгШыЧтбѕЛЏБЕШмвККѓЃЌеёЕДЁЂОВжУЃЌЯђШмвКжаМЬајМгШыЩйСПЧтбѕЛЏБЕШмвК
BЃЎдкМгШыЧтбѕЛЏБЕШмвККѓЃЌеёЕДЁЂОВжУЃЌЯђШмвКжадйМгШыЩйСПЬМЫсФЦШмвК
CЃЎдкМгШыЧтбѕЛЏБЕШмвККѓЃЌеёЕДЁЂОВжУЃЌШЁЩЯВуЧхвКдйМгШыЩйСПЬМЫсФЦШмвК
ЂкВйзїIIIЕФЗНЗЈЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЂЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЂЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛ
ЂлЫљЕУОЇЬхжаЬМЫсЧтФЦЕФДПЖШЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
49.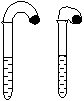 ЂХИпжаНЬВФжагаетбљвЛИіЪЕбщЃКдкСНжЇЪдЙмжаЗжБ№МгШы3mLЯЁбЮЫсЃЌНЋСНИіИїзАга0.3g NaHCO3Лђ Na2CO3ЗлФЉЕФаЁЦјЧђЗжБ№ЬздкСНжЇЪдЙмПкЁЃНЋЦјЧђФкЕФNaHCO3ЛђNa2CO3ЭЌЪБЕЙШыЪдЙмжаЃЌЙлВьЕНЯжЯѓШчЯТЃК
ЂХИпжаНЬВФжагаетбљвЛИіЪЕбщЃКдкСНжЇЪдЙмжаЗжБ№МгШы3mLЯЁбЮЫсЃЌНЋСНИіИїзАга0.3g NaHCO3Лђ Na2CO3ЗлФЉЕФаЁЦјЧђЗжБ№ЬздкСНжЇЪдЙмПкЁЃНЋЦјЧђФкЕФNaHCO3ЛђNa2CO3ЭЌЪБЕЙШыЪдЙмжаЃЌЙлВьЕНЯжЯѓШчЯТЃК
ЂйЪдЙмжа(ЬюВњЩњГСЕэЛђЦјЬхМАЗДгІЫйТЪЕШЯрЙиЯжЯѓ)
______________________________________________________
ЂкЪЂ______________ЕФЪдЙмжаЦјЧђБфЕУИќДѓЃЌДѓаЁЦјЧђ
(АќКЌЪдЙм) ЬхЛ§жЎБШдМЮЊ(ЬюзюМђЕЅећЪ§БШ)____________ЃЛ
ЂлМзЭЌбЇгУЪжДЅУўЪдЙмЃЌЗЂЯжЪЂNaHCO3ЗлФЉЕФЪдЙмБфРфЃЌЖјЪЂNa2CO3ЕФЪдЙмЮТЖШгаЩ§ИпЁЃгЩДЫЫћЕУГіЃКВЛЙмЦфзДЬЌШчКЮЃЌNaHCO3КЭHClЗДгІЮЊЮќШШЗДгІЃЌЖјNa2CO3КЭHClЗДгІЮЊЗХШШЗДгІЁЃРрЫЦШчжаКЭШШЃЌМзЭЌбЇаДГіСЫЯТСаШШЛЏбЇЗНГЬЪН(ЦфжаЁАaqЁБДњБэЫЎКЯЛђЮоЯоЯЁЪЭЕФКЌвх)ЃК
HCO3-(aq)+ H+(aq) =H2O(l)+ CO2(g) ЃЛЁїH>0ЁЁ
ЁЁЁЁЁЁЁЁЁЁ CO32-(aq)+ 2H+(aq)= H2O(l) + CO2(g)ЃЛ ЁїH<0ЁЁ
МзЯТНсТлЕФЗНЗЈЪЧЗёе§ШЗ____________ (Ьюе§ШЗЛђВЛе§ШЗ)
ЂЦ ЮЊбаОПЪЧЮќШШЛЙЪЧЗХШШЗДгІЃЌМЬајНјааСЫЯТСаЪЕбщ(УПДЮЪЕбщИїзі3ДЮЦНааЪЕбщЃЌШЁЦНОљжЕ)ЃК
|
ађКХ |
ЪдМС1 |
ЪдМС2 |
ЛьКЯЧАЮТЖШ |
ЛьКЯКѓзюИпЛђзюЕЭЮТЖШ |
|
Ђй |
35mLЫЎ |
2.5g NaHCO3ЙЬЬх |
20Ёц |
18.5Ёц |
|
Ђк |
35mLЫЎ |
3.2g Na2CO3ЙЬЬх |
20Ёц |
24.3Ёц |
|
Ђл |
35mLЯЁбЮЫс |
КЌ2.5g NaHCO3ЕФБЅКЭШмвК32.5mL |
20Ёц |
19Ёц |
|
Ђм |
35mLЯЁбЮЫс |
КЌ3.2g Na2CO3ЕФБЅКЭШмвК23.1mL+10mlЫЎ |
20Ёц |
24.2Ёц |
|
Ђн |
35mLЯЁбЮЫс |
2.5gNaHCO3ЙЬЬх |
20Ёц |
16.2Ёц |
|
Ђо |
35mLЯЁбЮЫс |
3.2g Na2CO3ЙЬЬх |
20Ёц |
25.1Ёц |
ЧыФуАяжњЬюаДЯрЙиФкШнЃК
ЂйИУбаОПБЈИцЕФЬтФПЪЧЁЖ________________________________________________ЁЗЃЛ
ЂкИУЪЕбщжаЫљгУЕФвЧЦїГ§ЪдЙмЁЂвЉГз(ЛђVаЭжНВл)ЁЂЦјЧђЁЂВЃСЇАєЁЂЩеБЁЂСПЭВЁЂБЃЮТЦПЭтЃЌЛЙашвЊЕФвЧЦїУћГЦЮЊ_________КЭ__________ЃЛЭЈЙ§ЩЯЪіЪЕбщПЩЕУГіЮхЬѕНсТлЃК
aЃКNaHCO3ЕФШмНтЪЧ_______(ЮќШШЛђЗХШШ)Й§ГЬЃЛЁЁ
bЃКNa2CO3ЕФШмНтЪЧ_______(ЮќШШЛђЗХШШ)Й§ГЬЃЛ
cЃКNaHCO3ЕФБЅКЭШмвККЭбЮЫсЕФЗДгІЪЧ____________(ЮќШШЛђЗХШШ)ЗДгІЃЛЁЁ
dЃКNa2CO3ЕФБЅКЭШмвККЭбЮЫсЕФЗДгІЪЧ____________(ЮќШШЛђЗХШШ)ЗДгІЃЛ
eЃКNaHCO3ЙЬЬхгыЯЁбЮЫсЗДгІЕФЗДгІШШЪЧгЩ______(ЬюaЁњdЕФзжФИ)ЕФШШаЇгІжЎКЭЁЃ
48.ЪЕбщЪвПЩгУТШЦјгыН№ЪєЬњЗДгІжЦБИЮоЫЎШ§ТШЛЏЬњЃЌИУЛЏКЯЮяЪЧзиКьЩЋЁЂвзГБНтЃЌ100ЁцзѓгвЪБЩ§ЛЊЁЃЯТЭМЪЧСНИібЇЩњЩшМЦЕФЪЕбщзАжУЁЂзѓБпЕФЗДгІзАжУЯрЭЌЃЌЖјгвБпЕФВњЦЗЪеМЏзАжУдђВЛЭЌЃЌЗжБ№Шч(Ђё)КЭ(Ђђ)ЫљЪОЁЃЪдЛиД№ЃК
ЁЁ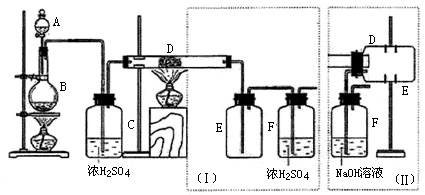
(1)BжаЗДгІЕФЛЏбЇЗНГЬЪНЮЊЃК___________________________________________________ЃЛ
ЁЁ(2)DжаЕФЗДгІПЊЪМЧАЃЌашХХГ§зАжУжаЕФПеЦјЃЌгІВЩШЁЕФЗНЗЈЪЧЃК
_______________________________________________________________ЁЃ
ЁЁ(3)DжаЗДгІЛЏбЇЗНГЬЪНЮЊЃК________________________________ЁЃ
ЁЁ(4)зАжУ(Ђё)ЕФжївЊШБЕуЪЧЃК
________________________________________________________ ЁЃ
ЁЁ(5)зАжУ(Ђђ)ЕФжївЊШБЕуЪЧЃК_____________________________ЁЃ
ШчЙћбЁгУДЫзАжУРДЭъГЩЪЕбщЃЌдђБиаыВЩШЁЕФИФНјДыЪЉЪЧЃК
__________________________________________________________
47.гУЯТУцЛ§МИжжЗНЗЈПЩвджЦЕУFe(OH)2ГСЕэЃК
ЗНЗЈ1.гУВЛКЌFe3+ЕФFeSO4ШмвКгыгУВЛКЌбѕЦјЕФгУеєСѓЫЎХфжЦЕФNaOHШмвКЗДгІжЦБИЃЌ
1).гУСђЫсбЧЬњОЇЬхХфжЦЩЯЪіFeSO4ШмвКЪБЃЌЛЙашМгШы_________________ЁЁЁЁ
2).Г§ШЅеєСѓЫЎжаШмНтЕФбѕЦјГЃВЩгУ___________ЁЁ ЕФЗНЗЈЁЃ
3).ЩњГЩАзЩЋЕФFe(OH)2ГСЕэЕФВйзїЪЧгУГЄЕЮЙмЮќШЁВЛКЌбѕЦјЕФNaOHШмвКЃЌВхШыFeSO4ШмвКЯТУцЃЌдйМЗГіNaOHШмвКЃЌетбљВйзїЕФРэгЩЪЧ _____________________________________.
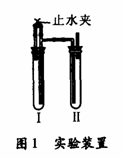 ЗНЗЈ2.дкШчЭМ1ЕФзАжУжаЃЌгУNaOHШмвКЁЂЬњаМЃЌЯЁСђЫсЕШЪдМСжЦБИЃЌ
ЗНЗЈ2.дкШчЭМ1ЕФзАжУжаЃЌгУNaOHШмвКЁЂЬњаМЃЌЯЁСђЫсЕШЪдМСжЦБИЃЌ
1)дкЪдЙмЂёРяМгШыЕФЪдМСЪЧ______________________________
2).дкЪдЙмЂђРяМгШыЕФЪдМСЪЧ____________________________
3)ЮЊСЫжЦЕУАзЩЋFe(OH)2ГСЕэЃЌдкЪдЙмЂёКЭЪдЙмЂђжаМгШыЪдМСЃЌДђПЊжЙЫЎМаЃЌШћНєШћзгКѓЕФЪЕбщВНжшЪЧ_______________________________
4).етбљЩњГЩЕФFe(OH)2ГСЕэФмНЯГЄЪБМфБЃГжАзЩЋЃЌЦфРэгЩЪЧ
______________________________________________
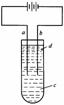 ЗНЗЈ3.гЩгкFe(OH)2МЋвзБЛбѕЛЏЃЌЫљвдЪЕбщКмФбгУбЧЬњбЮШмвКгыЩеМюЗДгІжЦЕУАзЩЋДПОЛЕФFe(OH)2ГСЕэЁЃгІгУШчЭМЫљЪОЕчНтЪЕбщПЩжЦЕУАзЩЋДПОЛЕФFe(OH)2ГСЕэЁЃСНЕчМЋЕФВФСЯЗжБ№ЮЊЪЏФЋКЭЬњЁЃ
ЗНЗЈ3.гЩгкFe(OH)2МЋвзБЛбѕЛЏЃЌЫљвдЪЕбщКмФбгУбЧЬњбЮШмвКгыЩеМюЗДгІжЦЕУАзЩЋДПОЛЕФFe(OH)2ГСЕэЁЃгІгУШчЭМЫљЪОЕчНтЪЕбщПЩжЦЕУАзЩЋДПОЛЕФFe(OH)2ГСЕэЁЃСНЕчМЋЕФВФСЯЗжБ№ЮЊЪЏФЋКЭЬњЁЃ
ЁЁ(1)aЕчМЋВФСЯгІЮЊ________ЃЌЕчМЋЗДгІЪНЮЊ_________________________ЁЃ
ЁЁ(2)ЕчНтвКcПЩвдЪЧ(ЬюБрКХ)__________________ЁЃ
ЁЁ AЃЎДПЫЎЁЁЁЁ BЃЎNaClШмвКCЃЎNaOHШмвКЁЁЁЁ DЃЎCuCl2ШмвК
ЁЁ(3)dЮЊБНЃЌЦфзїгУЮЊ_________________ЃЌдкМгШыБНжЎЧАЖдcгІзіКЮ
МђЕЅДІРэ?_____________________ЁЃ
ЁЁ (4)ЮЊСЫдкНЯЖЬЪБМфФкПДЕНАзЩЋГСЕэЃЌПЩВЩШЁЕФДыЪЉЪЧ(ЬюБрКХ)_________
ЁЁ AЃЎИФгУЯЁСђЫсзїЕчНтвКЁЁЁЁ BЃЎЪЪЕБдіДѓЕчдДЕФЕчбЙ
ЁЁ CЃЎЪЪЕБМѕаЁСНЕчМЋМфОрРыЁЁЁЁ DЃЎЪЪЕБНЕЕЭЕчНтвКЕФЮТЖШ
ЁЁ (5)ШєcЮЊNa2SO4ШмвКЃЌЕБЕчНтвЛЖЮЪБМфПДЕНАзЩЋFe(OH)2ГСЕэКѓЃЌдйЗДНгЕчдДЕчНтЃЌГ§СЫЕчМЋЩЯПДЕНЦјХнЭтЃЌЛьКЯЮяжаСэвЛУїЯдЯжЯѓЮЊ
____________________________________________ЁЃ
46.СђЫсЭЕФжЦБИЪЕбщЪЧЮоЛњЛЏбЇЪЕбщНЬбЇжавЛИіБизіЪЕбщЃЌФГбаОПадбЇЯАаЁзщЩшМЦСЫШчЯТСНИіЪЕбщЗНАИЃК
ЪЕбщвЛЃК
вђЭВЛФмгыЯЁСђЫсжБНгЗДгІЃЌЪЕбщжавдХЈЯѕЫсЗжДЮМгШыЕНЭКЭЯЁСђЫсЕФЛьКЯвКжаЃЌМгШШЪЙжЎЭъШЋЗДгІЃЌЭЈЙ§еєЗЂЁЂЮіОЇЕШВйзїЕУЕНСђЫсЭОЇЬхЁЃ
(1)ХЈЯѕЫсЫљЦ№ЕФзїгУЪЧ___________________________________
(2)ИУЗДгІЕФдРэЪЧ(гУЛЏбЇЗНГЬЪНБэЪО)
______________________________________________ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЪЕбщЖўЃК
вдПеЦјЮЊбѕЛЏМСЕФвЛВНбѕЛЏЗЈЃЌНЋПеЦјЛђбѕЦјжБНгЭЈШыЕНЭЗлгыЯЁСђЫсЕФЛьКЯЮяжаЃЌЦфЗДгІдРэЮЊ2Cu + O2 + 2H2SO4 = 2CuSO4 + 2H2O ЃЌЕЋЗДгІЫйТЪЬЋаЁЃЌЕБЩ§ИпЮТЖШЕН80-90ЁцЃЌЗДгІШдШЛЛКТ§ЁЃШчдкЭЗлКЭЯЁСђЫсЕФЛьКЯЮяжаМгШыЩйСПFe2(SO4)3ШмвКЃЌдђЫйТЪУїЯдМгПьЁЃ
(3)гУРызгЗНГЬЪНБэЪОЫйТЪУїЯдМгПьЕФдРэ
______________________________________________ЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЃ
Fe2(SO4)3ЕФзїгУЪЧ__ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(4)ЕУЕНЕФЛьКЯвКгУ______________ЕїНкpH =2-4ЃЌЪЙFe3+аЮГЩFe(OH)3ГСЕэЖјГ§ШЅЃЌЧвFe(OH)3ПЩвдбЛЗЪЙгУЁЃ
(5)ЧыИљОнвдЩЯФкШнЃЌЖдетСНИіЪЕбщЗНАИНјааЦРМлЃЌЬюЯТБэЃК
|
ЁЁ |
ЪЕ бщ
вЛ |
ЪЕ бщ
Жў |
|
жївЊгХ Еу |
ЁЁ ЁЁ ЁЁ |
ЁЁ ЁЁ |
|
жївЊШБ Еу |
ЁЁ ЁЁ |
ЁЁ ЁЁ ЁЁ |
45. ФГаЫШЄаЁзщЭЌбЇЙВЭЌЩшжУСЫШчЭМЫљЪОЕФЪЕбщзАжУЃЌМДПЩгУгкжЦШЁЦјЬхЃЌгжПЩгУгкбщжЄЮяжЪЕФаджЪЁЃЧыЛиД№ЯТСаЮЪЬтЃК
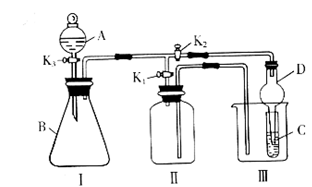

(1)ЁЁЁЁЁЁ РћгУзАжУЂёжЦШЁЦјЬхЃЌЩњГЩЦјЬхЕФЗДгІгІОпБИЕФЬѕМўЪЧ
_________________________________________________________________ЁЃ
зАжУЂѓжавЧЦїDдкЪЕбщжаЕФзїгУЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(2)РћгУЂёЁЂЂђзАжУжЦШЁЦјЬх(K2ЙиБеЃЌK1ДђПЊ)ЁЃ
МзЭЌбЇШЯЮЊЃКРћгУЂђзАжУПЩвдЪеМЏH2ЁЂNH3ЕШЦјЬхЃЌЕЋВЛФмЪеМЏO2КЭNOЕШЦјЬхЃЌЦфРэгЩЪЧ________________________________________________________________________ЁЃ
ввЭЌбЇШЯЮЊЃКРћгУЂђзАжУзїМђвзИФНј(ВЛИФБфвЧЦїзАжУ)вВПЩвдЪеМЏO2КЭNOЕШЦјЬхЃЌЕЋВЛФмЪеМЏSO2ЕШЦјЬхЃЌИФНјЕФЗНЗЈЪЧ______________________________________________ЃЌРћгУЂђзАжУдйзїМђвзИФНј(ВЛИФБфвЧЦїзАжУ)вВПЩвдЪеМЏSO2ЕШЦјЬхЃЌИФНјЕФЗНЗЈЪЧ_________________________________________________________ЁЃ
(3)РћгУЂёЁЂЂѓзАжУбщжЄЮяжЪЕФаджЪ(K2ДђПЊЃЌK1ЙиБе)ЁЃШчЩшМЦЪЕбщжЄУїбѕЛЏадЃК
KMnO4ЃОCl2ЃОBr2дђдкAжаМгХЈбЮЫсЃЌBжаМг__________ЃЌCжаМг________ЁЃЙлВьЕНCжаЕФЯжЯѓЪЧ________________________________________ЁЃЁЁ
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com