
题目列表(包括答案和解析)
(1-10题有一个正确选项;11-20题有一个或两个正确选项,漏选得1分,错选得0分)
1.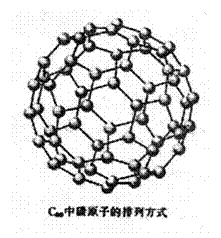 C60发现导致了一门新兴学科--碳球化学的兴起。根据对其分子结构特点的研究,科学家预测。C60的很多化合物可能在超导体、长效药物载体等方面有着重要的应用。目前已证明,C60与金属钾作用得到一种物质K3C60,其在低温下具有超导性能。下列说法中,不正确的是 ( )
C60发现导致了一门新兴学科--碳球化学的兴起。根据对其分子结构特点的研究,科学家预测。C60的很多化合物可能在超导体、长效药物载体等方面有着重要的应用。目前已证明,C60与金属钾作用得到一种物质K3C60,其在低温下具有超导性能。下列说法中,不正确的是 ( )
A.K3C60是一种新型的化合物
B.C6+0是一种含碳化合物
C.金刚石、石墨、C60是碳元素的同素异形体
D.在C60和K3C60中,碳元素分别以游离态和化
合化合态形式存在
26. (14分)
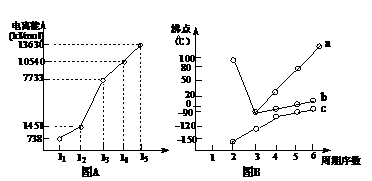 (1)I.短周期某主族
(1)I.短周期某主族
元素M的电离能情况如右
图(A)所示。则M元素
位于周期表的第 族。
II.图B折线c可以
表达出第 族元素氢
化物的沸点的变化规律。两
位同学对某主族元素氢化物的沸点的变化趋势画出了两条折线a和b,你认为正确的是:
(填“a”或“b”);
部分有机物的熔沸点见下表:
|
烃 |
CH4 |
CH3CH3 |
CH3(CH2)2CH3 |
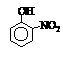
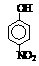
硝基苯酚 |
 |
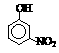 |
 |
|
沸点/℃ |
-164 |
-88.6 |
-0.5 |
熔点/℃ |
45 |
96 |
114 |
由这些数据你能得出的结论是(至少写2条): ,
。
(2)COCl2俗称光气,分子中C原子采取 杂化成键;其中碳氧原子之间共价键含有 (填字母):a.2个σ键;b.2个π键;c.1个σ键、1个π键。
(3)金属是钛(22Ti) 将是继铜、铁、铝之后人类广泛使用的第四种金属,试回答:
I.Ti元素的基态原子的价电子层排布式为 ;
II.已知Ti3+可形成配位数为6的配合物。现有紫色和绿色两种含钛晶体,其组成均为TiCl3·6H2O。为测定这两种晶体的化学式,设计了如下实验:a.分别取等质量的两种晶体的样品配成溶液;b.向两种溶液中分别滴入AgNO3溶液,均产生白色沉淀;c.沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量发现:其沉淀质量:绿色晶体为紫色晶体的2/3。则绿色晶体配合物的化学式为 。
25.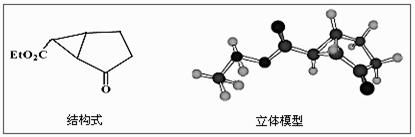 (14分)Ⅰ、下图是某药物中间体的结构示意图:
(14分)Ⅰ、下图是某药物中间体的结构示意图:
观察上面的结构式与立体模型,通过对比指出结构式中的“Et表示 ;该药物中间体分子的分子式为 。
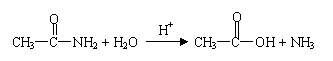
 Ⅱ、已知:
有机物A是一种镇痛解热药品,其结构简式为:
Ⅱ、已知:
有机物A是一种镇痛解热药品,其结构简式为:
(1)B、D的关系是 (填序号);
a.同种物质 b.互为同系物 c.互为同分异构体
(2)写出反应②的化学方程式,注明反应类型:
, ;
(3)1molA在氢氧化钠溶液中水解,最多消耗氢氧化钠 mol;
(4)能与FeCl3溶液发生显色反应,且属于酯类的C的同分异构体有多种,写出其中一种的结构简式 。
24.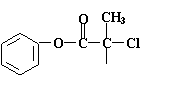 某有机物X是农药生产中的一种中间体,其结构简式为
某有机物X是农药生产中的一种中间体,其结构简式为
(如图)
(1)X的分子式为____________
(2)X分子中含有的官能团有____________________ CH2-OH
(3)X可能发生多种反应,下列有关X发生化学反应的叙述中正确的是( )(多选扣分)
A.在氢氧化钠醇溶液中共热能发生消去反应
B.在铜作催化剂时加热,可被氧气氧化生成能发生银镜反应的物质
C.在浓硫酸存在时加热可发生消去反应
D.在铁作催化剂时,可跟液溴发生取代反应
(4)写出X跟氢氧化钠稀溶液共热时所发生反应的化学方程式
________________________________________________。
(5)X可能有多种同分异构体,写出符合下列条件的一种同分异构体的结构简式 __。
①苯环只有分处在对位的两个取代基②遇氯化铁溶液不变色,但遇pH试纸显红色
22. (12分)向草酸(H2C2O4)溶液中逐滴加入酸性高锰酸钾溶液时,溶液褪色总是先慢后快。对其原因,某研究性学习小组结合化学反应原理提出猜想与假设,并设计了一系列实验进行探究:
实验(1):在2支试管中分别加入10mL等浓度的草酸溶液,在①号瓶中加入少量硫酸锰固体。然后在两支试管中加入0.1 mol·L-1的高锰酸钾溶液。现象如下(表1)
|
加入药品 |
不加硫酸锰的硫酸酸化的草酸溶液 |
加少量硫酸锰的硫酸酸化的草酸溶液 |
|
实验现象(褪色时间) |
草酸褪色很慢(30s) |
草酸褪色很快(2s) |
实验(2):在2支试管中分别加入5 mL等浓度的草酸溶液,在②号试管中再滴加10滴稀硫酸,然后加入5滴0.1 mol·L-1的高锰酸钾溶液。现象如下(表2)
|
编号 |
①号试管 |
②号试管 |
|
褪色时间 现象 |
100 s |
90 s |
|
均有气泡产生;②号试管的溶液褪色比①号试管的溶液快,它们颜色变化如下:紫红色→红色→橙红色→橙色→黄色→无色。 |
实验(3):取3支试管分别加入5 mL等浓度草酸溶液,然后在①、②、③号试管中依次加入10滴、1 mL、2 mL稀硫酸溶液,各加入5滴0.1 mol·L-1的高锰酸钾溶液,然后置于温度为65℃的水浴中加热。观察现象(表3)。
|
编号 |
①号试管 |
②号试管 |
③号试管 |
|
褪色时间 实验现象 |
80 s |
100 s |
120 s |
|
均有气泡产生;①号试管的溶液褪色比②、③号试管的溶液快,它们颜色变化如下:紫红色→红色→橙红色→橙色→黄色→无色。 |
(1) 该研究性学习小组提出猜想与假设的理论依据是(从化学反应原理的角度作答):
。
(2)该研究性学习小组进行实验时所用的方法是科学实验中常用的一种方法,该方法
叫 法;
(3)设计实验(1)对应的假设是 ;
实验(1)得出的结论是 。
(4)由实验(2)和实验(3)得出的结论是
;
(5)据有关现象写出草酸溶液与酸性高锰酸钾溶液的离子方程式:
H2C2O4+ MnO4-+ = Mn2++ + H2O
21.(16分) N2在化工生产、农业、医疗、航天航空等诸多领域用途广泛。某化学兴趣小组同学为探究在实验室制备较为纯净N2,进行了认真的准备。请你参与交流与讨论。
[查阅资料] N2的制法有下列三种方案:
方案1:加热条件下,以NH3还原CuO可制得N2,同时获得活性铜粉。
方案2:加热NaNO2和NH4Cl的浓溶液制得N2。
方案3:将空气缓缓通过灼热的铜粉获得较纯的N2。
[实验准备] 以实验室常见仪器(药品)等设计的部分装置如下图(有的夹持和加热仪器未画出)。
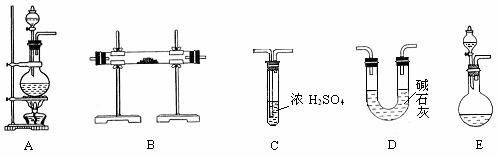
[分析交流]
⑴若按方案1制得干燥、纯净的N2,且需要的NH3以生石灰和浓氨水作原料,整套制气装置按气流从左到右的顺序连接的顺序是(填写序号,下同)_______________。获得N2的反应原理是(写反应方程式)_________________________________。
⑵若以排水法收集N2,其中会混入水蒸气。但也不宜用排空气法,其原因是____________________________________。你提出的收集方法是__________________。
⑶若以方案2制得N2,应选择的发生装置是__________。为保证实验安全顺利进行,操作时应____________________________________________________(填写两点)。
⑷上述三个方案中,制得的N2纯度最差的是__________。在N2纯度要求不甚严格的情况下,有人建议将方案1和方案3结合使用,你认为其优越性在于___________________。
20.(11分)在一固定容积的密闭容器中进行着如下反应:
CO2(g) + H2(g) 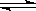 CO(g) + H2O(g)
CO(g) + H2O(g)
其平衡常数K和温度t的关系如下:
|
t℃ |
700 |
800 |
850 |
1000 |
1200 |
|
K |
2.6 |
1.7 |
1.0 |
0.9 |
0.6 |
(1) K的表达式为: ; (2) 该反应的正反应为 反应(“吸热”或“放热”)
(3) 能判断该反应是否已经达到化学平衡状态的是:
A.容器中压强不变 B.混合气体中CO浓度不变
C.v(H2)正 = v(H2O)逆 D.c(CO2) = c(CO)
(4) 在850℃时,可逆反应:CO2(g)
+ H2(g) 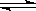 CO(g) + H2O(g),在该容器内各物质的浓度变化如下:
CO(g) + H2O(g),在该容器内各物质的浓度变化如下:
|
时间/min |
CO2 (mol/L) |
H2 (mol/L) |
CO (mol/L) |
H2 O ( mol/L) |
|
0 |
0.200 |
0.300 |
0 |
0 |
|
2 |
0.138 |
0.238 |
0.062 |
0.062 |
|
3 |
c1 |
c2 |
c3 |
c3 |
|
4 |
c1 |
c2 |
c3 |
c3 |
计算:3min-4min达到平衡时CO的平衡浓度c3和CO2 (g)的转化率,要求写出简单的计算过程(c3精确到小数点后面三位数)。
19.(12分)海水中蕴藏着丰富的资源。海水综合利用的流程图如下。
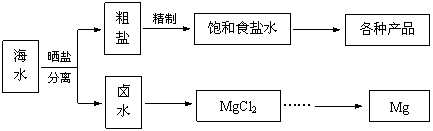
(1)用NaCl做原料可以得到多种产品。
① 工业上由NaCl制备金属钠的化学方程式是_______________________________。
② 实验室用惰性电极电解100 mL0.1 mol/LNaCl溶液,若阴阳两极均得到112 mL气体(标准状况),则所得溶液的pH为_________(忽略反应前后溶液的体积变化)。
③ 电解氯化钠稀溶液可制备“84消毒液”,通电时氯气被溶液完全吸收,若所得消毒液仅含一种溶质,写出相应的化学方程式:____________________________。
(2)分离出粗盐后的卤水中蕴含着丰富的镁资源,经转化后可获得MgCl2粗产品。
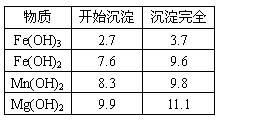 ① 粗产品的溶液中含有Na+、Fe2+、Fe3+和Mn2+,需将Fe2+、Fe3+、Mn2+转化为沉淀除去。Fe(OH)2呈絮状,常将其转化为Fe(OH)3而除去(生成氢氧化物沉淀的pH见表)。若只加一种上述(1)中得到的产品,该物质的化学式为_______________,控制溶液的pH为____________________。
① 粗产品的溶液中含有Na+、Fe2+、Fe3+和Mn2+,需将Fe2+、Fe3+、Mn2+转化为沉淀除去。Fe(OH)2呈絮状,常将其转化为Fe(OH)3而除去(生成氢氧化物沉淀的pH见表)。若只加一种上述(1)中得到的产品,该物质的化学式为_______________,控制溶液的pH为____________________。
② 在家用电热水器不锈钢内胆表面镶嵌镁棒,利用电化学原理来防止内胆腐蚀,
写出正极的电极反应式:____________________________________________。
18. LiFePO4新型锂离子动力电池以其独特的优势成为奥运会绿色能源的新宠。已知该电池放电时的电极反应式为:正极 FePO4+Li++e-==LiFePO4 负极 Li-e-== Li+
下列说法中正确的是
A.充电时电池反应为FePO4+Li = LiFePO4
B.充电时动力电池上标注“+”的电极应与外接电源的正极相连
C.放电时,在正极上是Li+得电子被还原
D.放电时电池内部Li+向负极移动
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com