
题目列表(包括答案和解析)
21.(11分)现在普遍应用的工业合成氨的方法是哈伯于1905年发明的,但此法反应物的转化率不高。
2001年两位希腊化学家提出了电解合成氨的方法,即在常压下把氢气和用氦气稀释的氮气,分别通入一个加热到570℃的电解池中,氢气和氮气在电极上合成了氨,反应物转化率大大提高。
请回答:
(1)哈伯合成氨的化学方程式为____________ ;在电解法合成氨的电解池中______(填“能”或“不能”)用水作电解质溶液的溶剂,原因是_________________________________
。
(2)新法合成氨电解池中的电解质能传导H+,请写出阴极反应式____________________ ______。
(3)氨是一种重要的化工原料,在一定条件下氨可与其他物质反应生成化肥──尿素( CO(NH2)2 )。已知3.01×1022个尿素分子在高温、高压下分解生成0.85g NH3、0.56 L CO2(标准状况下)和一定数量的三聚氰胺分子。三聚氰胺的相对分子质量为126,则三聚氰胺的分子式为 ,尿素分解的化学反应方程式为 。已知三个A分子可反应得到一分子三聚氰胺,请写出A的结构式 。
崇文区2008-2009学年度第一学期高三期末统一练习
20.(11分)下图为常见气体制备、分离、干燥和性质验证的部分仪器装置(加热设备及夹持固定装置均略去,已知乙醇的沸点为78.5℃),请根据要求完成下列问题(仪器装置可任意选用,必要时可重复选择,a、b为旋钮)。
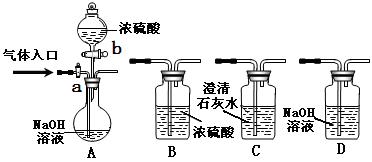
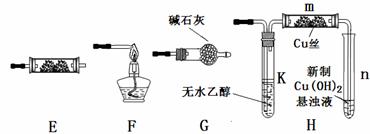
(1)若A中气体入口通入CO和CO2的混合气体,E内放置CuO,欲得到纯净干燥的CO,并验证其还原性及氧化产物,所选装置的连接顺序为________ ___ (填写装置代号)。能验证CO氧化产物的实验现象是_______________________________ ____。
(2)完成(1)实验后,将A中a旋钮关闭,并在E内放置Na2O2,按A→E→D→B→H装置顺序,制取纯净干燥的O2,并用O2氧化乙醇。
①为获得氧气,关闭a旋钮后,首先需进行的操作是 。
②为得到平稳的乙醇蒸气流,提高反应效率,可采取的措施是(用文字简述或在原装制图的相应位置画出简图)__________ ___;
m中发生反应的化学方程式是________________________________________________ ____。
③若想观察到试管n中有红色沉淀出现,还需要进行的操作是________ __________。
19. (12分) 某有机物A只含C、H、O三种元素,可用作染料、医药的中间体,具有抗菌、祛痰、平喘作用。A的蒸气密度为相同状况下氢气密度的77倍,有机物A中氧的质量分数约为41.6%,请结合下列信息回答相关问题。
① A可与NaHCO3溶液作用,产生无色气体;
② 1 mol A与足量金属钠反应生成H2 33.6L(标准状况);
③ A可与FeCl3溶液发生显色反应;
④ A分子苯环上有三个取代基,其中相同的取代基相邻,不同的取代基不相邻。
请回答:
(1)A的分子式是 ;A中含氧官能团的名称是 。
(2)按要求写出下面反应的化学方程式:
A + NaHCO3(溶液): 。
(3)已知:
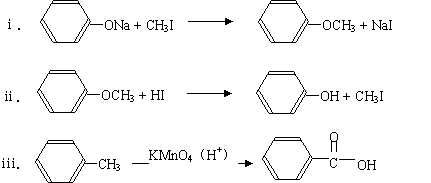

有机物B的分子式为C7H8O2,在一定条件下,存在如下转化,可最终生成A:
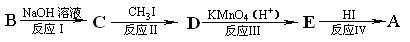
请回答:
①反应Ⅱ的化学方程式是 。
②上述转化中,反应Ⅰ、Ⅱ两步的作用是 。
③B可发生的反应有 (填字母)。
a. 取代反应 b. 加成反应 c. 消去反应 d. 水解反应
(4)芳香族化合物F与A互为同分异构体,可发生银镜反应,1 mol F可与含3 mol溶质的NaOH溶液作用,其苯环上的一卤代物只有一种。写出符合要求的F的一种可能的结构简式 。
18.(12分)如下图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。
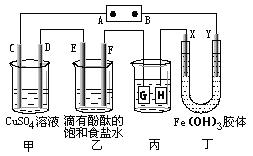
请回答:
(1)B极是电源的 ,一段时间后,甲中溶液颜色 ,丁中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深,这表明 ,在电场作用下向Y极移动。
(2)若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为 。
(3)现用丙装置给铜件镀银,则H应该是 (填“镀层金属”或“镀件”),电镀液是 溶液。当乙中溶液的pH是13时(此时乙溶液体积为500mL),丙中镀件上析出银的质量为 ,甲中溶液的pH (填“变大”、“变小”或“不变”)。
(4)若将C电极换为铁,其他装置都不变,则甲中发生总反应的离子方程式是 。
16.下列比较中,正确的是
A.常温下,同浓度的一元酸HA比HB易电离,则相同浓度的NaA溶液比NaB溶液的pH大
B.0.2 mol/L NH4NO3 和 0.l mol/L NaOH 溶液等体积混合后:
c(NH4+) > c (NO3- ) > c (Na+) > c (OH-) >c (H+)
C.物质的量浓度相等的醋酸溶液和氢氧化钠溶液等体积混合:
c (Na+) + c(H+) = c (CH3COO-) + c (OH-) + c (CH3COOH)
D.同浓度的下列溶液:①NH4Al(SO4)2 ②NH4Cl ③NH3·H2O ④CH3COONH4,
其中c(NH4+) 由大到小的顺序是:①>②>④>③
第Ⅱ卷(非选择题 共60分)
本卷共5小题,共60分。
15.将1mol H2(g) 和2mol I2(g) 置于2L密闭容器中,在一定温度下发生反应:
 H2(g)+ I2(g)
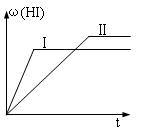
H2(g)+ I2(g) 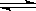 2HI(g) ;△H<0,并达到平衡,HI的体积
2HI(g) ;△H<0,并达到平衡,HI的体积
分数ω(HI)随时间变化如图(II)所示。若改变反应条件,
ω(HI)的变化曲线如图(Ⅰ)所示,则改变的条件可能是
A.恒温恒容条件下,加入适当催化剂
B.恒温恒压条件下,充入1 mol N2
C.恒容条件下,升高温度
D.恒温恒容条件下,再充入1 mol H2(g) 和2 mol I2(g)
14.下列划线部分物质在充分反应后能完全消耗的有
A.含少量CO2的1molH2与1mol Na2O2在密闭容器中,不断用电火花点燃
B.1mol MnO2与含4mol HCl的浓盐酸加热反应
C. 1mol 无水C2H5OH、2mol冰醋酸与浓H2SO4混合共热
D.少量淀粉酶加入含2g淀粉的溶液中,适当温度下反应足够长的时间
13.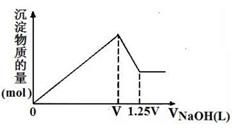 有MgCl2、Al2(SO4)3的混合溶液,向其中不断加入
有MgCl2、Al2(SO4)3的混合溶液,向其中不断加入
NaOH溶液,得到沉淀的物质的量与加入NaOH溶液体积的关系
如图所示,则溶液中MgCl2与Al2(SO4)3的物质的量浓度之比为
A.1:1 B.2:3
C.3:2 D.2:1
12.根据下列事实得出的结论正确的是


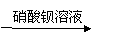
A. Na2SO3试样 白色沉淀 沉淀不溶解
结论:此Na2SO3试样已变质
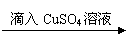
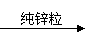
B.稀硫酸 产生气泡的速率较慢 产生气泡的速率明显加快
结论:CuSO4对此反应有催化作用


C.某溶液 瓶口产生白雾
结论:此溶液一定为浓盐酸


D.无色试液 产生无色无味气体 石灰水变浑浊
结论:原无色试液中可能含有CO32-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com