
题目列表(包括答案和解析)
23.碳酸钠是造纸、玻璃、纺织、制革等行业的重要原料。工业碳酸钠(纯度约98%)
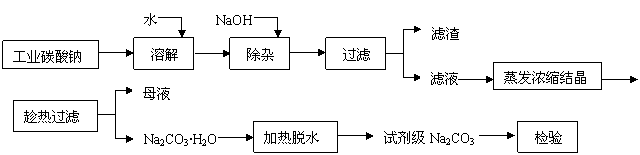 中含有Ca2+、Mg2+、Fe3+、Cl-和SO
中含有Ca2+、Mg2+、Fe3+、Cl-和SO 等杂质,提纯工艺路线如下:
等杂质,提纯工艺路线如下:
已知碳酸钠的溶解度(S)随温度变化的曲线如图所示:
回答下列问题:
(1)滤渣的主要成分为_________________________。
(2)“趁热过滤”的原因是______________________。
(3)在实验室做Na2CO3·H2O脱水实验,判断其脱水完全的方法是:__________________。
(4)生产过程中“母液”__________(填“能”或“不能”)循环使用。若不能,其原因是:
_________________________________________________________________________。
(5)已知:Na2CO3·10H2O(s)=Na2CO3(s)+10H2O(g);ΔH1= +532.36 kJ·mol-1
Na2CO3·10H2O(s)=Na2CO3·H2O(s)+9H2O(g);ΔH2= +473.63 kJ·mol-1
写出Na2CO3·H2O脱水反应的热化学方程式_________________________________________。
22.(14分)A、B、C、D、E均为中学化学常见物质,它们之间的反应关系如图所示:
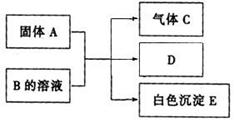
(1)若A是短周期原子半径最大的元素(稀有气体除外)构成的单质,E既可溶于盐酸又可溶于NaOH溶液,则E溶于NaOH溶液的离子方程式为 ;工业上冶炼A的化学反应方程式为 ;气体C在使用前需要检验纯度,操作方法是 。
(2)若C是一种四原子分子,燃烧时有浓烈的黑烟,且A与B的溶液反应时只生成气体C、CaCO3和H2O。C的电子式为 ;B的名称为 ;实验室制取C的化学反应方程式为 ;C的燃烧热为1300kJ·mol-1,则C燃烧的热化学方程式为 。
21.(7分)天然气化工是指通过甲烷的化学反应来生产一系列化工产品的工艺过程,是以C1化学为中心面向21世纪的重要开发领域。以天然气为原料经下列反应路线可得工程塑料PBT。
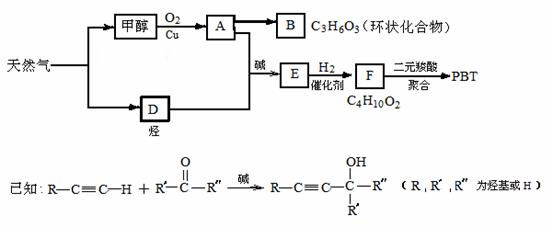
(1)B分子结构中只有一种氢、一种氧、一种碳,则B的结构简式是 ;B的同分异构体中与葡萄糖具有类似结构的是 。(写结构简式)
(2)F的结构简式是 ;PBT属于 类有机高分子化合物。
(3)由A、D生成E的反应方程式为 ,其反应类型为 。
(4)E的同分异构体G不能发生银镜反应,能使溴水褪色,能水解且产物的碳原子数不等,则G在NaOH溶液中发生水解反应的化学方程式是 。
20.(5分)下列有关实验的叙述,正确的是 (填序号,多选一个倒扣1分)
A.分液时,分液漏斗下层液体从下口放出,上层液体从上端口倒出
B.氢气还原氧化铜实验中,先加热氧化铜后通氢气
C.蒸馏石油时,加热一段时间后发现未加碎瓷片,立刻拔开橡皮塞并投入碎瓷片
D.实验室做钠的实验时,余下的钠屑投入到原试剂瓶中
E.浓硫酸不小心沾到皮肤上,立刻用稀NaOH溶液洗涤
F.不慎将苯酚沾到皮肤上,立即用酒精清洗;
G.配制浓硫酸和浓硝酸的混合酸时,将浓硫酸沿器壁慢慢加入浓硝酸中,并不断搅拌;
H.配制银氨溶液时,将稀氨水慢慢滴加到硝酸银溶液中,产生沉淀后继续滴加到沉淀刚好溶解为止
19.(5分)在下列①~⑩中选出适宜的词语填入下列每小题的空格中(填编号):
①渗析 ②盐析 ③聚沉 ④溶胶 ⑤凝胶 ⑥布朗运动 ⑦电泳 ⑧丁达尔现象 ⑨中和 ⑩水解
(1)肥皂水中透过强光,可以见到光亮的“通路”。这种现象称为___________。
(2) 在制取肥皂时,加入食盐细粒使肥皂析出,这个过程称为_____________。
(3)在肥皂水中滴加酚酞,溶液变成红色,说明高级脂肪酸根离子发生了______________。
(4)在氢氧化铁胶体中加入浓硫酸铵溶液,产生红褐色沉淀,这种现象叫做_____________。
(5)用半透膜把制取的氢氧化铁胶体中含有的NaCl分离出来的方法叫做___________。
18.将Mg、Cu组成的混合物26.4g投入到适量的稀硝酸中,固体完全溶解,收集到标准状况下的NO气体8.96L,向反应后的溶液中加入过量的5mol·L-1的NaOH溶液300mL,金属离子完全沉淀。则形成沉淀的质量是 ( )
A.43.2g B. 46.8g C. 53.6g D. 63.8g
第Ⅱ卷(非选择题 共54分)
17.食品香精菠萝酯的生产路线(反应条件略去)如下:
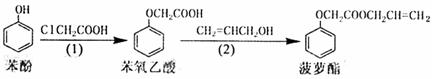
下列叙述错误的是 ( )
A.步骤(1)产物中残留的苯酚可用FeCl3溶液检验
B.苯酚和菠萝酯均可与酸性KMnO4溶液发生反应
C.苯氧乙酸和菠萝酯均可与NaOH溶液发生反应
D.步骤(2)产物中残留的烯丙醇可用溴水检验
16.在甲、乙、丙、丁四个烧杯内分别放入0.1mol的钠、氧化钠、过氧化钠和氢氧化钠,然后各加入100mL水,搅拌,使固体完全溶解,则甲、乙、丙、丁所得溶液里溶质的质量分数大小顺序是 ( )
A.甲<乙<丙<丁 B.丁< 甲<乙=丙 C.甲=丁<乙=丙 D.丁<甲<乙<丙
15.某二价金属的碳酸盐和酸式碳酸盐的混合物,跟足量的稀盐酸反应,消耗H+和生成CO2物质的量之比为6:5,则该混合物中碳酸盐和酸式碳酸盐的物质的量之比是 ( )
A.1:1 B.1:2 C.1: 3 D.1:4
14.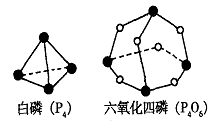 化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1 mol化学键时释放(或吸收)的能量。已知白磷(P4)和P4O6的分子结构如下图所示:
化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1 mol化学键时释放(或吸收)的能量。已知白磷(P4)和P4O6的分子结构如下图所示:
现提供以下化学键的键能:P-P 198KJ·mol-1、P-O 360kJ·mol-1、O=O 498kJ·mol-1。则P4+3O2=P4O6的反应热△H为 ( )
A.+1638 kJ·mol-1 B.一1638 kJ·mol-1
C.-126 kJ·mol-1 D.+126 kJ·mol-1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com